
科目: 来源: 题型:解答题
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | ||
| B | 甲烷(甲醛) | ||
| C | 乙酸乙酯(乙酸) | ||
| D | 淀粉(氯化钠) | . |
查看答案和解析>>
科目: 来源: 题型:单选题

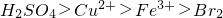

查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:多选题
 )与碳酸氢钠溶液反应:
)与碳酸氢钠溶液反应: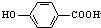 +HCO3-→
+HCO3-→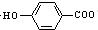 -+CO2↑+H2O
-+CO2↑+H2O查看答案和解析>>
科目: 来源: 题型:解答题
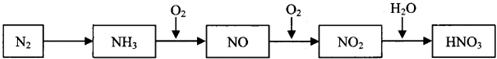
查看答案和解析>>
科目: 来源: 题型:解答题
| 读数次数 | 质量/g | |
| 第1次 | 196.30 | |
| 第2次 | 196.15 | |
| 锥形瓶十水十试样 | 第3次 | 196.05 |
| 第4次 | 196.00 | |
| 第5次 | 196.00 |

查看答案和解析>>
科目: 来源: 题型:解答题
 MnCl2+Cl2↑+2H2O; B.SO2+2H2S=2H2O+3S↓;
MnCl2+Cl2↑+2H2O; B.SO2+2H2S=2H2O+3S↓;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com