
科目: 来源:09真题汇编-物质的制备、分离与提纯、鉴别与检验 题型:实验题
(10分)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。与Cl2比,ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
(1)在ClO2的制备方法中,有下列两种制备方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O:
用方法二制备的ClO2更适合用于饮用水的消毒,其主要原因是 。
(2)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子
(ClO2-)。2001年我国卫生部规定,饮用水中ClO2-的含量应不超过0.2mg·L-1。
饮用水中ClO2、ClO2-的含量可用连续碘量法进行测定。ClO2被I-还原为ClO2-、Cl-的转化率与溶液pH的关系如图所示。
当pH≤2.0时,ClO2-也能被I-还原成Cl-。
反应生成的I2用标准Na2S2O3溶液滴定:
Na2S2O3+I2=Na2S4O6+2NaI
①请写出pH≤2.0时,ClO2-与I-反应的离子方程式 。
②请完成相应的实验步骤:
步骤1:准确量取VmL水样加入到锥形瓶中。
步骤2:调节水样的pH为7.0~8.0。
步骤3:加入足量的KI晶体。
步骤4:加入少量淀粉溶液,用cmol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3
溶液V1mL。
步骤5: 。
步骤6:再用cmol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL。
③根据上述分析数据,测得该饮用水样中ClO2-浓度为 mol·L-1用含字母的代数式表示)
④若饮用水中ClO2-的含量超标,可向其中加入适量的Fe2+将ClO2-还原成Cl-,
该反应的氧化产物是 (填化学式)。
查看答案和解析>>
科目: 来源:2011-2012学年云南景洪第一中学高一上期末考试化学试卷(带解析) 题型:计算题
实验室要用4 mol·L-1的浓硫酸配制500 mL 0.2 mol·L-1的稀H2SO4溶液。
(1).实验中所需用到的主要玻璃仪器有:量筒、烧杯、玻璃棒、 、 等。
(2).需用浓度为4mol/L的浓硫酸的体积为多少mL?
(3).取20 mL该稀溶液,然后加入足量的锌粒,求生成的气体体积(标况下)。
查看答案和解析>>
科目: 来源:2013届浙江省金华一中高三12月月考化学试卷(带解析) 题型:计算题
(15分)淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去):实验过程如下:①将1∶1的淀粉水乳液与少许硫酸(98%)加入烧杯中,水浴加热至85℃~90℃,保持30 min,然后逐渐将温度降至60℃左右;②将一定量的淀粉水解液加入三颈烧瓶中;③控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3、98%H2SO4的质量比为2:1.5)溶液;④反应3h左右,冷却,减压过滤后再重结晶得草酸晶体。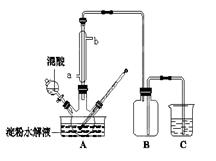
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O 3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
请回答下列问题:
(1)实验①加入98%硫酸少许的目的是: 。
(2)冷凝水的进口是 (填a或b);实验中若混酸滴加过快,将导致草酸产量下降,其
原因是 。
(3)检验淀粉是否水解完全所用的试剂为 。
(4)草酸重结晶的减压过滤操作中,除烧杯,玻璃棒外,还必须使用属于硅酸盐材料的仪器有
(5)当尾气中n(NO2):n(NO)=1:1时,过量的NaOH溶液能将NOx全部吸收,发生的化学反应方程式为: 。
(6) 将产品在恒温箱内约90℃以下烘干至恒重,得到二水合草酸。用KMnO4标准溶液滴定,该反应的离子方程式为:2MnO4- + 5H2C2O4 + 6H+ = 2Mn2+ + 10CO2↑+ 8H2O
称取该样品0.12 g,加适量水完全溶解,然后用0.020 mol·L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),此时滴定终点的现象为 。滴定前后滴定管中的液面读数如图所示,则该草酸晶体样品中二水合草酸的质量分数为 。
查看答案和解析>>
科目: 来源:2011-2012学年广东省汕头金山中学高一第一学期期末考试化学试卷 题型:计算题
(15分)为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
① ② ③ ④ ⑤
称取粗盐

 滤液
滤液
⑥ ⑦
 精盐
精盐
(1)判断BaCl2已过量的方法是
(2)第④步中,相关的离子方程式是
(3)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是
(4)为检验精盐纯度,特配制150 mL 0.2 mol·L—1 NaCl溶液,下图是该同学转移溶液的示意图,图中的错误是 
(5)提纯过程中步骤①⑤⑦都用到相同的仪器,名称:
这三个步骤中还需要用到的属于硅酸盐材料的仪器有 (填写仪器名称)
查看答案和解析>>
科目: 来源:2011-2012学年宁夏中卫市海原一中高一第二学段考试化学试卷 题型:计算题
(5分)实验室用8.7g的MnO2与足量的浓盐酸制取氯气:求生成氯气的体积(标准状况)和被氧化的HCl的物质的量。
查看答案和解析>>
科目: 来源:2010—2011学年四川省攀枝花市米易中学高二4月月考化学试卷 题型:计算题
(12分)某化学课外小组用下图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
(1) 写出A中反应的化学方程式______________________
(2) 实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡;
目的是______ ___,写出有关的化学方程式:_______________ ____
(3) C中盛放CCl4的作用是 。
(4)能证明苯和液溴发生的是取代反应,而不是加成反应,可向
试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验
证的方法是向试管D中加入______ ___,现象是 。
查看答案和解析>>
科目: 来源:2011-2012学年浙江省温州市十校联合体高二下学期期末考试化学试卷(带解析) 题型:问答题
(12分)以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:

氯化铵和硫酸钠的溶解度随温度变化如上图所示。回答下列问题:
(1)写出制备 NH4Cl的化学方程式: 。
(2)实验室进行蒸发浓缩用到的主要仪器有 、带铁圈的铁架台、玻璃棒、酒精灯等。
(3)实验过程中趁热过滤的目的是 。冷却结晶后的过滤采用抽滤,其装置如图1所示,请指出该装置中的错误之处 ;

图1 图2
(4)趁热过滤后,滤液冷却结晶。一般情况下,下列哪些因素有利于得到较大的晶体 。
| A.缓慢冷却溶液 | B.溶液浓度较高 |
| C.溶质溶解度较小 | D.缓慢蒸发溶剂 |
查看答案和解析>>
科目: 来源:2012-2013学年北京市西城区(北区)高一上学期期末考试化学试卷(带解析) 题型:填空题
某课外小组同学用下图所示装置进行实验(夹持装置已省略)。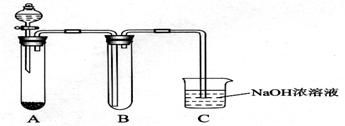
(1)用该装置制备NO2并研究其性质。
①收集一试管NO2,取下试管B倒立在水中,观察到的现象是________________。
②该反应的化学方程式是________________________________。
③C中NaOH溶液吸收NO2,生成两种盐,且被氧 化与被还原的NO2的物质的量之比是1:1,请写出该反应的离子方程式________________________________。
(2)该装置也可用于制备Cl2并研究其性质。
①若A中固体为漂白粉,滴入浓盐酸,则A中发生反应的化学方程式是___________。
②在B中放一小块湿润的淀粉碘化钾试纸,可观察到试纸变蓝,请结合离子方程式解释原因________________________________________。
③硫代硫酸钠(Na2S2O3)可替代NaOH溶液吸收氯气,已知25.0mL 0.1 mol·L-1的Na2S2O3溶液恰好把标准状况下224 mL Cl2完全转化为Cl-时,S2O32-转化成_____(填选项)。
a. S2- b. S c. SO32- d. SO42-
查看答案和解析>>
科目: 来源:2012-2013学年新疆兵团农二师华山中学高一上学期期末考试化学试卷(带解析) 题型:填空题
实验室要用98%(ρ=1.84g·cm-3)的硫酸配制3.68mol·L-1的硫酸溶液500mL
(1)需准确量取98%的硫酸 mL。
(2)准确量取一定体积的98%的硫酸后,要配制3.68mol·L-1的硫酸溶液500mL,必须用到的实验仪器是(填写序号): .
①500mL量筒 ②烧杯 ③1000mL容量瓶 ④500mL 容量瓶
⑤天平 ⑥胶头滴管 ⑦锥形瓶 ⑧玻璃棒
(3)若配制3.68mol·L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,将例所配制的硫酸溶液浓度的影响(偏高,偏低,或不变)
| A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒 |
| B.将烧杯内的稀硫酸向容量瓶中转移时,因操作不当使部分稀硫酸溅出瓶外。 |
| C.用胶头滴管向容量瓶中加水时溶液凹液面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切。 |
| D.用胶头滴管加水时,仰视观察溶液凹液面与容量瓶刻度相切。 |
查看答案和解析>>
科目: 来源:2012-2013学年黑龙江友谊县红兴隆第一高级中学高二6月月考化学卷(带解析) 题型:填空题
芳香族化合物A只有两个对位取代基,在一定条件下有如下图所示转化关系。其中,1 mol C与Na完全反应生成1 mol H2,若l mol C与NaHCO3完全反应,也产生l mol气体,E可以使溴的四氯化碳溶液褪色。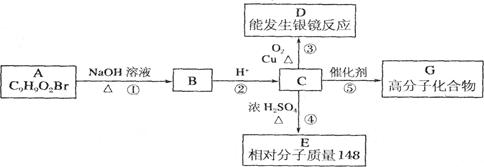
(1)D分子中的含氧官能团名称是___________,A的结构简式是___________。
(2)反应④的基本类型是_______反应,反应⑤的化学方程式是___________________________ 。
(3)与C取代基位置相同,既能与FeCl3溶液显色、又能发生水解反应的结构简式为: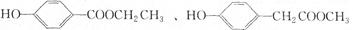 ,______________________、_____________________。(写两种即可)
,______________________、_____________________。(写两种即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com