
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验序号 | 双氧水体积 | 催化剂 | 待测数据 |
| a | 15mL | 无 | |
| b | 15mL | 0.5g CuO | |
| c | 15mL | 0.5g MnO2 |

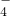 +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
| 选项 | A | B | C | D |
| 添加成分 | Co2O3(氧化钴) | Cu2O | Fe2+ | PbO |
| 玻璃的色彩或性能 | 蓝色 | 红色 | 钢化玻璃 | 光学玻璃 |
查看答案和解析>>
科目: 来源: 题型:解答题
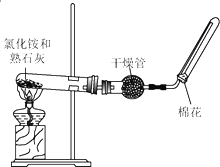 为探究氨气的一些性质,同学们做了以下两个实验.
为探究氨气的一些性质,同学们做了以下两个实验.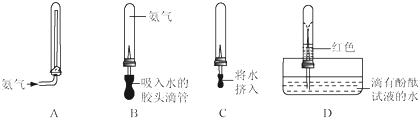
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com