
科目: 来源:2011届河南省五市高中高三毕业班第二次联考(理综)化学部分 题型:填空题
研究化学反应原理对生产生活很有意义,请用化学反应原理的相关知识回答下列问题: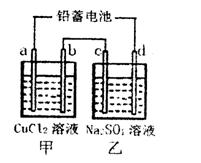
(1)用铅蓄电池电解甲、乙两电解池中的溶液。已知铅蓄电池的总反应为:Pb(s)+PbO2(s)+2H2SO4(aq)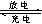 2PbSO4(s)+2H2O(1)。电解一段时间后,向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是______
2PbSO4(s)+2H2O(1)。电解一段时间后,向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是______ ______
______
(填写序号)
| A.d极为阴极 |
| B.若利用甲池精炼铜,b极应为粗铜 |
| C.放电时铅蓄电池负极的电极反应式为: PbO2(s)+4H+(aq)+ 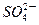 (aq)+4e- (aq)+4e- PbSO4(s)+2H2O(1) PbSO4(s)+2H2O(1) |
| D.若四个电极材料均为石墨,当析出6.4g Cu时,两池中共产生气体3.36L(标准 |
 H++A2-,请回答下列问题:
H++A2-,请回答下列问题: mol·L-1的NaHA溶液的pH=2,则0.1mol·L-1的H2A溶液中氢离子的物质的量浓度可能是__________0.1lmol·L-1(填“<”、“>”或“=”),理由是:___________________________.
mol·L-1的NaHA溶液的pH=2,则0.1mol·L-1的H2A溶液中氢离子的物质的量浓度可能是__________0.1lmol·L-1(填“<”、“>”或“=”),理由是:___________________________. CH3OH(g); △H=-90.8kJ·mol-1
CH3OH(g); △H=-90.8kJ·mol-1 CH3OH(g)
CH3OH(g) CH3OCH3(g)+H2O(g); △H=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g); △H=-23.5kJ·mol-1 CO2(g)+H2(g);△=-41.3kJ·mol-1
CO2(g)+H2(g);△=-41.3kJ·mol-1 2SO3(g)。在一定温度下,将0.23 mol SO2和0.11 mol氧气放入容积为l L的密闭容器中发生反应,达到平衡后得到0.12 mol SO3,则反应的平衡常数K=________。若温度不变,再加入0.50 mol氧气后重新达到平衡,则SO3的体积分数将___________(填“增大”、“不变”或“减小”)。
2SO3(g)。在一定温度下,将0.23 mol SO2和0.11 mol氧气放入容积为l L的密闭容器中发生反应,达到平衡后得到0.12 mol SO3,则反应的平衡常数K=________。若温度不变,再加入0.50 mol氧气后重新达到平衡,则SO3的体积分数将___________(填“增大”、“不变”或“减小”)。查看答案和解析>>
科目: 来源:2011届江西省吉安市高三第三次模拟考试(理综)化学部分 题型:填空题
现有某金属硝酸盐化学式为M(NO3)2,为了探究其热分解产物,某化学小组开展探究性学习:
金属活泼性不同,其硝酸盐分解产物不同。如 :2KNO3
:2KNO3 2KNO2+O2↑
2KNO2+O2↑
2Cu(NO3)2 2CuO+4NO2↑+O2↑,2AgNO3
2CuO+4NO2↑+O2↑,2AgNO3 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑
猜想1:M(NO3)2 M(NO2)2+O2↑
M(NO2)2+O2↑
猜想2:2M(NO3)2 2MO+4NO2↑+O2↑
2MO+4NO2↑+O2↑
猜想3:(此处不写) 。
为了探究上述猜想,设计如下实验装置:
实验步骤:①连接仪器;②检查装置气密性;③取一定量的样品装于大试管中,并重新连接好 仪器;④加热;⑤……
(1)写出猜想3的化学方程式:  ;
;
(2)测定气体体积应选择 (填A或B);
(3)实验收集到一定量气体,为了检验收集到的气体的成分,其操作方法是 ;
(4)在实验后的水里加入适量碳酸氢钠粉末,溶液中产生大量气体,说明 正确(填:猜想l、猜想2或猜想3);
(5)该小组测得一组数据:实验前样品质量为Wg,收集到气体体积为VL(已折算成标准状况 ),则M的相对原子质量为____;
),则M的相对原子质量为____;
(6)已知4Fe(NO3)2 2Fe2O3+8NO2↑+O2↑,现在对KNO3、Cu(NO3)2、Fe(NO3)2 的混合粉末充分加热后未收集到任何气体,则KNO3、Cu(NO3)2、Fe(NO3)2的物质的量之比可能是 ( )
2Fe2O3+8NO2↑+O2↑,现在对KNO3、Cu(NO3)2、Fe(NO3)2 的混合粉末充分加热后未收集到任何气体,则KNO3、Cu(NO3)2、Fe(NO3)2的物质的量之比可能是 ( )
A.1:2:2 B.2:1:4 C.1:2:3 D.3:8:6
查看答案和解析>>
科目: 来源:2011届西藏拉萨中学高三第七次月考(理综)化学部分 题型:填空题
已知向FeCl3浓溶液中加入Na2CO3浓溶液,可以观察到产生红褐色沉淀和无色气体,写出该反应的离子方程式 。
从形式上看,Na2SO3和Na2CO3相似,那么Na2SO3和FeCl3之间的反应情况又如何呢?某化学研究性学习小组提出了两种可能:一是发生氧化还原反应:2Fe3++SO32-+H2O=2Fe2++SO42-+2H+;二是发生双水解反应:2Fe3++3SO32-+6H2O=3Fe(OH)3(胶体)+3H2SO3; 为了弄清楚发生的是那一种反应发生,同学们设计并实施了下列实验,请填写下列空白:
实验Ⅰ:实验用品 Na2SO3浓溶液、BaCl2稀溶液、稀盐酸、试管若干、胶头滴管若干。从选择的药品分析,实验者设计这个实验的目的是 。
实验Ⅱ:取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液的颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3浓溶液至过量,溶液的颜色加深,最终变为红褐色。这种红褐色物质是 。向红褐色物质中逐滴加入稀盐酸至过量,可以观察的现象是 。将溶液分成两等份,其中一份加入KSCN溶液,溶液变成血红色,反应的离子方程式为: 。另一份加入BaCl2稀溶液,有少量白色沉淀生成,反应的离子方程式为: 。
实验Ⅲ:换用稀FeCl3和Na2SO3溶液重复实验Ⅱ,产生的现象完全相同。
由上述试验得出的结论是 。
查看答案和解析>>
科目: 来源:2011届山东省兖州市高三第三次模拟考试(理综)化学部分 题型:填空题
实验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体。
(1)为了节约原料,硫酸和硝酸的物质的量之比最佳为: ;为了吸收该反应中产生的尾气,请选择下列中合适的装置 。
(2)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:以空气为氧化剂法
方案1:以空气为氧化剂。将铜粉在仪器B中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,即发生反应,生成硫酸铜。反应完全后,加物质甲调节pH ,铁元素全部沉淀(一般认为铁离子的浓度下降到10-5mol·L-1,就认为沉淀完全),然后过滤、浓缩、结晶。
已知:Ksp[Cu((OH)2]≈10-22, Ksp[Fe((OH)2]≈10-16, Ksp[Fe((OH)3]≈10-38
请回答下列问题:
如开始加入的铜粉为3.2 g,最后所得溶液为500 mL,溶液中含有铁元素0.005 mol。
①方案1中的B仪器名称是 。
②为了使铁元素全部沉淀,应调节pH至少为_________。
③方案2中甲物质可选用的是 。
| A.CaO | B.NaOH | C.CuCO3 | D.Cu2(OH)2CO3 E、Fe2(SO4)3 |
查看答案和解析>>
科目: 来源:2011届浙江省台州市高三调考试题(理综)化学部分 题型:填空题
阿司匹林(乙酰水杨酸)已应用百年,成为医药史上三大经典药物之一,至今它仍是世界上应用最广泛的解热、镇痛和抗炎药,也是作为比较和评价其他药物的标准制剂。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成该物质,设计的合成路线为:
一、制备K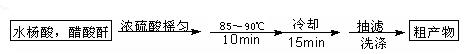 s*5u
s*5u
二、提纯
方案1
方案2
主要试剂和产品的物理常数
| 名 称 | 相对分子质量 | 熔点或沸点(0C) | 水 | 醇 | 醚 |
| 水杨酸 | 138 | 158(熔点) | 微溶 | 易溶 | 易溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 反应 | 可溶 | 易溶 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 | 可溶 | 微溶 |

查看答案和解析>>
科目: 来源:2011届广东省广州市普通高中毕业班综合测试(二)(理综)化学部分 题型:填空题
已知FeSO4在不同条件下分解得到的产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2。某研究小组探究在酒精喷灯加热条件下FeSO4分解的气体产物。已知SO3的熔点是16.8℃,沸点是44.8℃。
(1)装置Ⅱ的试管中不装任何试剂,其作用是_______________________,试管浸泡在50℃的水浴中,目的是________________________________。
(2)装置Ⅲ和装置Ⅳ的作用是探究本实验气体产物成分。请完成实验设计,填写检验试剂、预期现象与结论。
限选试剂:3 mol·L-1 H2SO4、6 mol·L-1 NaOH、0.5 mol·L-1 BaCl2、0.5 mol·L-1 Ba(NO3)2、0.01 mol·L-1酸性KMnO4溶液、0.01 mol·L-1溴水。
| 检验试剂 | 预期现象和结论 |
| 装置Ⅲ的试管中加入________________。 | 产生大量白色沉淀,证明气体产物中含有SO3。 |
| 装置Ⅳ的试管中加入________________。 | ______________________________ ______________________________ ______________________________ ______________________________ |
查看答案和解析>>
科目: 来源:2011届云南省高三第二次毕业生复习统一检测(理综)化学部分 题型:填空题
常温下,用 0.1000 mol L-1NaOH溶液滴定 20.00 ml0.1000 mol.L-1CH3COOH溶液,所得滴定曲线如下图所示。
请回答:
(1) 有人认为,C点时NaOH与CH3COOH恰好完全反应,这种看法是否正确______?(选填“是”或“否”),理由是________________________;
(2) 关于该滴定实验,从下列选项中选出最恰当的一项____ (选填字母);
(3) 在B点时,溶液中 ________
________ (选填“>”、“<”或“=”);
(选填“>”、“<”或“=”);
(4) 在A?D区间内,下列大小关系可能存在的是________;
①
②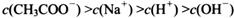
③
④
(5) 若向该醋酸溶液中加入少量的醋酸钠晶体,则溶液的pH会____(选填“增大”、“减小”或“不变”);
(6) 常温下,用该NaOH溶液滴定25.00 mL—定浓度的某稀H2SO4溶液,达到滴定终点时消耗NaOH溶液的体积为25.00 mL,则该稀H2SO4溶液的pH=____。
查看答案和解析>>
科目: 来源:2010—2011学年山东省德州一中高二下学期期中考试化学试卷A 题型:填空题
(4分)下列实验的操作或所用的试剂有错误的是
| A.实验室制取乙烯气体时,将温度计的水银球放入液面以下 |
| B.可用酒精洗涤沾有苯酚的试管 |
| C.证明分子CH2=CH-CHO既含有醛基又含有C=C,可先向溶液中加入足量的银氨溶液加热,充分反应后,再加入足量的溴水 |
D.配制银氨溶 液时,将硝酸银 液时,将硝酸银 溶液逐滴滴入氨水中 溶液逐滴滴入氨水中 |
查看答案和解析>>
科目: 来源:2011届河北省邢台市高三第一次模拟考试(理综)化学部分 题型:填空题
以黄铜矿(CuFeS2)为原料冶炼铜的反应为:
8CuFeS2+21O2

(1)若Cu为+2价,则反应中每生成1molCu需要转移 mol电子。
(2)为综合利用炉气中的大量SO2,下列方案合理的是 。
a.用浓硫酸吸收 b.用于制备硫酸
c.高空排放 d.用纯碱液吸收制亚硫酸钠
(3)为检验所得矿渣是中是否含有FeO、Fe2O3、CuO、A12O3、SiO2等氧化物,进行了以下实验;
①取一定量矿渣粉末,加入适量浓硫酸后加热,固体全部溶解,得溶液A;将产生的气体通入品红溶液中,溶液褪色。由此判断矿渣中一定含有 ,一定没有 。
②将溶液A稀释后分成两份,取其中一份,加入过量NaOH溶液,有沉淀产生,静置后取上层清液,通入过量的CO2溶液变浑浊。由此判断出矿渣中含有 ,写出通入过量的CO2所发生反应的离子方程式: 。
③取另一份溶液A加入过量的铁粉充分反应后过滤,得到的固体中有红色物质,由此判断矿渣中有 ,写出此步操作中得到红色物质所发生反应的离子方程式 。
查看答案和解析>>
科目: 来源:2011届江苏省抚州调研室高三模拟考试(理综)化学部分 题型:填空题
Ⅰ.现在四种化学仪器:
| A.量筒 | B.容量瓶 | C.滴定管 | D.烧杯 |
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
| 实验步骤 | 实验操作 | 实验操作目的 |
| 步骤1 | | |
| 步骤2 | | |
| 步骤3 | | |
| 步骤4 | 洗涤沉淀 | |
| 步骤5 | | 得到FeSO4溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com