
科目: 来源:2012届辽宁省铁岭中学高三上学期第三次月考化学试卷 题型:实验题
黄铁矿的主要成分是FeS2。测定黄铁矿中FeS2含量的两种方法如下图所示:
已知:
①王水是由1体积的浓硝酸(ρ=1.42g·cm-3)和3体积的浓盐酸(ρ=1.19g·cm-3)混合而成的。
②黄铁矿和王水反应的方程式为Fe S2+5HNO3+3HCl=FeCl3+2H2SO4+5NO↑+2H2O
S2+5HNO3+3HCl=FeCl3+2H2SO4+5NO↑+2H2O
请回答下列问题:
(1)简述实验室配制王水的操作过程_____________________________________
(2)方法一中过滤、洗涤、灼烧都用到的仪器是_______________。
(3)方法二中要判断BaCl2溶液是否过量,可向滤液中加入X溶液,X可以是____(填代号)
| A.NaOH | B.BaCl2 | C.HCl | D.Na2SO4 |

 ,则该矿石中FeS2的质量分数是________________。
,则该矿石中FeS2的质量分数是________________。查看答案和解析>>
科目: 来源:2012届江西省汾阳中学高三第三次月考化学试卷 题型:实验题
(10分).某课外活动小组学生模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),设计用下图所示的仪器来制取氧气并测量氧气的体积上图中量气装置E是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水。甲管有刻度(0~50mL),供量气用;乙管可上下移动,以调节液面高低。
实验室可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水
试回答:(1)上述装置的连接顺序是(填各接口的编号,其中连接胶管及夹持装置均省略):___________。
(2)装置C中放入的反应物是__________和__________。
(3)装置A的作用是__________,装置B的作用是__________。
(4)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数,求其差值的过程中,应注意____________和____________(填写字母编号)。
a.视线与凹液面最低数相平
b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平
d.读数时不一定使甲、乙管液面相平
查看答案和解析>>
科目: 来源:2012届福建省福州三中高三上学期期中考试化学试卷 题型:实验题
(12分)某研究性学习小组为测定,13.7g某Na2CO3样品的纯度(其中只含NaHCO3杂质),选用下图所示的仪器装置进行实验(②装置未画全)。试回答有关问题: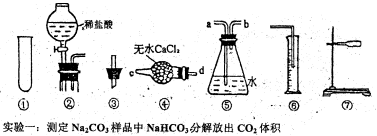
(1)请选择适当的仪器,连接装置的正确顺序是_ 。
(2)加热时NaHC03分解的化学方程式为 。
(3)完成该实验尚缺的玻璃仪器是 (填名称);产生气体从装置④的 进入,从装置⑤的 进入(填接口序号)。
实验二:测定上述实验完成后剩余固体与盐酸反应产生CO2的体积。
(4)加热后的固体与足量盐酸反应的离子方程式为 。
数据分析及结论:
(5)加入盐酸至无气体产生时,生成CO2体积在标准状况时为2.24L,则Na2CO3样品的纯度为 。
误差分析:
(6)有同学认为实验一⑤中用水会使测量结果产生误差,你认为原因可能是 。
(7)有同学发现在实验—读取CO2体积时,⑥中液体的液面低于⑤中液体的液面,但未做任何处理,则a值 (填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目: 来源:2012届湖南省衡阳八中高三第四次月考化学试卷 题型:实验题
(12分)已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性。
用如图所示装置进行Mg和SO2反应的实验。 (1)选择制取SO2的最合适试剂 (填序号)。
(1)选择制取SO2的最合适试剂 (填序号)。
①10%的H2SO4溶液 ②80%的H2SO4溶液
③Na2SO3固体 ④CaSO3固体
(2)写出装置乙和B中发生的主要反应的化学方程式:
乙中 
 ;
;
B中 。
装置C中NaOH溶液的作用是 。
(3)你认为该装置是否有不足之处? 。如果有,请说明 。
查看答案和解析>>
科目: 来源:2012届湖南省湖南师大附中高三第三次月考化学试卷 题型:实验题
(10分)某化学研究性学习小组拟测定食醋的总酸量(g/10mL),请你参与该小组 的实验并回答相关问题。
的实验并回答相关问题。
[实验目的]测定食醋的总酸量
[实验原理]中和滴定
[实验用品]蒸馏水,市售食用白醋样品500mL(商标注明总酸量:3.50g/100mL~5.00g/100mL),0.1000mol/L NaOH标准溶液;100mL容量瓶,10mL移液管,碱式滴定管,铁架台,滴定管夹,锥形瓶,烧杯,酸碱指示剂(可供选用的有:甲基橙,酚酞,石蕊)。
[实验步骤]
①配制并移取待测食醋溶液
用10mL移液管吸取10mL市售白醋样品置于100mL容量瓶中,用处理过的蒸馏水稀释至刻度线,摇匀后用酸式滴定管取待测食醋溶液20mL,并移至锥形瓶中。
②盛装标准NaOH溶液
将碱式滴定管洗净后,用NaOH标准溶液润洗3次,然后加入NaOH标准溶液,排 除尖嘴部分气泡后,使液面位于“0”刻度或“0”度以下。静置,读取数据并记录为NaOH标准溶液体积的初读数。
除尖嘴部分气泡后,使液面位于“0”刻度或“0”度以下。静置,读取数据并记录为NaOH标准溶液体积的初读数。
③滴定
往盛有待测食醋溶液的锥形瓶中的滴加某酸碱指示计2~3滴,滴定至终点。记录NaOH的终读数。重复滴定3次。
[数据记录]
[问题与思考]
(1)步骤①中用煮沸并迅速冷却的方法处理蒸馏水的目的是除去 ,防止其对实验结果的影响。
(2)步骤③中你选择的酸碱指示剂是 ,理由是 。
(3)样品总酸量= g/100mL。
(4)导致实验结果偏大的主 要原因是 (填写序号)
要原因是 (填写序号)
①滴定终点时,仰视滴定管读数
②滴定后滴定管尖嘴处悬有一滴液体
③移液管用蒸馏水洗净后,就用来 吸取待测液
吸取待测液
④滴定前,碱式滴定管无气泡,滴定后产生气泡
⑤锥形瓶只用蒸馏水洗涤后仍留有少量蒸馏水
查看答案和解析>>
科目: 来源:2012届黑龙江省绥棱县第一中学高三11月月考化学试卷 题型:实验题
(10分)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
| 实验编号 | HA物质的量浓度(mol·L-1) | NaOH物质的量浓度(mol·L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
 2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2________(选填“是”或“否”)。混合液中离子浓度c(A-)与 c(Na+)的大小关系是__________
2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2________(选填“是”或“否”)。混合液中离子浓度c(A-)与 c(Na+)的大小关系是__________
 l·L-1。
l·L-1。查看答案和解析>>
科目: 来源:2011-2012学年山东省济宁市邹城二中高一上学期期中质量检测化学试卷 题型:实验题
(10分)某活动课程小组拟用50 mL NaOH溶液吸收CO2气体,制备Na2CO3溶液.为了防止通入过量的CO2气体生成NaHCO3,设计了如下实验步骤:
a.取25 mL  NaOH溶液吸收过量的CO2气体,至CO2
NaOH溶液吸收过量的CO2气体,至CO2 气体不再溶解;
气体不再溶解;
b.小火煮沸溶液1~2 min,赶走溶解在溶液中的CO2气体;
c.在得到的溶液中加入另一半(25 mL)NaOH溶液,使其充分混合反应.
(1)此方案能制得较纯净的Na2CO3,写出c步骤的离子方程式_________________.
此方案第一步的实验装置如下图所示:
(2)加入反应物前,如何检验整个装置的气密性:________________________ ________________________________________________
(3)若用大理石与盐酸制CO2,则装置B中盛放 的试剂是_____
的试剂是_____  _,作用是_____________________________________________
_,作用是_____________________________________________
(4)在实验室通常制法中,装置A还可作为下列______ (填序号)气体的发生装置.
①HCl ②H2 ③O2 ④NH3
(5)已知所用NaOH溶液中溶质的质量分数为40%,室温下该溶液密度为1.44 g/mL,假设反应前后溶液的体积不变,不考虑实验误差,计算用此种方法制备所得Na2CO3溶液的物质的量浓度为_______ mol/L.
查看答案和解析>>
科目: 来源:2012届重庆市万州二中高三上学期期中考试理科综合试题(化学部分) 题型:实验题
(18分)测定SO2转化成SO3的转化率可以用下图装置,装置中烧瓶内发生的化学反应方程式为:Na2SO3(s)+H2SO4(85%)=Na2SO4+H2O+SO2↑。
(已知SO3的熔点是16.8℃,沸点是44.8℃) 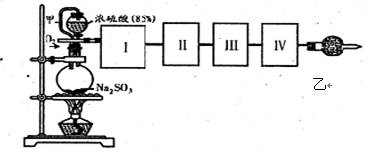
(1)装置中甲管的作用是 ;
乙装置的作用是 。
(2)根据实验需要,应该在I、II、Ⅲ、IV处连接合适的装置,请从下图A~E装置中选择最适合装置并将其序号填放下面的空格中。I、Ⅱ、Ⅲ、Ⅳ处连接的装置分别是 、 、 、 。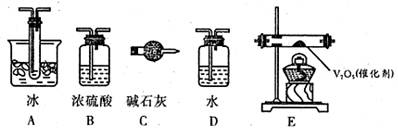
(3)为使SO2有较高的转化率,实验中加热 催化剂与滴加浓硫酸的顺序中,应采取的操作
催化剂与滴加浓硫酸的顺序中,应采取的操作 是 ,若用大火加热烧瓶时,SO2的转化率会 (填“升高”、“不
是 ,若用大火加热烧瓶时,SO2的转化率会 (填“升高”、“不 变”或“降低”)。
变”或“降低”)。
(4)将SO2通入含1 mol氯酸的溶液中,可生成一种强酸和一种氧化物,并有6.02×1023个电子转移,则该反应的化学方程式为 。
(5)用nmolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅳ增重了mg,则实验中SO2的转化率为 。(用含m、n的代数式填写)
查看答案和解析>>
科目: 来源:2012届重庆市万州二中高三上学期期中考试理科综合试题(化学部分) 题型:实验题
(15分)从固体混合物A出发可以发生如下框图所示的一系列变化。
(1)在实验室,气体C的检验方法是 。 (2)操作②的名称是 ,该操作所使用的玻璃仪器有 。
(3)写出下列反应的离子方程式:
反应③ ;
反应④ 。
(4)实验中多余的气体I必须吸收,以免污染空气。下图是实验室用NaOH吸收气体I的装置,为防止产生倒吸现象,不合理的装置是 (填序号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com