
科目: 来源:2011-2012学年云南蒙自高中高一上学期10月教学质量监测化学试卷 题型:实验题
(14分)把18.0mol·L-1的浓硫酸稀释成2.00mol·L-1的稀硫酸100ml,实验操作如下:
| A.将配好的稀硫酸倒入试剂瓶中,贴好标签; |
| B.盖好容量瓶塞,反复颠倒,摇匀; |
| C.用量筒量取ml的18.0mol·L-1的浓硫酸; |
| D.将浓硫酸沿烧杯内壁慢慢注入盛有少量水的烧杯中; |
查看答案和解析>>
科目: 来源:2012届福建省惠安高级中学高三第三次月考化学试卷(解析版) 题型:实验题
硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放。某校兴趣小组欲测定硫酸工业尾气中二氧化硫含量,采用以下方案:
甲方案:如下图所示,图中气体流量计B用于准确测量通过尾气的体积。将尾气通入一定体积已知浓度的碘水中测定二氧化硫的含量。
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验准确度,其理由是:
。
(2)洗气瓶C中的溶液可以用其他试剂替代,请你举出一种: 。
(3)本实验的关键在于关闭气体流量计的时机,请问应当在什么时候关闭活塞A: 。
乙方案:实验步骤如以下流程图所示:
(4)写出步骤①中反应的化学方程式  。
。
(5)如何判断步骤②中沉淀是否完全的方法 。
(6)通过的尾气体积为VL(已换算成标准状况)时,该尾气中二氧化硫含量(体积分数)
为 (用含有V、m的代数式表示)。
丙方案:将乙方案中步骤①省略,直接将尾气通入过量Ba(OH)2溶液,其余步骤与方案乙相同。
(7)你认为丙方案是否合理,说明理由:
。
查看答案和解析>>
科目: 来源:2011-2012学年云南大理云龙一中高二上学期期末考试化学试卷 题型:实验题
(12分)50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
(1)烧杯间填满碎泡沫塑料的作用是_________ ______________________
(2)大烧杯上如不盖硬纸板,求得的中和热数值________(填“偏大”“偏小”“无影响”)。
(3)实验中改用60 mL 0.50 mol·L-1盐酸进行反应,与上述实验相比,所放出的热量________(填“相等”、“不相等”),所求中和热__________(填“相等”、“不相等”),简述理由___
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会________(填“偏大”、“偏小”“无影响”)。
查看答案和解析>>
科目: 来源:2012届山东省潍坊市重点中学高三2月月考化学试卷 题型:实验题
(12分)鸡蛋壳中含有大量钙、少量镁和钾等元素。实验室可用图示流程测定鸡蛋壳中钙、镁元素含量。依据的反应可以表示为:Ca2++Y2-=CaY、Mg2++Y2-=MgY。回答下列问题。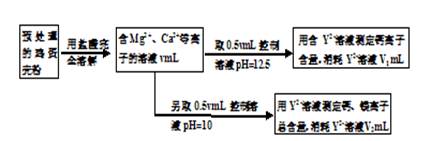
(1)测定Ca2+、Mg2+总含量时,控制溶液pH=10。若pH过大,测定结果将 (填“偏大”、“偏小”或“无影响”);
(2)测定Ca2+含量的关键是控制溶液的pH,使溶液中Mg2+形成沉淀,若要使溶液中c(Mg2+)不大于1.2×10-7mol/L,则溶液pH应不小于 (已知:Ksp[Mg(OH)2]=1.2×10-11,上述实验均在室温下进行)。
(3)如果鸡蛋壳粉质量为mg,溶液中Y2+浓度为c mol/L,则鸡蛋壳样品中镁元素质量分数是 。
(4)有同学提出可采用如下装置、通过测定鸡蛋壳与盐酸反应产生的二氧化碳的量就能测定鸡蛋壳中的钙的总含量。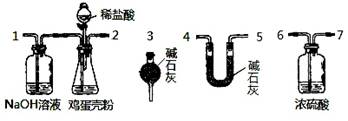
①采用该方法进行实验,各装置从左到右的连接顺序依次:
1—2—__ ________________(填各装置对应接口的数字序号)。
②若排除实验仪器和操作的影响因素,此实验方法测得的结果是否准确?
答:________(填“准确”、“不一定准确”或“无法判断”)。
原因是___________________ __
。
查看答案和解析>>
科目: 来源:2012届浙江省宁波四中高三第一学期期末考试化学试卷 题型:实验题
(11分)过氧化氢是重要的氧化剂和还原剂,常用于消毒、杀菌、漂白等。某化学兴趣小组同学围绕着过氧化氢开展了调查研究与实验。
Ⅰ.调查
(1)通过查阅资料,发现过氧化氢的沸点为152.1℃,而相对分子质量相同的硫化氢的沸点为-60.4℃,造成两者沸点差异大的主要原因是 ;
(2) 资料显示,过氧化氢制备目前最常用的是乙基蒽醌法,其主要过程可以用如图所示,写出此过程的总反应方程式是 。
Ⅱ.不稳定性实验研究
(3)为了探究温度、催化剂等外界条件对H2O2的分解速率的影响,某兴趣小组同学设计了如下三组实验,部分实验数据已经填在下面表中。
| 实验编号 | T/℃ | H2O2初始浓度/ mol·L-1 | FeCl3初始浓度/ mol·L-1 |
| Ⅰ | 20 | 1.0 | |
| Ⅱ | 50 | 1.0 | 0 |
| Ⅲ | 50 | | 0.1 |
| | 第一次 | 第二次 | 第三次 | 第四次 |
| 体积(mL) | 17.10 | 18.10 | 18.00 | 17.90 |
查看答案和解析>>
科目: 来源:2012届福建省龙岩一中高三第一学段模块考试化学试卷 题型:实验题
(8分)某学生用0.2000 mol/L KOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
| A.取20.00 mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞 |
| B.将已用蒸馏水洗净的碱式滴定管,再用标准溶液润洗碱式滴定管2~3次 |
| C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液 |
| D.取标准KOH溶液注入碱式滴定管至刻度0以上2~3厘米 |
查看答案和解析>>
科目: 来源:2012届江苏省重点中学高三下学期开学质量检测化学试卷 题型:实验题
(16分)某兴趣小组,对物质A的组成和性质,进行了如下系列研究:
实验1:对A的溶液进行了焰色反应;现象:火焰呈绿色。
实验2:从A的溶液中获取固体A。
实验3:加热干燥的固体A9.4g,出现大量的红棕色气体,经处理集得不溶于水的气体0.56L(标况下),且该气体能使带火星的木条复燃,残留黑色固体4.0g。
实验4:用酒精喷灯再对黑色固体加热,待固体完全 变红,又集得能使带火星的木条复燃的气体0.28L(标况下)。
变红,又集得能使带火星的木条复燃的气体0.28L(标况下)。
资料:①氧化亚铜属碱性氧化物,在酸性介质中能发生自身氧化还原反应;在空气中灼烧会转化为黑色固体,而在高温下较为稳定。
②酒精灯的火焰温度一般在400-500℃;酒精喷灯的火焰温度一般在1000℃左右;
根据题中信息,回答下列问题:
(1)实验1中进行焰色反应实验时,一次完整的操作次序为 (填序号,可重复);
a.灼烧 b.用盐酸清洗铂丝 c. 用铂丝蘸取待测液
(2)实验2中如何从溶液中获取固体A? ;
实验中所需主要的仪器有:铁架台(附铁圈)、 ;
(3)实验3中经处理集得不溶于水的气体0.56L,这里的“经处理”是将气体通过 ,然后用排水法收集气体。
(4)写出实验3中的分解反应式: ;
(5)写出实验4中的分解反应式: ;
(6)实验4中红色固体为纯净物,化学式可以通过计算来确定,也可以通过实验来进一步确定,请设计一个简单的实验确定方案,并写出所发生的反应式。 。
查看答案和解析>>
科目: 来源:2011-2012学年上海市松江二中高二上学期期末考试化学试卷 题型:实验题
(18分)工业生产的纯碱中常含有少量NaCl杂质。为测定某纯碱样品的纯度,化学课外活动小组设计了三种实验方案:
【方案一】取样品溶解后,加试剂使CO32-沉淀,测定沉淀的质量。
【方案二】用0.100 mol/L盐酸滴定。
【方案三】用稀酸将CO32-转化为CO2,测定CO2的质量。
解答1-4小题:
1.方案一的操作步骤有:①称量并溶解样品;②加入足量的BaCl2溶液;③过滤;④洗涤;⑤干燥;⑥称量并进行恒重操作。称量时所需定量实验仪器为____________________。判断是否达到恒重的标准是_____________________________________________________。
2.方案二的具体过程为: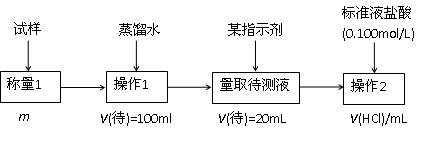
①操作1所需要的仪器有_____________________________________________。
②滴定时选择的指示剂为甲基橙。当溶液____________________________________时,说明达到了滴定终点。
③为减少偶然误差,通常的处理办法是_______________________________。
④滴定时若锥形瓶内有少量液体溅出,则测定结果_________。(选填“偏高”、“偏低”、“不影响”,下同),若盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗,测定结果_________。
3.方案三的实验装置如下图: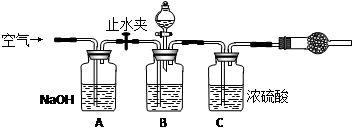
操作步骤有:①检查装置的气密性;②在干燥管内装满碱石灰,称量质量为W1 g;③称量W2 g样品装入广口瓶B中;④关闭止水夹;⑤缓慢加入稀H2SO4至不再产生气体为止;⑥ 打开止水夹;⑦缓缓鼓入空气数分钟,再称量干燥管,质量为W3 g。
该方案样品中纯碱的质量分数为__________________________(用代数式表示)。
上图中装置A的作用是_____________________。装置C的作用是_____________________。有同学认为空气中的水蒸气会进入干燥管导致测量结果_____________(填“偏大”、“偏小”或“无影响”)。改进措施可以是______________________________________________。
4.若用下图装置对样品进行分析,根据量瓶中收集到的液体的体积来计算样品中碳酸钠的含量。则下列装置中,最合理的是______。(选填序号)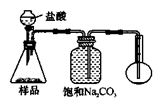
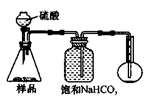
A B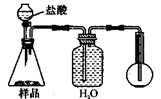
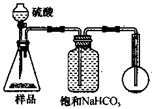
C D
查看答案和解析>>
科目: 来源:2012届山东省莱州一中高三第三次质量检测化学试卷 题型:实验题
(12分)已知某纯碱样品中含有 NaCl杂质,为测
NaCl杂质,为测 定样品中纯碱的质量分数,甲同学用下图装置及试剂进行实验(夹持仪器略)。填写下列空白处。
定样品中纯碱的质量分数,甲同学用下图装置及试剂进行实验(夹持仪器略)。填写下列空白处。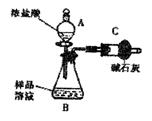
(1)仪器A、B的名称分别是 、 。
(2)甲同学按实验正常操作的主要步骤如下:
① ;
②将ag试样放入仪器B中,加适量蒸馏水溶解,得到样品溶液;
③称量盛有碱石灰的干燥管的质量为bg;
④从仪器A中滴入浓盐酸,直到不再产生气体时为止;
⑤再次称量盛有碱石灰的干燥管的质量为cg;
(3)甲同学根据以上实验求得的样品中Na2CO3的质量分数是 (用含a、b、c的式子表示)
(4)乙同学认为甲同学在实验装置设计和使用药品上都有缺陷,会导致测得的Na2CO3的质量分数偏高,而丙同学则认为甲同学的实验装置会使测得的结果偏低,丙同学认为结果偏低的原因可能是:
。
(5)若要解决乙、丙同学指出的甲同学实验中的问题,可对甲同学的实验装置和实验药品进行适当的改动,请按合理顺序选择仪器并完成下表:(用大写字母代表仪器,仪器 可重复使用,夹持仪器略)
可重复使用,夹持仪器略)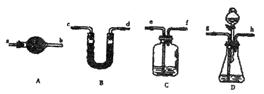
选用的 仪器 仪器 | | | | | |
| 添加的药品及必要的操作 | | | | | |
查看答案和解析>>
科目: 来源:2011-2012学年宁夏银川一中高二上学期期末考试化学试卷 题型:实验题
(5分)用实验确定HCOOH是弱电解质。两同学的方案是:
甲:①称取一定质量的HCOOH配制0.1 mol·L-1的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HCOOH是弱电解质。
乙:①用已知物质的量浓度的HCOOH溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;②分别取这两种溶液各10 mL,加水稀释为100 mL;③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HCOOH是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是 。
(2)甲方案中,说明HCOOH是弱电解质的理由是测得溶液的pH 1(选填>、<、=)。
乙方案中,说明HCOOH是弱电解质的现象是
a.装HCl溶液的试管中放出H2的速率快;
b.装HCOOH溶液的试管中放出H2的速率快;
c.两个试管中产生气体速率一样快:
(3)一定温度下有:a.盐酸;b.硫酸;c.醋酸三种酸。
①当其物质的量浓度相同时,c(H+)由大到小的顺序是___________________________。
②当c(H+)相同、体积相同时,同时加入镁,若产生相同体积的H2(相同状况),则开始时的反应速率____________________。(用a b c的大小关系表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com