
科目: 来源:2012-2013学年广东省龙川一中高二12月月考化学试卷(带解析) 题型:实验题
下图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出)。图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液。
(1)在上述装置中,实验需要加热的仪器为(填序号) 。
(2)为使A中乙醇平稳地汽化成乙醇蒸气,常用的方法是 。
(3)若E中的固体为纯净物,则E的化学式是 。
查看答案和解析>>
科目: 来源:2012-2013年广东省珠海市高一上学期期末质检化学试卷(B)(带解析) 题型:实验题
学生利用下图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3·6H2O 晶体。(图中夹持及尾气处理装置均已略去)
(1)回答下列问题:所用铁粉中若有杂质,欲除去不纯铁粉中混有的铝粉可以选用的试剂为 (填序号)。
| A.稀盐酸 | B.氢氧化钠溶液 | C.浓硫酸 | D.FeCl3溶液 |
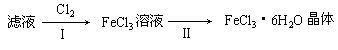
查看答案和解析>>
科目: 来源:2013届山东省淄博一中高三12月阶段性检测化学试卷(带解析) 题型:实验题
(共17分)硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下: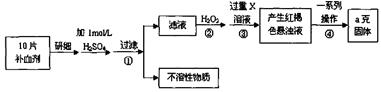
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是先滴加KSCN溶液,再滴加 ,该过程的现象为: 。
(2)步骤②加入过量H2O2的目的: 。
(3)步骤③中反应的离子方程式: 。
(4)步骤④中一系列处理的操作步骤:过滤、 、灼烧、 、称量。
(5)若实验无损耗,则每片补血剂含铁元素的质量 g。
(6)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5Fe2++MnO4—+8H+→5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻棒、烧杯、胶头滴管外,还需 。
②上述实验中的KMnO4溶液需要酸化,用于酸化的酸是 。
a.稀硝酸 b.稀硫酸 c.稀盐酸 d.浓硝酸
③滴定到终点时的现象描述为 ________________
查看答案和解析>>
科目: 来源:2013届山东省淄博一中高三12月阶段性检测化学试卷(带解析) 题型:实验题
(共14分)某中学化学实验小组为了证明和比较SO2和氯水的漂白性,设计了如下装置: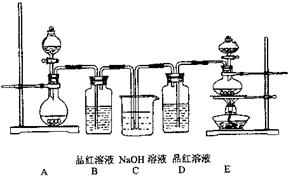
(1)实验室常用装置E制各Cl2,写出该反应的离子方程式__________________________指出该反应中浓盐酸所表现出的性质
(2)反应开始后,发现B、D两个容器中的品红溶液都褪色,停止通气后,给B、D两个容器加热,两个容器中的现象分别为:B D
(3)装置C的作用是
(4)该实验小组的甲、乙两位同学利用上述两发生装置按下图装置继续进行实验: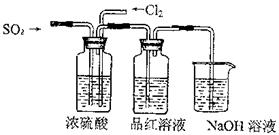
通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红溶液随时间的推移变得越来越浅。试根据该实验装置和两名同学的实验结果回答问题。
①试分析甲同学实验过程中,品红溶液不褪色的原因是: 。(用离子方程式进行说明)
②你认为乙同学是怎样做到让品红溶液变得越来越浅的?
查看答案和解析>>
科目: 来源:2013届北京市西城区高三上学期期末考试化学试卷(带解析) 题型:实验题
(8分)某小组取一定质量的FeSO4固体,利用下图装置进行实验。
| | 实验过程 | 实验现象 |
| ① | 通入一段时间N2,加热 | A中固体变为红棕色,B中有白色沉淀,D试管中有无色液体 |
| ② | 用带有火星的木条靠近装置D的导管口 | 木条复燃 |
| ③ | 充分反应,停止加热,冷却后,取A中固体,加盐酸 | 固体溶解,溶液呈黄色 |
| ④ | 将③所得溶液滴入D试管中 | 溶液变为浅绿色 |
查看答案和解析>>
科目: 来源:2013届山东省济宁市泗水一中高三上学期期末模拟化学试卷(带解析) 题型:实验题
(10分)已知用P2O5作催化剂,加热乙醇可制备乙烯,反应温度为80℃~210℃。某研究性小组设计了如下的装置制备并检验产生的乙烯气体(夹持和加热仪器略去)。

(1)仪器a的名称为_________________
(2)用化学反应方程式表示上述制备乙烯的原理______________________________。
(3)已知P2O5是一种酸性干燥剂,吸水放大量热,在实验过程中P2O5与乙醇能发生作用,因反应用量的不同,会生成不同的磷酸酯,它们均为易溶于水的物质,沸点较低。写出乙醇和磷酸反应生成磷酸二乙酯的化学方程式(磷酸用结构式表示为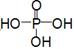 )__________________________________________________________。
)__________________________________________________________。
(4)某同学认为用上述装置验证产生了乙烯不够严密,理由是___________________。
(5)某同学查文献得知:40%的乙烯利(分子式为C2H6ClO3P)溶液和NaOH固体混和可快速产生水果催熟用的乙烯,请在上述虚线框内画出用乙烯利溶液和NaOH固体制取乙烯的装置简图(夹持仪器略)。
查看答案和解析>>
科目: 来源:2013届辽宁省丹东市宽甸二中高三上学期期末考试化学试卷(带解析) 题型:实验题
(12分)用含少量铁的氧化铜制取氯化铜晶体(CuCl2·xH2O)。有如下操作: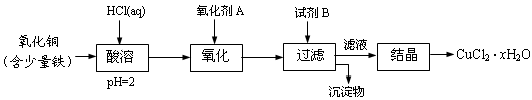
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,而此时Cu2+却几乎不水解。
(1)氧化剂A可选用_______(填编号,下同)
① Cl2 ② KMnO4 ③ HNO3 ④ H2O2
(2)要得到较纯的产品,试剂B可选用_______
① NaOH ② FeO ③ CuO ④Cu2(OH)2CO3
(3)试剂B的作用是______
① 提高溶液的pH ② 降低溶液的pH ③ 使Fe3+完全沉淀 ④ 使Cu2+完全沉淀
(4)从滤液经过结晶得到氯化铜晶体的方法是_________(按实验先后顺序选填编号)
① 过滤 ② 蒸发浓缩 ③ 蒸发至干 ④ 冷却
(5)为了测定制得的氯化铜晶体(CuCl2·xH2O)中x值,某兴趣小组设计了两种实验方案:
方案一:称取m g晶体灼烧至质量不再减轻为止,冷却、称量所得无水CuCl2的质量为n g。
方案二:称取m g晶体、加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止、冷却、称量所得固体的质量为n g。
试评价上述两种实验方案,其中正确的方案是______,据此计算得x = _________(用含m、n的代数式表示)。
查看答案和解析>>
科目: 来源:2013届河北省唐山一中高三第二次月考化学试卷(带解析) 题型:实验题
(14分)工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是 。
(2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,应选用 (选填序号)。
a.KSCN溶液和氯水 b.KSCN溶液和铁粉
c.浓氨水 d.酸性KMnO4溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应:
SO2+Br2+2H2O=2HBr+H2SO4,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中SO2的体积分数为 。
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和Q气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
(3)装置B中试剂的作用是 。
(4)认为气体Y中还含有Q的理由是 (用化学方程式表示)。
(5)为确认Q的存在,需在装置中添加M于 (选填序号)。
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有H2,预计实验现象应是 。
查看答案和解析>>
科目: 来源:2012-2013学年山东省鱼台一中高一上学期期末模拟化学试卷(带解析) 题型:实验题
(10分)氢化钙(CaH2,其中H元素的化合价为 –1价)固体是登山运动员常用的能源提供剂。氢化钙要密封保存,一旦接触到水就发生反应生成氢氧化钙和氢气。氢化钙通常用氢气与金属钙加热制取,下图是模拟制取装置。
(1)氢化钙与水反应的化学方程式为:__________________。
该反应中氧化产物与还原产物的物质的量之比为:__________________。
(2)利用图示实验装置进行实验,实验步骤如下:检查装置气密性后装入药品;打开分液漏斗活塞,_____________________(请按正确的顺序填入下列步骤的序号)。
①加热反应一段时间 ②收集气体并检验其纯度
③关闭分液漏斗活塞 ④停止加热,充分冷却
(3)装置B的作用是:_____________________________________;为了确认进入装置C的氢气已经干燥,应在B、C之间再接一装置,该装置中加入的试剂是:_____________。
查看答案和解析>>
科目: 来源:2012-2013学年云南省玉溪一中高一上学期期末考试化学试卷 题型:实验题
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验”。
请回答该实验中的问题。
(1)写出该反应的化学方程式 。
(2)实验前必须对整套装置进行的操作是 。
(3)圆底烧瓶中盛装的是水,该装置受热后的主要作用是 。
(4)干燥管中盛装的物质可以是 ,
作用是 。
(5)试管中收集到的气体是 ,如果要在A处玻璃管口处点燃该气体,则必须对该气体进行 ,这一操作的目的是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com