
科目: 来源:2012届河北省石家庄市高三上学期教学质量检测化学试卷 题型:实验题
(10分)某研究性学习小组为探究Cu(OH)2受热分解产物及产物性质,设计如下实验。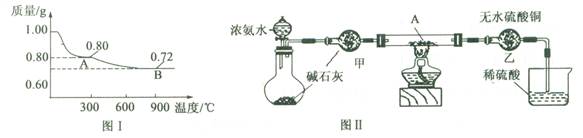
(1)取0.98 g Cu(OH)2固体加热,质量随温度变化的曲线如图1所示,产物A、B的化学式分别为 和 。
(2)取少量产物B加入足量的稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在,该反应的离子方程式为 。
(3)为证明产物A在加热时能与NH3反应,某同学设计了如图Ⅱ(夹持装置未画出)所示实验装置。
①简述检查该装置气密性的方法 。
②实验过程中观察到两个明显现象: i直玻璃管中固体由黑色变为红色;ii装置乙中固体由白色变为蓝色。能证明产物A与NH3发生了反应的判断依据的是 (填选项字母)。
a.只有i可以 b.只有ii可以 c.i或ii都可以
查看答案和解析>>
科目: 来源:2011-2012学年河北省正定中学高二上学期期末考试化学试卷 题型:实验题
(12分)工业上可用下列装置来测定黄铁矿中硫的质量分数(忽略SO2、H2SO3与氧气的反应)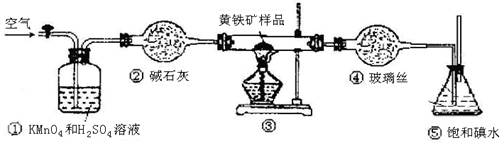
实验的正确操作步骤如下:
A.连接好装置,并检查装置的气密性
B.称取研细的黄铁矿样品
C.将2.0g样品小心地放入硬质玻璃管中
D.以1L/min的速率鼓入空气
E.将硬质玻璃管中的黄硫铁矿样品加热到800℃~850℃
F.用300mL的饱和碘水吸收SO2,发生的反应是:I2+SO2+2H2O=2HI+H2SO4
G.吸收液用CCl4萃取,分液
H.取20.00mL吸收液,用标准0.2000mol·L-1的NaOH溶液滴定。
试回答:
(1)已知:4FeS2 + 11 O2 = 2Fe2O3+ 8SO2 如12gFeS2完全燃烧放热85.3kJ,则FeS2燃烧热的热化学方程式是 。
(2)步骤G中所用主要仪器是 ,应取 (填“上”或“下” )层溶液进行后续实验。
(3)装置①的作用是 。
(4)步骤H中滴定时应选用 作指示剂
(5)假定黄硫铁矿中的硫在操作E中已全部转化为SO2,并且被饱和碘水完全吸收。滴定得到的数据如表所示:
| 滴定次数 | 待测液体的体积/mL | 标准碱溶液的体积/mL | |
| 滴定前 | 滴定后 | ||
| 第一次 | 20.00mL | 0.00 | 20.58 |
| 第二次 | 20.00mL | 0.22 | 20.20 |
| 第三次 | 20.00mL | 0.36 | 20.38 |
查看答案和解析>>
科目: 来源:2012届安徽省淮北市高三第一次模拟考试化学试卷 题型:实验题
(10分)某研究性学习小组研究HNO3的氧化性,设计了如下实验:在盛有新配制FeS04溶液的试管中滴入2滴KSCN溶液,观察现象,然后再滴人几滴浓HN 03,溶液的颜色变红,但是将红色溶液放置一会儿则发现溶液由红色突然变为蓝色,并产生红棕色气体。这一奇特现象激起了同学的好奇心与求知欲望,对此现象设计了探究性实验。
(1)实验室粗略配制一定质量分数的硫酸亚铁溶液的方法是:将一定质量的绿矾(FeS04·7H2 0)置于烧杯中,__________________________。
(2)提出假设:
甲同学认为是FeS04与HN03作用
乙同学认为是KSCN与HNO3作用
(3)根据乙同学的观点,设计了如下实验方案进行验证:向浓HN03中逐滴加入KSCN溶液,实验开始时无明显现象,一段时间后溶液慢慢变红色至深红色,突然剧烈反应产生大量气泡,放出红棕色气体。继续滴入KSCN,溶液变为浅蓝色,最后变成无色。将产生的气体通人过量的Ba(OH)2溶液,产生浑浊,并剩余一种气体(该气体是空气中的主要成分之一);向反应后的溶液中加入BaC12溶液产生白色沉淀。
写出向浓HNO3中滴入KSCN溶液反应的离子方程式:__________________
丙同学认为还应设计K2S04溶液与浓硝酸作用的实验,他的理由是__________________
(4)延伸探究:丁同学认为SCN-的性质还应进一步探究,查资料发现:(SCN)2是一种“拟卤素”,与C12、Br2有相似的性质。他据此设计了以下方案:向Fe(SCN)3中分别滴加过量的氯水、溴水,溶液的红色均变为黄色。请写出Fe(SCN)3与氯气反应的离子方程式: 。
(5)通过本次探究,可以得出以下结论:
a、用SCN -间接检验Fe2+时加入氧化剂应注意 (填“少量”、“过量”);
b、与SCN-反应使溶液变红的不一定是Fe3+
查看答案和解析>>
科目: 来源:2011-2012学年江苏省南通市小海中学高一上学期期末考试化学试卷 题型:实验题
某教师在课堂上用下图所示的装置来验证浓硫酸与铜是否发生反应,并探讨反应所产生气体的性质。请回答下列问题: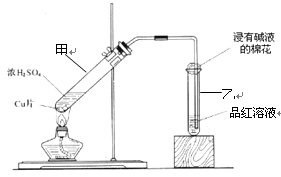
①通过试管乙中发生的 现象说明了铜和浓硫酸发生了化学反应,并且该现象还能说明产生的气体具有 性。
②写出试管甲中所发生反应的化学方程式 。
③该反应体现了浓硫酸的 性和 性。
查看答案和解析>>
科目: 来源:2011-2012学年广东省中山市高一上学期期末统一考试化学试卷 题型:实验题
(9分)某小组同学为探究铜跟浓硫酸的反应情况,并收集一瓶反应产生的气体,设计了如右图所示装置。实验中他们取6.4g铜片与12mL 18mol/L浓硫酸放在圆底烧瓶中加热,直到反应完毕仍发现烧瓶中有铜剩余。
(1)为防止空气污染,请补画右图虚框中的实验装置,并注明所需要的试剂名称。
(2)写出铜跟浓硫酸反应的化学方程式:
。
(3)该小组认为铜片未完全溶解,则瓶中可能还有一定量的硫酸剩余,其原因是:
。
(4)为证明反应结束后的烧瓶中确有余酸,可选用下列药品中的 (填写字母序号):
| A.铁粉 | B.BaCl2溶液 | C.银粉 | D.Na2CO3溶液 |
查看答案和解析>>
科目: 来源:2011-2012学年福建省三明市普通高中高一上学期联合命题考试化学试卷 题型:实验题
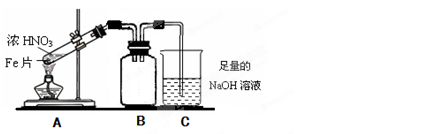
(16分)Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质。请你参与研究并回答下列问题:
(1)甲同学完成了Fe、Cu分别与S、Cl2反应的实验,下列物质中不可能为甲同学实验得到的生成物是
| A.FeCl3 | B.FeCl2 | C.CuCl2 | D.FeS |
查看答案和解析>>
科目: 来源:2011-2012学年云南省昆明一中高二上学期期末考试化学试卷 题型:实验题
(12分)某化学课外活动小组研究乙醇氧化的实验并验证其产物,设计了甲、乙两套装置(图中的夹持仪器均未画出,“△”表示酒精灯热源),每套装置又可划分为①、②、③三部分。仪器中盛放的试剂为:a—无水乙醇(沸点:78℃);b—铜丝;c—无水硫酸铜;d—新制氢氧化铜悬浊液。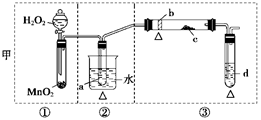

(1)简述两套方案各自的优点:
甲:__________________________________________________________________,
乙:___________________________________________________________________。
(2)集中两套方案的优点,组成一套比较合理完善的实验装置,可按气流由左至右的顺序表示为_________________________________________________________(例如甲①,乙②)。
(3)若要保证此实验有较高的效率,还需补充的仪器有________,理由_______________。
(4)实验中能验证乙醇氧化产物的实验现象是________________________________。
(5)装置中,若撤去第①部分,其它操作不变,则无水硫酸铜无明显变化,其余现象与(4)相同,推断燃烧管中主要反应的化学方程式:__________________________________。
查看答案和解析>>
科目: 来源:2012届山东省枣庄市高三上学期期末测试化学试卷 题型:实验题
(16分)现有以下实验装置供实验时挑选使用。
(1)利用Cu和浓硝酸反应制备NO2,用过氧化氢溶液和MnO2制取O2,根据反应原理应选用___________装置(填序号,从A、B、C中选取)。
(2)某同学设计下列四种制备NH3的方法,不合理的是_________(填序号)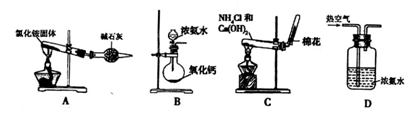
(3)欲用石灰石和浓盐酸反应制取纯净干燥的CO2气体,将你所选的仪器按气体由左向右方向连接,连接顺序为______________→G→___________________。
用饱和碳酸氢钠溶液除去挥发出的HCl优于用水除HCl的原因是_____________________
____________________________________________________。
(4)某小组为了探究Ag与浓硝酸反应过程中可能产生NO,设计了一连接顺序为D→H→I→K的实验装置。
①检验这一装置气密性的方法是________________________________________________
__________________________________________________________________________,
②反应开始前通入N2的目的是______________________________________________,
③反应结束,若H瓶中溶液体积为100mL,从中取出25.00mL溶液以酚酞作指示剂,用0.1000mol·L—1NaOH溶液进行滴定,两次滴定用去NaOH溶液的体积分别为16.98mL和17.0.2mL,则该瓶中硝酸的物质的量浓度为_________________。
若实验测得NO的体积为95.2mL(已折算成标准状况),请你通过数据说明Ag与浓硝酸反应过程中是否有NO产生____________________________________________________
___________________________________________________________________________。
查看答案和解析>>
科目: 来源:2011-2012学年福建省师大附中高一上学期期末考试化学试卷 题型:实验题
(18分)科学探究结果的准确性来自于探究活动中研究方法的科学性,研究过程的计划性、研究目的明确性。
(一)学生(甲)应用下图装置(A)所示意的方法研究氯气的性质,其中气体的主要成分是氯气(含有空气和水蒸气)。请回答下列问题:
(1)该项研究(实验)的主要目的是
(2)浓硫酸的作用是 。与研究目的直接相关的实验现象是 ________________ _ 。
(3)虚框中的装置应选择 (填“B”或“C”),其盛放的试剂
为 (填试剂名称);使用该装置的目的是 ;该装置内发生反应的化学方程式为 。
(二)学生(乙)设计实验探究金属铝表面氧化膜的性质:将铝片(含氧化膜)投入浓氯化铜溶液中,铝表面很快出现一层海绵状暗红色物质。若用同样的铝片投入同浓度的硫酸铜溶液中,在短时间内铝片无明显变化。回答下列问题:
(1)铝片表面出现的暗红色物质的过程中发生的离子反应方程式是 。
(2)同学(乙)认为:铝与氯化铜溶液能迅速反应,而与同浓度的硫酸铜溶液在短时间内不反应的原因是“氯离子能破坏氧化铝表面薄膜,而硫酸根离子不能”。并设计如下实验方案进行验证,请你根据其思路完成下列空格:
[实验方案] 在硫酸铜溶液中加入铝片,无明显现象,再加入 (填试剂名称),若反应明显加快了,说明上述推断正确。
查看答案和解析>>
科目: 来源:2011-2012学年福建省师大附中高一上学期期末考试化学试卷 题型:实验题
(9分)有一已磨成粉末的混合物试样,是由下列六种物质中的若干种等量组成:
NaCl 、 KCl 、 CaCl2、CuSO4( 无水)、 Na2SO4、Na2CO3
为了要确定该粉末试样的成分,某研究性学习小组先查了资料后,研拟了一个检验粉末试样的流程图,并在老师的指导下在化学实验室中进行实验。以下是该小组实验报告的一部分﹕
实验一:用烧杯取粉末试样约2克,加蒸馏水约100毫升,搅拌后形成无色的透明溶液X。
实验二:在溶液X中加了盐酸,观察到在溶液中陆续产生气泡,至溶液不再冒气泡,溶液仍为无色透明(贴上卷标Y)。
实验三:在无色透明的溶液Y中,滴加BaCl2溶液,即见白色沉淀。
实验四:继续滴加BaCl2溶液,至白色沉淀不再产生后,过滤分离出白色沉淀,得到透明的无色滤液Z。
实验五:在滤液Z中,滴入AgNO3溶液,则见白色沉淀,加入稀硝酸,沉淀不溶解。
(1)根据上述实验报告,原粉末中一定没有哪两种物质﹖ (填化学式)
(2)原粉末中,一定含有哪两种物质 ﹖ ( 填化学式)
(3)若只需回答上述(1)(2)的问题,你认为该小组同学不需要做哪两个实验 (填标号)
a、实验一 b、实验二 c、实验三 d、实验四 e、实验五
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com