
科目: 来源:2011-2012学年浙江东阳中学、兰溪一中高二下学期期中考试化学卷(带解析) 题型:实验题
(8分)维生素C是一种水溶性维生素(其水溶液呈酸性),它的分子式是C6H8O6。维生素C易被空气中的氧气氧化。在新鲜的水果,蔬菜,乳制品中都富含有维生素C,如新鲜橙汁中维生素C的含量为500mg·L-1左右。某校课外活动小组测定了某品牌的软包装橙汁中维生素C的含量,下面是测定分析的实验报告:
(1)测定目的:测定XX牌软包装橙汁中维生素C的含量。
(2)测定原理:C6H8O6 + I2 → C6H6O6 + 2H+ + 2I- 。
(3)实验用品:
①实验仪器:酸式滴定管,铁架台,锥形瓶,滴管等。
②试剂:指示剂 (填名称),7.5×10-3mol·L-1标准碘液,蒸馏水。
(4)实验步骤:
①洗涤仪器:检查滴定管是否漏水,润洗好后装好标准碘液。
②打开软包装橙汁,目测颜色(橙黄色,澄清度好),用酸式滴定管向锥形瓶中移入20.00ml待测橙汁,滴入2滴指示剂。
①用左手控制滴定管的 (填部位),右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化直到滴定终点,判断滴定终点的现象是 。
记下读数,再重复操作两次。
(5)数据记录处理,若经数据处理,滴定中消耗标准碘溶液的体积是15.00ml,则此橙汁中维生素C的含量为 mg·L-1。
(6)误差分析:若在实验中存在下列操作,其中会使维生素C的含量偏低的是
| A.量取待测橙汁的仪器水洗后未润洗 |
| B.锥形瓶水洗后未用待测液润洗 |
| C.滴定前尖嘴部分有一气泡,滴定终点时消失 |
| D.滴定前仰视读数,滴定后俯视读数 |
查看答案和解析>>
科目: 来源:2011-2012学年浙江省东阳中学高二下学期第一次阶段性测试化学试卷(带解析) 题型:实验题
为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
丙
(1)定性分析:如图甲可通过观察 ,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是 。
(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。图中仪器A的名称为 ,检查该装置气密性的方法是
,实验中需要测量的数据是 。
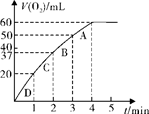
(3)加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图丙所示
① 写出H2O2在MnO2作用下发生反应的化学方程式 。
②计算H2O2的初始物质的量浓度_____________。(请保留两位有效数字)
查看答案和解析>>
科目: 来源:2011-2012学年安徽省蚌埠二中高一下学期期中考试化学试卷(带解析) 题型:实验题
一般的易拉罐主要为铝合金,其中以铝铁合金和铝镁合金最为常见。本次实验选取可口可乐公司生产的雪碧汽水易拉罐作为探究的对象。
提出假设:易拉罐的主要成分是铝和铁。
探究过程及现象:
1.配制6 mol/L氢氧化钠溶液和6 mol/L的盐酸。
2.将易拉罐剪开,用砂纸打磨使表面油漆和氧化膜去掉,再剪取一小块进行实验。
实验一:用胶头滴管向装有铝合金的大试管中加入足量的氢氧化钠溶液,可以看到有气泡生成,反应一段时间后,溶液中还有不溶物。
实验二:用滴管继续向实验一的试管中逐滴加入6 mol/L的盐酸至足量,静置24小时。
按实验顺序,该同学记录的现象如下:①开始没有明显现象;②有白色絮状沉淀生成;③白色沉淀消失;④原溶液中不溶物完全溶解,此时溶液呈浅绿色;⑤静置24小时后,溶液呈棕黄色。
实验三:再向该试管中加入一定量的氢氧化钠溶液,最终只得到红棕色沉淀。
请回答下列问题:
(1)实验一反应的化学方程式__________________________________________。
(2)实验二所得溶液为什么静置24小时后由浅绿色变为棕黄色
_______________________________________________________________________。
(3)写出实验二中产生①、②现象的反应离子方程式:__________________________,
____________________________________。
(4)由此可知该假设_____________(填“成立”,“不成立”或“无法确定”)。
查看答案和解析>>
科目: 来源:2012届宁夏贺兰一中高三下学期第三次月考化学试卷(带解析) 题型:实验题
(14分)某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验。
[实验1]铜与浓硫酸反应,实验装置如图所示。
实验步骤:
①先连接好装置,检验气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面。
(1)装置A中发生反应的化学方程式为 。
(2)熄灭酒精灯后,因为有导管D的存在,B中的液体不会倒吸,其原因是 。
(3)拆除装置前,不需打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是 。
[实验2]实验中发现试管内除了产生白色固体外,在铜丝表面还产生黑色固体甲,其中可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧化亚铜。
查阅资料:
①氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,在氧气流中煅烧,可以转化为氧化铜。
②硫化铜和硫化亚铜常温下都不溶于稀盐酸,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫。
为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图的实验: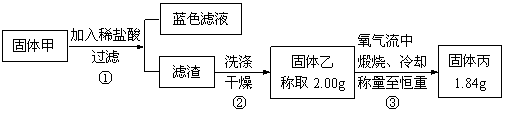
(4)②中检验滤渣是否洗涤干净的实验方法是
(5)③中在煅烧过程中一定发生的反应的化学方程式为 。
(6)下列对于固体甲的成分的判断中,正确的是(填字母选项) 。
| A.固体甲中,CuS和Cu2S不能同时存在 |
| B.固体甲中,CuO和Cu2O至少有一种 |
| C.固体甲中若没有Cu2O,则一定有Cu2S |
| D.固体甲中若存在Cu2O,也可能有Cu2S |
查看答案和解析>>
科目: 来源:2011-2012学年河北省衡水中学高二下学期调考试化学试卷(带解析) 题型:实验题
(14分) 已知烃B分子内C、H原子个数比为1︰2,相对分子质量为28,核磁共振氢谱显示分子中只有一种化学环境的氢原子,且有如下的转化关系:
(1)B的结构简式是
(2)A可能属于下列哪类物质___________
a.醇 b.卤代烃 c.酚 d.羧酸
(3)反应①是D与HCl按物质的量之比1︰1的加成反应,则D的分子式是___________。
反应②可表示为:G + NH3 → F + HCl (未配平),该反应配平后的化学方程式是(有机化合物均用结构简式表示):
化合物E(HOCH2CH2Cl)和 F [ HN(CH2CH3)2 ]是药品普鲁卡因合成的重要中间体,普鲁卡因的合成路线如下:(已知:  )
)
(4)甲的结构简式是 _________________。
由甲苯生成甲的反应类型是_________________。
(5)乙中有两种含氧官能团,反应③的化学方程式是
(6)丙中官能团的名称是 。
(7)普鲁卡因有两种水解产物丁和戊。
① 戊与甲互为同分异构体,戊的结构简式是_____________________。
② 戊经聚合反应制成的高分子纤维广泛用于通讯、宇航等领域。该聚合反应的化学方程式是 。
③ D的红外光谱表明分子内除C—H键、C—C键外还含有两个C—O单键。则D与F在一定条件下反应生成丁的化学方程式是________________________________。
查看答案和解析>>
科目: 来源:2012届黔东南州高三第一次模拟考试理综化学试卷(带解析) 题型:实验题
(17分)铁不能与冷水反应,但能与水蒸气反应,某化学兴趣小组为探究铁与水蒸气反应,请你为他们完成实验报告。
实验目的:探究铁与水蒸气的反应
反应原理: (用化学反应方程式表示)
实验装置:回答以下问题(加热装置略去)
| 装置编号 | A | B | C | D | |
| 装置 |  |  |  |  | |
| 装置所起作用 | | | | | |
| 按加热先后从左至右,实验装置连接顺序和导管连接方法 | 装置连接顺序: (填装置编号) | ||||
| 需要加热的装置 | (填装置编号) | ||||
查看答案和解析>>
科目: 来源:2012届陕西省交大附中高三第四次诊断化学试卷(带解析) 题型:实验题
(8分)某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究。⑴提出假设 ①该反应的气体产物是CO2。②该反应的气体产物是CO。③该反应的气体产物是 。
⑵设计方案 如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。
⑶查阅资料
氮气不与碳、氧化铁
发生反应。实验室可
以用氯化铵饱和溶液和
亚硝酸钠(NaNO2)饱
和溶液混合加热反应制
得氮气。请写出该反应的离子方程式: 。
⑷实验步骤
①按上图连接装置,并检查装置的气密性,称取3.20g氧化铁、0.48g碳粉混均匀,放入50.00g的硬质玻璃管中;
②加热前,先通一段时间纯净干燥的氮气;
③停止通入N2后,夹紧弹簧夹,加热一段时间,澄清石灰水(足量)变浑浊;
④待反应结束,再缓缓通入一段时间的氮气。冷却至室温,称得硬质玻璃管和固体总质量为52.24g;
⑤过滤出石灰水中的沉淀,洗涤、烘干后称得质量为2.00g。
步骤②、④中都分别通入N2,其作用分别为
。
⑸数据处理试根据实验数据分析,写出该实验中氧化铁与碳发生反应的化学方程式: 。zx
查看答案和解析>>
科目: 来源:2011-2012学年浙江杭州萧山九中高二下学期第一次质量检测化学试卷(解析版) 题型:实验题
某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol· L-1盐酸、0.55mol· L-1NaOH溶液,尚缺少的实验玻璃用品是 、 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否”),其原因是 。
(3)他们记录的实验数据如下:
| 实验用品 | 溶液温度 | 中和热 △H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | |
查看答案和解析>>
科目: 来源:2012届河南省郑州市高三第一次质量预测化学试卷(解析版) 题型:实验题
(12分〉某研究性学习小组欲探究SO2能否与BaCl2溶液反应生成BaSO3沉淀。查阅资料得知常温下BaSO3的KSP为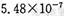 ,饱和亚硫酸中
,饱和亚硫酸中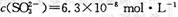 。
。
(1) 将0.1 mol ? L—1的BaCl2溶液滴入饱和亚硫酸中,_______ (填“能”或“不能”)生成BaSO3沉淀,原因是______________ (请写出必要的推断过程)。
(2) 浓硫酸的沸点为338°C,酒精灯火焰的温度为400?5000C,甲同学用装置I进行实验,发现BaCl2溶液中出现白色沉淀,且白色沉淀不溶于盐酸。
①写出加热试管中发生反应的化学方程式:_____________________
②白色沉淀的化学式是_______,请用离子方程式表示生成该白色沉淀的可能原因___________________________________
(3) 乙同学认为甲同学的装置不完善,设计了改进装置II进行实验(夹持装置和A中加热装置已略,气密性已检验)。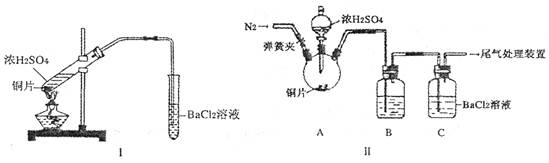
①打开弹簧夹,通入N2—段时间后关闭弹簧夹
②滴加一定量浓硫酸,加热A,一段时间后C中未见沉淀生成。
操作①的目的是_______,洗气瓶B中的试剂是______________。
(4) 丙同学取乙实验后的C中溶液少许,滴加一种无色溶液,也产生不溶于盐酸的白色沉淀,丙滴加的试剂可能是______________。
| A.NaOH溶液 | B.Na[Al(OH)4]溶液 | C.H2O2溶液 | D.酸性 KMnO4溶液 |
查看答案和解析>>
科目: 来源:2011-2012学年广东省梅州市曾宪梓中学高一下学期3月月考化学试卷 题型:实验题
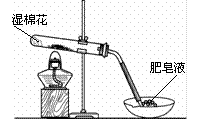
(13分)制取氨气并完成喷泉实验(图中夹持装置均已略去)。
(1)写出实验室制取氨气的化学方程式: 。
(2)收集氨气应使用 法,要得到干燥的氨气可选用 做干燥剂。
(3)用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是 。该实验利用了氨气的 性质。
(4)如果只提供如图2的装置,请说明引发喷泉的方法 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com