
科目: 来源:2010—2011学年黑龙江省大庆实验中学高一下学期开学测试化学试卷 题型:填空题
(4分)氯碱工业是以电解食盐水为基础的基本化学工业,电解食盐水同时得到两种气体(气体A是所有气体中密度最小的气体,气体B是制取漂白粉的原料)和一种易溶、易电离的碱。
(1)试写出电解食盐水的化学方程式 (注明反应条件)。
(2)试写出气体B与澄清石灰水反应的离子方程式 。
查看答案和解析>>
科目: 来源:2011届吉林省长春市高三第二次模拟考试(理综)化学部分 题型:填空题
(15分)
我国有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如下图所示(图中某
些转化步骤及生成物未列出):
请填写下列空白:
(1)已知0.5 mol甲烷和0.5 mol水蒸气在t ℃,p k Pa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量。该反应的热化学方程式是: ______。
(2)上述流程中,工业上分离H2、CO2合理的方法是___________。
| A.混合气先通入氢氧化钠溶液,再在溶液中加盐酸 |
| B.混合气加压冷却,使CO2液化 |
| C.混合气用氨水洗涤 |
| D.混合气先通入到石灰浆,然后高温煅烧固体, |
查看答案和解析>>
科目: 来源:2011届山东省日照市高三第一次模拟考试(理综)化学部分 题型:填空题
(12分)美日科学家因研发“有机合成中的钯催化的交叉偶联”而获得2010年度诺贝尔化学奖。有机合成常用的钯/活性炭催化剂长期使用,催化剂会被杂质(如:铁、有机物等)污染而失去活性,成为废催化剂,故需对其回收再利用。一种由废催化剂制取氯化钯(PdCl2)的工艺流程如下: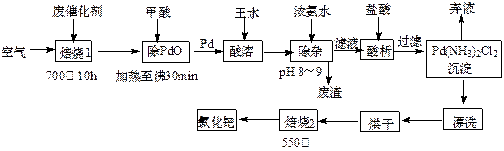
(1)甲酸在反应中的作用是 (选填:“氧化剂”或“还原剂”);
(2)加浓氨水时,钯元素转变为可溶性[Pd(NH3)4]2+,此时铁元素的存在形式是 (写化学式);
(3)王水是浓硝酸与浓盐酸按体积比1∶3混合而成的,钯在王水中溶解的过程中有化合物A和一种无色、有毒气体B生成。
①气体B的化学式为 ,
②经测定,化合物A由3种元素组成,有关元素的质量分数为Pd:42.4%,H:0.8%。则A的化学式为 ;
(4)700℃“焙烧1”的目的是 ,550℃“焙烧2”的目的是 。
查看答案和解析>>
科目: 来源:2011届湖北省黄石二中高三二月份调研考试(理综)化学部分 题型:填空题
利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制硝酸,在工业上一般可进行连续生产。请回答下列问题:
(1)已知:N2(g)+O2(g)=2NO(g);△H= +180.5kJ/mol N2(g)+3H2(g)
N2(g)+3H2(g)  2NH3(g);△H= -92.4kJ/mol
2NH3(g);△H= -92.4kJ/mol
2H2(g)+O2(g)=2H2O(g) ;△H= -483.6kJ/mol
氨气经催化氧化生成一氧化氮气体和水蒸气反应的热化学方程式为 。
(2)在容积固定的密闭容器中发生上述氨气的催化氧化反应,容器内部分物质的物质的量浓度如下表:
| 时间/浓度 | c(NH3)(mol/L) | C(O2)(mol/L) | C(NO)(mol/L) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.54 | 0.9 | 0.56 |
查看答案和解析>>
科目: 来源:2011届江苏省苏锡常镇四市高三调研测试(一)化学试卷 题型:填空题
(12分)磷肥生产过程中得到的副产物石膏(CaSO4·2H2O)可转化为硫酸钾肥料和氯化钙水合物储热材料,其工艺流程示意图如下:
(1)本工艺中需用CaCO3作原料,它可制备上述流程用的_________、_________ 原料,除CaCO3、CaSO4·2H2O、NH3、H2O外,还需要_________等原料。
(2)吸收流程中通入CO2和NH3量的关系分别为_________(选填序号)
A.足量的CO2,适量的NH3 B.足量的NH3,少量的CO2
C.适量的CO2,足量的NH3 D.少量的NH3,足量的CO2
(3)在实验室进行过滤操作,所需的玻璃仪器为_________(从A~H中选择)。
A.试管 B.烧瓶 C.烧杯 D.分液漏斗
E.普通漏斗 F.蒸馏烧瓶 G.玻璃棒 H.酒精灯
(4)过滤I所得滤 液是(NH4)2SO4溶液,检验滤液中是否含有CO32―的方法是_________ 。
液是(NH4)2SO4溶液,检验滤液中是否含有CO32―的方法是_________ 。
(5)转化I过程中加入适量十二烷基苯磺酸钠,其作用可能是__________________。
查看答案和解析>>
科目: 来源:2011届江苏省苏锡常镇四市高三调研测试(一)化学试卷 题型:填空题
(12分)高铁酸钾是一种高效的多功能的水处理剂。工业上常采用NaClO氧化法生产,原理为:
3NaClO + 2Fe(NO3)3 + 10NaOH=2Na2FeO4↓+ 3NaCl + 6NaNO3 + 5H2O
Na2FeO4+2KOH=K2FeO4+2NaOH
主要的生产流程如下: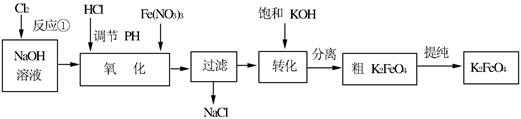
(1)写出反应①的离子方程式_____________________________。
(2)流程图中“转化”是在某低温下进行的,说明此温度下Ksp(K2FeO4) _________ Ksp(Na2FeO4)(填“>”或“<”或“=”)。
(3)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。
图1为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;
图2为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4生成率的影响。
①工业生产中最佳温度为_______℃,此时Fe(NO3)3与NaClO两种溶液最佳质量浓度之比为_______。
②若NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:
____________________________________________________。
若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式:____________________________________。
(4)K2FeO4 在水溶液中易水解:4FeO42—+10H2O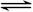 4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用_______溶液(填序号)。
4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用_______溶液(填序号)。
| A.H2O | B.CH3COONa、异丙醇 | C.NH4Cl、异丙醇 | D.Fe(NO3)3、异丙醇 |
查看答案和解析>>
科目: 来源:2011届江苏省苏锡常镇四市高三调研测试(一)化学试卷 题型:填空题
(8分)化合物G是冶炼某常见金属的原料,工业上提取G的流程如下图所示(已知晶体E的焰色反应呈黄色):
(1)溶液A为_____________溶液(用化学式表示,下同),赤泥浆C的主要成分有_____________ ,
(2)操作Ⅰ为_____________;操作Ⅱ为_____________ ,
(3)写出由B生产F的离子方程式为_________________________________
(4)苛化试剂与E溶液反应生成溶液A,则苛化试剂是_____________ ,该工艺的优点是_____________(答一条,合理即可)。
查看答案和解析>>
科目: 来源:2011届四川省南充高中高三第七次月考化学卷 题型:填空题
(14分)近年来,随着我国经济的快速发展,对电力的需求越来越高,这也促进了我国电力工业高速发展,但我国电力结构中,火电比重非常大,占发电装机总容量的75%以上,且火电比重还在逐年上升。火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g);ΔH1=-574kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g);ΔH2=-1160kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为: 。
(2)脱碳。将CO2转化为甲醇的热化学方程式为: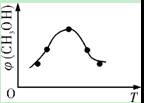
CO2(g)+3H2(g) CH3OH(g)+H2O(g);ΔH3
CH3OH(g)+H2O(g);ΔH3
①取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如右图所示,则上述CO2转化为甲醇的反应的ΔH3 0(填“>”、“<”或“=”)。
②在一恒温恒容密闭容器中充入1mol CO2和3mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如下图所示。下列说法正确的是 (填字母代号)。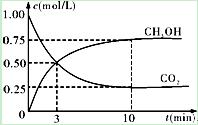
| A.第10min后,向该容器中再充入1mol CO2和3mol H2,则再次达到平衡时c(CH3OH)=1.5mol·L-1 |
| B.0~10min内,氢气的平均反应速率为0.075mol/(L·min) |
| C.达到平衡时,氢气的转化率为0.75 |
| D.升高温度将使n(CH3OH)/n(CO2)减小 |
查看答案和解析>>
科目: 来源:2011届江苏省扬州中学高三下学期开学练习化学试卷 题型:填空题
右图为工业制备硝酸的设备示意图,其生产过程中发生的反应主要有: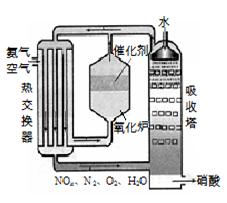
①4NH3(g)+5O2(g) 4NO(g) +6H2O(l) △H<0
4NO(g) +6H2O(l) △H<0
②2NO(g)+O2 (g) 2NO2(g) △H<0
2NO2(g) △H<0
③3NO2(g)+H2O(l) 2HNO3(l) +NO(g) △H<0
2HNO3(l) +NO(g) △H<0
⑴能使吸收塔内反应速率增大,且能提高HNO3产率的措施是 ▲ 。
| A.适当升高温度 |
| B.适当增大吸收塔内的压强 |
| C.增大空气中O2的浓度 |
| D.吸收塔内填充瓷环,增大气液接触面 |
 m3)。假设工业生产硝酸过程中,通过循环操作可以使NH3、O2得以完全利用。
m3)。假设工业生产硝酸过程中,通过循环操作可以使NH3、O2得以完全利用。查看答案和解析>>
科目: 来源:2011届黑龙江省哈三中等四校高三第一次高考模拟联考(理综)化学部分 题型:填空题
(15分)
纯碱一直以来都是工业生产的重要原料,很长一段时间来纯碱的制法都被欧美国家所垄断。上个世纪初我国著名的工业化学家侯德榜先生,经过数年的反复研究终于发明了优于欧美制碱技术的联合制碱法(又称侯氏制碱法)。并在天津建造了我国独立研发的第一家制碱厂。其制碱原理的流程如下: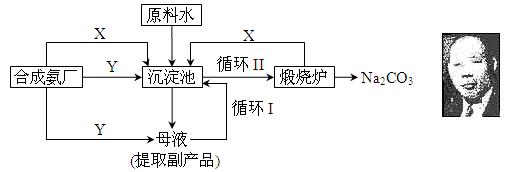
⑴侯德榜选择天津作为制碱厂的厂址有何便利条件(举二例说明) 、 。
⑵合成氨工厂需要向制碱厂提供两种原料气体,它们分别是: 、 。(填化学式)这两种气体在使用过程中是否需要考虑添加的顺序: (填“是”或“否”),原因是: 。
⑶在沉淀池中发生的反应的化学方程式是: 。
⑷使原料水中溶质的利用率从70%提高到90%以上,主要是设计了 (填上述流程中的编号)的循环。从母液中可以提取的副产品的应用是 (举一例)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com