
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
 发酵粉是一种化学膨松剂,可由小苏打、臭粉(碳酸氢铵)、明矾中的两种物质组成.某小组为探究不同品牌的发酵粉的化学成分,进行如下实验.
发酵粉是一种化学膨松剂,可由小苏打、臭粉(碳酸氢铵)、明矾中的两种物质组成.某小组为探究不同品牌的发酵粉的化学成分,进行如下实验.| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量样品溶于足量的盐酸后,将溶 液分成两份,分别装入A、B试管中. | |
| 步骤2:______ | ______,证明有Na+,发酵粉中有NaHCO3. |
| 步骤3:______ | ______,结合步骤2中的结论,假设2成立. |
查看答案和解析>>
科目: 来源: 题型:解答题
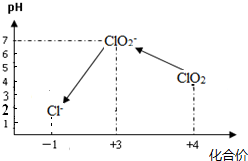
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:单选题
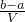 mol?L-1
mol?L-1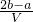 mol?L-1
mol?L-1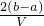 mol?L-1
mol?L-1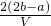 mol?L-1
mol?L-1查看答案和解析>>
科目: 来源: 题型:解答题
 MnCl2+Cl2↑+2H2O,一定质量的二氧化锰固体溶解在100mL 过量的浓盐酸中,当反应生成 4.48L 氯气(标况下)时,请计算:被氧化HCl的物质的量.(要求写出计算过程)
MnCl2+Cl2↑+2H2O,一定质量的二氧化锰固体溶解在100mL 过量的浓盐酸中,当反应生成 4.48L 氯气(标况下)时,请计算:被氧化HCl的物质的量.(要求写出计算过程)查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com