
科目: 来源: 题型:
| A、1molAl和足量的NaOH溶液反应,失去的电子数为3NA(NA表示阿伏加德罗常数) | B、原电池的负极发生氧化反应,电解池的阳极发生还原反应 | C、Cu能被FeCl3溶液腐蚀,其离子方程式为:Cu+Fe3+=Cu2++Fe2+ | D、Na+、Ba2+、NO3-、SO32-四种离子在溶液中因发生氧化还原反应而不能大量共存 |
查看答案和解析>>
科目: 来源: 题型:
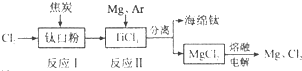
| A、反应Ⅰ中钛白粉(TiO2)作氧化剂 | ||||
B、反应Ⅱ的化学方程式为:2Mg+TiCl4
| ||||
| C、可以用N2代替Ar作为反应II中的保护气 | ||||
| D、该工艺中可以循环使用的物质只有Cl2 |
查看答案和解析>>
科目: 来源: 题型:
| △ |
| A、若反应中C和S的质量比为3:4,则n(KClO3):n(CO2)为1:1 |
| B、若反应中C和S的质量比为3:16,则n(KClO3):n(CO2)为2:1 |
| C、SO2通入NaHCO3溶液产生CO2,可证明非金属性S强于C |
| D、KClO3与SO2在强酸性溶液中反应制得ClO2,可证明SO2的还原性强于ClO2 |
查看答案和解析>>
科目: 来源: 题型:
| A、NaC1O3中氯元素得电子,化合价降低被还原 | B、该反应中反应物的总能量一定大于生成物的总能量 | C、NaC1O3和Na2SO4都属于离子化合物,且都含有共价键 | D、反应过程中,每转移4mol电子生成22.4L CO2(标准状况) |
查看答案和解析>>
科目: 来源: 题型:
| A、一维SiC纳米棒“比表面积”大,对微小粒子有较强的吸附能力 | B、上述反应中SiC既是氧化产物又是还原产物 | C、SiCl4是由极性键构成的非极性分子 | D、CCl4分子、SiCl4分子、SiC晶体中各原子都达到了8电子稳定结构 |
查看答案和解析>>
科目: 来源: 题型:
| A、该反应说明Fe(NO3)2溶液不宜加酸酸化 | B、该反应中氧化剂与还原剂物质的量之比为8:1 | C、若有1mol NO3-发生氧化反应,转移电子5mol | D、若将该反应设计成原电池,则负极反应为Fe3++e-═Fe2+ |
查看答案和解析>>
科目: 来源: 题型:
| A、只含有金属元素的离子不一定是阳离子 | B、金属阳离子被还原不一定得到金属单质 | C、氧化还原反应中,非金属单质必是氧化剂 | D、元素从化合态变为游离态时,一定被还原 |
查看答案和解析>>
科目: 来源: 题型:
| A、在焙烧明矾的反应中,还原剂与氧化剂的物质的量之比是3:4 | B、最后得到的K2SO4溶液呈中性,所以c(K+)=c(SO42-) | C、焙烧产生的SO2可用于制硫酸,焙烧948t明矾(M=474g/mol),若SO2的利用率为96%,可生产质量分数为98%的硫酸432t | D、工业上冶炼Al2O3制得Al,以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是Al+3NiO(OH)+NaOH═NaAlO2+3Ni(OH)2 |
查看答案和解析>>
科目: 来源: 题型:
| A、CuFeS2中硫的化合价为-1 | B、CuFeS2发生还原反应 | C、1mol CuFeS2完全反应转移13mol电子 | D、CuSO4和SO2既是氧化产物,又是还原产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com