
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
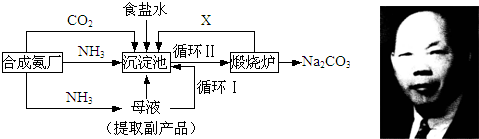
| 温度溶解度盐 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | -① | - | - | - |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
查看答案和解析>>
科目: 来源: 题型:多选题
查看答案和解析>>
科目: 来源: 题型:单选题
 Si+2CO↑的反应中,每当有1mol气体生成,就有4N4个电子转移
Si+2CO↑的反应中,每当有1mol气体生成,就有4N4个电子转移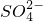 )>0.4mol?L-1
)>0.4mol?L-1查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
 ;对人类健康会产生危害,为了降低饮用水中N
;对人类健康会产生危害,为了降低饮用水中N ;的浓度,某兴趣小组提出以下两种方案:
;的浓度,某兴趣小组提出以下两种方案: ,还原产物为NH3;
,还原产物为NH3; ,还原产物为N2.
,还原产物为N2. +______OH-=______Al
+______OH-=______Al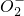 +______N2↑+______H2O
+______N2↑+______H2O查看答案和解析>>
科目: 来源: 题型:多选题
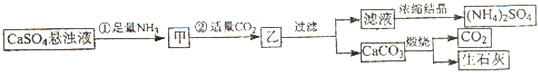
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
 钠与水反应的离子方程式是________.在探究金属钠与水反应(如图)的实验过程中,某课外小组同学记录了如下实验现象和实验结论:
钠与水反应的离子方程式是________.在探究金属钠与水反应(如图)的实验过程中,某课外小组同学记录了如下实验现象和实验结论:| 实验现象 | ⑦ | ________ | ③ | ________ |
| 实验结论 | ________ | ⑥ | ________ | ① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com