
科目: 来源: 题型:单选题
 如图是向MgCl2、AlCl3混合溶液中,开始滴加6ml试剂A,之 后改滴试剂B,所得沉淀y mol与试剂体积V(ml)间的关系.以下结论不正确的是
如图是向MgCl2、AlCl3混合溶液中,开始滴加6ml试剂A,之 后改滴试剂B,所得沉淀y mol与试剂体积V(ml)间的关系.以下结论不正确的是查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
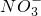 ⑤S2-⑥
⑤S2-⑥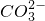 ⑦
⑦ ⑧Mg2+⑨Al3+ ⑩
⑧Mg2+⑨Al3+ ⑩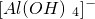 离子.其实,这些离子中有一部分不必再鉴定就能加以否定,你认为不必鉴定的离子组是
离子.其实,这些离子中有一部分不必再鉴定就能加以否定,你认为不必鉴定的离子组是查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
 H2(g)+
H2(g)+ C12(g)═HCl(g)△H=-92.3kJ/mol ③
C12(g)═HCl(g)△H=-92.3kJ/mol ③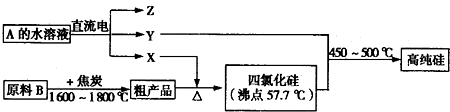
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
 、Fe3+
、Fe3+查看答案和解析>>
科目: 来源: 题型:解答题
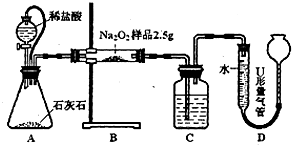 为测定含有Na2O杂质的Na2O2样品的纯度,甲、乙二位同学设计了二种不同的实验方案.
为测定含有Na2O杂质的Na2O2样品的纯度,甲、乙二位同学设计了二种不同的实验方案.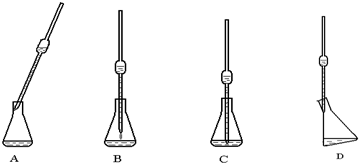
| 滴定次数 | 第一次滴定 | 第二次滴定 | 第三次滴定 |
| 消耗标准盐酸的体积(mL) | 24.98 | 25.00 | 25.02 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com