
科目: 来源: 题型:
| A、一定温度下,反应2NaCl(s)═2Na(s)+Cl2(g)的△H<0,△S>0 | B、温度一定时,向水中滴加少量酸或碱形成稀溶液,水的离子积常数Kw不变 | C、常温下,将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 | D、由于Ksp(BaSO4)<Ksp(BaCO3),因此不可能使BaSO4沉淀转化为BaCO3沉淀 |
查看答案和解析>>
科目: 来源: 题型:
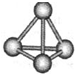 意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂lmolN-N吸收167kJ热量,生成1mol N≡N放出945kJ热量.根据以上信息和数据,下列说法正确的是( )
意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂lmolN-N吸收167kJ热量,生成1mol N≡N放出945kJ热量.根据以上信息和数据,下列说法正确的是( )| A、N4晶体属于由非极性键构成的分子晶体 | B、氮元素非金属性比磷强,可知N4沸点比P4(白磷)高 | C、1mol N4气体转变为N2气体吸收888kJ热量 | D、N4与N2互为同分异构体 |
查看答案和解析>>
科目: 来源: 题型:
A、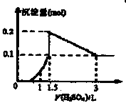 图表示向1L浓度均为0.1 mol?L-1的Ba(OH)2、NaAlO2混合液中逐滴加入0.1 mol?L-1稀H2SO4溶液,产生沉淀量的变化 | B、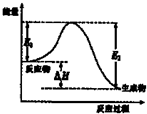 图中逆反应的热效应△H=E1-E2<0,所以逆反应为放热反应 | C、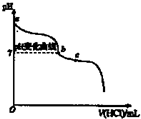 图表示向20mL 0.1mol?L-1 Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液,溶液pH的变化,c点溶液中:c(HCO3-)+2c(CO32-)+c(Cl-)>c(Na+) | D、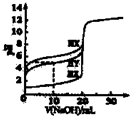 用0.1 mol?L-1NaOH溶液分别滴定浓度相同的三种一元酸,由图中曲线可确定HX的酸性最强 |
查看答案和解析>>
科目: 来源: 题型:
A、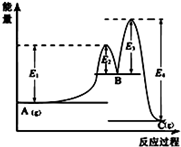 图中可以看出反应A(g)=C(g)的△H=(E1-E4)kJ?mol-1 | B、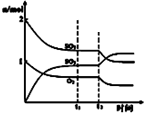 图中表示一定条件下进行的反应2SO2+O2═2SO3各成分的物质的量变化,t2时刻改变的条件可能是扩大了容器的体积 | C、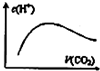 图中表示将CO2通入NaOH的稀溶液中,随着CO2的通入,溶液中水电离出的c(H+)变化关系 | D、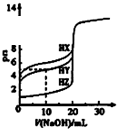 图中曲线表示用0.1000mol/L NaOH溶液分别滴定浓度相同的三种一元酸,由此可判断HX的酸性最强 |
查看答案和解析>>
科目: 来源: 题型:
| A、1,3-环己二烯加氢是吸热反应 | B、1,3-环己二烯比苯稳定 | C、苯比1,3-环己二烯稳定 | D、苯加氢生成环己烷是吸热反应 |
查看答案和解析>>
科目: 来源: 题型:
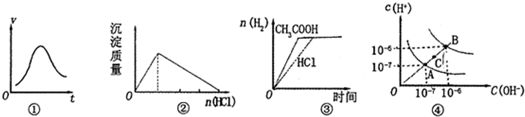
| A、图①表示一定条件下某化学反应的速率随时间变化的趋势图,该反应一定为放热反应 | B、图②表示在四羟基合铝酸钠溶液中加入盐酸,产生沉淀的质量变化 | C、图③表示等体积、等物质的量浓度的盐酸和醋酸溶液,分别加入足量镁粉,产生H2的物质的量的变化 | D、图④为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法 |
查看答案和解析>>
科目: 来源: 题型:
| A、压缩容器体积,平衡不移动 | B、升高温度,平衡正向移动,v(正)增大、v(逆)减小 | C、A(s)与B(g)的总能量高于2C(g)的总能量 | D、反应:2A(g)+2B(g)?4C(g)△H>2a,(a<0) |
查看答案和解析>>
科目: 来源: 题型:
| A、已知2SO2(g)+O2(g)?2SO3(g)△H<0,该反应在任何温度下均可自发进行 | ||
| B、0.01 mol?L-1NaHCO3溶液中c(Na+)=c(HCO3 -)+2c(CO32-)+c(H2CO3) | ||
C、25℃,0.1mol?L-1 K2CO3溶液中
| ||
| D、室温下,Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=9.0×10-12,向浓度相等的Na2CrO4和NaCl的混合稀溶液中滴加0.01mol?L-1 AgNO3溶液,先生成Ag2CrO4沉淀 |
查看答案和解析>>
科目: 来源: 题型:
A、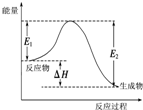 图中逆反应的热效应△H=E1-E2<0,所以逆反应为放热反应 | B、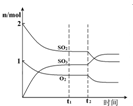 图表示一定条件下进行的反应2SO2+O2═2SO3各成分的物质的量变化,t2时刻改变的条件可能是缩小容器体积 | C、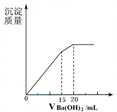 图表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20 mL Ba(OH)2溶液时铝离子恰好沉淀完全 | D、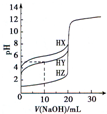 用0.1000mol/L NaOH溶液分别滴定浓度相同的三种一元酸,由图中曲线可确定HX的酸性最强 |
查看答案和解析>>
科目: 来源: 题型:
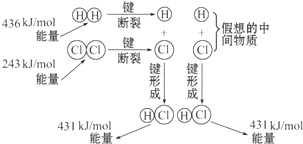 如图所示是101kPa时,氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )
如图所示是101kPa时,氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )| A、此反应的热化学方程式为:H2(g)+Cl2(g)═2HCl(g)△H=+183kJ?mol-1 | B、2molHCl分子中的化学键形成时要释放862kJ能量 | C、1molH2中的化学键断裂时需要吸收436kJ能量 | D、此反应的热化学方程式为:1/2H2(g)+1/2Cl2(g)═HCl(g)△H=-91.5kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com