
科目: 来源: 题型:
| A、化学键断裂吸收能量,化学键生成放出能量 | B、化学反应中有物质变化也有能量变化 | C、需要加热的化学反应不一定是吸热反应 | D、图中所示的反应为放热反应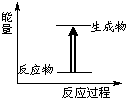 |
查看答案和解析>>
科目: 来源: 题型:
| A、凡需要加热的反应一定是吸热反应 | B、氢分子(H-H)变成2个氢原子时会放出能量 | C、H2O与CaO的化合反应是放热反应 | D、反应物的总能量一定比生成物的总能量高 |
查看答案和解析>>
科目: 来源: 题型:
| A、所有的化学反应都释放能量 | B、化学反应中的能量变化与化学键无关 | C、NaOH溶液与盐酸反应释放能量 | D、NH4Cl晶体与Ba(OH)2?8H2O反应释放能量 |
查看答案和解析>>
科目: 来源: 题型:

| A、每生成2分子AB吸收bkJ热量 | B、该反应热△H=(b-a)kJ?mol-1 | C、反应物的总能量低于生成物的总能量 | D、断裂1molA-A和1molB-B键,放出akJ能量 |
查看答案和解析>>
科目: 来源: 题型:
| A、化学变化过程是原子的重新组合过程 | B、化学反应中能量变化多少与其反应物用量有关 | C、一个化学反应,当反应物能量大于生成物能量时,反应放热 | D、化学反应中的能量变化都是以热量形式表现出来 |
查看答案和解析>>
科目: 来源: 题型:
A、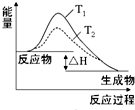 表示SO2与O2反应过程中的能量变化,其中T1>T2 | B、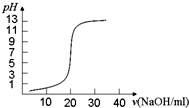 表示0.1000mol?L-1 NaOH溶液滴定20.00ml 0.1000mol?L-1 CH3COOH溶液所得到的滴定曲线 | C、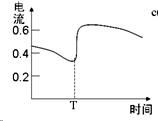 表示酸性介质Zn-Cu原电池反应过程中的电流强度的变化,T时可能加入了H2O2 | D、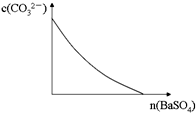 表示在饱和Na2CO3溶液中逐步加BaSO4固体后,溶液中c(CO32-)的浓度变化 |
查看答案和解析>>
科目: 来源: 题型:
| A、常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)能自发进行,则该反应的△H<0 | B、铅蓄电池放电时的负极和充电时的阴极均发生氧化反应 | C、常温下Ksp(Ag2CrO4)=1.1×10-12,Ksp(AgCl)=1.8×10-10,则Ag2CrO4的溶解度小于AgCl | D、等体积、物质的量浓度的HA与NaA(HA为弱酸)混合溶液,其酸碱性取决于Ka(HA)的大小 |
查看答案和解析>>
科目: 来源: 题型:
| 13 |
| 2 |
| A、+8Q kJ?mol-1 |
| B、-8Q kJ?mol-1 |
| C、-16Q kJ?mol-1 |
| D、+16Q kJ?mol-1 |
查看答案和解析>>
科目: 来源: 题型:
| 容器 | 起始各物质的物质的量/mol | 达到平衡时体系能量的变化 | |||
| SO2 | O2 | SO3 | Ar | ||
| 甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2 |
| 丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
| A、Q1=Q2=Q3=197kJ |
| B、若在上述条件下反应生成2mol SO3(s)的反应热为△H1,则△H1<-197kJ?mol-1 |
| C、甲、乙、丙3个容器中反应的平衡常数不相等 |
| D、达到平衡时,丙容器中SO2的体积分数最大 |
查看答案和解析>>
科目: 来源: 题型:
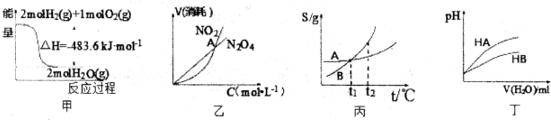
| A、丙表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A | B、丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度的NaB溶液的pH | C、甲表示H2与O2发生反应过程中的能量变化,则H2的标准燃烧热为△H=-241.8kJ?mol-1 | D、乙表示恒温恒容条件下发生的可逆反应2NO2?N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com