
科目: 来源: 题型:
| A、物质的化学变化都伴随着能量变化 | B、凡是吸热反应都需要加热 | C、表示中和热的热化学方程式:NaOH+HCl═NaCl+H2O△H=-57.3 kJ?mol-1 | D、等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 |
查看答案和解析>>
科目: 来源: 题型:
| A、反应热和焓变的单位都是kJ | B、如果反应是在恒温恒压条件下进行的,此时的反应热与焓变相等 | C、如果反应是在恒温恒容条件下进行的,此时的反应热与焓变相等 | D、任何化学反应的反应热均可通过实验直接测定 |
查看答案和解析>>
科目: 来源: 题型:
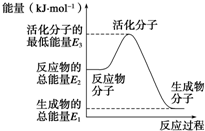 已知:①N2(g)+O2(g)═2NO(g)△H1=+180kJ?mol-1
已知:①N2(g)+O2(g)═2NO(g)△H1=+180kJ?mol-1| A、反应②中的能量变化如图所示,则△H2=E1-E3 | B、H2的燃烧热为241.8 kJ?mol-1 | C、由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N2和3 mol H2,反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2充分反应后放出的热量为Q2 kJ,则184.8>Q2>2Q1 | D、氨的催化氧化反应为4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=+906 kJ?mol-1 |
查看答案和解析>>
科目: 来源: 题型:
| A、加入催化剂,改变了反应的途径,反应的△H也随之改变 | B、改变压强,平衡不发生移动,反应放出的热量不变 | C、升高温度,反应速率加快,反应放出的热量不变 | D、向容器中加入、TaS2可以提高I2的转化率 |
查看答案和解析>>
科目: 来源: 题型:
| A、甲烷的标准燃烧热为-890.3kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ?mol-1 | B、相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 | C、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H<0 | D、已知①2H2(g)+O2(g)═2H2O(g)△H1=a kJ?mol-1②2H2(g)+O2(g)═2H2O(l)△H2=b kJ?mol-1,则a>b |
查看答案和解析>>
科目: 来源: 题型:
A、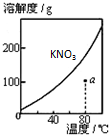 图表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 | B、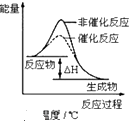 图表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 | C、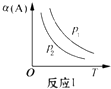 图表示反应aA(g)+bB(g)?cC(g)表示改变某一条件对化学平衡的影响(纵坐标表示转化率),若p1>p2 此反应自发进行,必须满足的条件是高温 | D、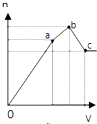 图表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀的物质的量的变化曲线 |
查看答案和解析>>
科目: 来源: 题型:
| A、-69.4 kJ?mol-1 | B、-45.2 kJ?mol-1 | C、+69.4 kJ?mol-1 | D、+45.2 kJ?mol-1 |
查看答案和解析>>
科目: 来源: 题型:
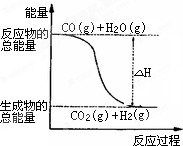 已知热化学方程式:①CO(g)+
已知热化学方程式:①CO(g)+| 1 |
| 2 |
| 1 |
| 2 |
| A、H2的燃烧热为241.8kJ?mol-1 | ||
| B、由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41.2 kJ?mol-1 | ||
| C、H2(g)转变成H2O(g)的化学反应一定要释放能量 | ||
D、根据②推知反应H2(g)+
|
查看答案和解析>>
科目: 来源: 题型:
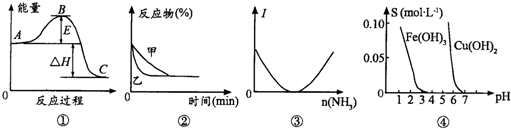
| A、根据图①判断,物质A反应生成物质C的△H>0 | B、压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响可用图②表示 | C、往乙酸溶液中通入氨气至过量,溶液导电能力(I)的变化可用图③表示 | D、根据图④溶解度(s)与溶液pH的关系,若要除去CuSO4溶液中的Fe3+,可向溶液中加入适量CuO,调节pH至4 |
查看答案和解析>>
科目: 来源: 题型:
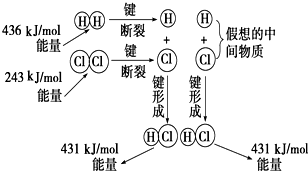 如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )
如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )| A、1 molH2中的化学键断裂时需要吸收436 kJ能量 | ||||
| B、2 molHCl分子中的化学键形成时要释放862 kJ能量 | ||||
| C、此反应的热化学方程式为:H2(g)+Cl2(g)═2HCl(g)△H=+183 kJ/mol | ||||
D、此反应的热化学方程式为:
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com