
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
 MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:多选题
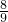 (同温、同压),原混合气体中H2O、O2、CO2物质的量之比可能为
(同温、同压),原混合气体中H2O、O2、CO2物质的量之比可能为查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
 、Cl-、Br-、I-中的若干种,现取部分溶液依次进行如下实验:
、Cl-、Br-、I-中的若干种,现取部分溶液依次进行如下实验: 、I-
、I-查看答案和解析>>
科目: 来源: 题型:解答题
 合金是建筑航空母舰的主体材料.
合金是建筑航空母舰的主体材料.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com