
科目: 来源: 题型:解答题
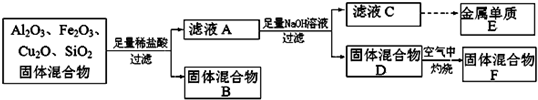
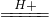 Cu+Cu2+;②AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-
Cu+Cu2+;②AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-查看答案和解析>>
科目: 来源: 题型:单选题
| 选项 | 实 验 事 实 | 结 论 |
| A | 其他条件相同,硫代硫酸钠溶液浓度越大,析出硫沉淀所需时间越短 | 当其他条件不变时,增大反应物浓度化学反应速率加快 |
| B | 在化学反应前后,催化剂的质量和化学性质都没有发生改变 | 催化剂一定不参与化学反应 |
| C | 等体积H+浓度相同的盐酸和醋酸同时分别与少量等质量的形状相同的锌粒反应 | 产生氢气的质量相同 |
| D | 在容积可变的密闭容器中发生反应: H2(g)+I2(g)?2HI(g),把容积缩小一倍 | 正反应速率加快,逆反应速率不变 |
查看答案和解析>>
科目: 来源: 题型:解答题
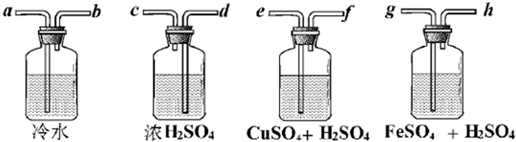
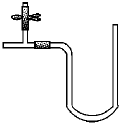 I.“阿波罗登月计划”总指挥韦伯在“阿波罗”登月成功后曾说:“阿波罗计划”中没有一项新发明的技术,都是现成的技术,关键在于综合.综合也是创新,例如可以用玻璃管制成的U形管、T形管、乳胶管、弹簧夹连接成如图所示的一种装置,在U型管中加入适量的红色溶液,即得简单U型气压计,我们可将它应用于多项实验,如:A.证明空气中的氧气参与氧化还原反应的实验(如铁生锈);B.溶解热效应实验(如硝酸铵溶于水);C.装置的气密性检验实验;D.检验某些气体性质的实验(如CO2,SO2、Cl2等与碱溶液的反应)等等.请从A或B中选择一项实验,画出该实验的装置图,写出实验名称.要求:①除U形气压计外,其他实验仪器或用品仅能从以下仪器中选取:广口瓶、小试管、胶头滴管、橡皮塞、乳胶管、导管;②实验药品或试剂自定,但需在图中注明.
I.“阿波罗登月计划”总指挥韦伯在“阿波罗”登月成功后曾说:“阿波罗计划”中没有一项新发明的技术,都是现成的技术,关键在于综合.综合也是创新,例如可以用玻璃管制成的U形管、T形管、乳胶管、弹簧夹连接成如图所示的一种装置,在U型管中加入适量的红色溶液,即得简单U型气压计,我们可将它应用于多项实验,如:A.证明空气中的氧气参与氧化还原反应的实验(如铁生锈);B.溶解热效应实验(如硝酸铵溶于水);C.装置的气密性检验实验;D.检验某些气体性质的实验(如CO2,SO2、Cl2等与碱溶液的反应)等等.请从A或B中选择一项实验,画出该实验的装置图,写出实验名称.要求:①除U形气压计外,其他实验仪器或用品仅能从以下仪器中选取:广口瓶、小试管、胶头滴管、橡皮塞、乳胶管、导管;②实验药品或试剂自定,但需在图中注明.
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
 数为0.5NA
数为0.5NA查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
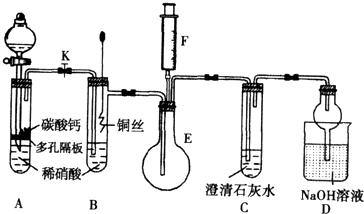
查看答案和解析>>
科目: 来源: 题型:解答题
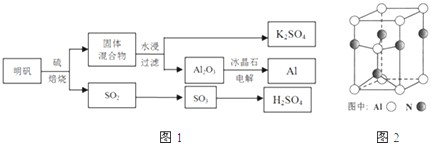
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com