
科目: 来源: 题型:
| 3 |
| 2 |
| A、-2491 kJ?mol-1 |
| B、+859 kJ?mol-1 |
| C、-1403 kJ?mol-1 |
| D、-859 kJ?mol-1 |
查看答案和解析>>
科目: 来源: 题型:
| ||
| A、Q1>Q2 |
| B、Q1=Q2 |
| C、Q1<Q2 |
| D、无法比较 |
查看答案和解析>>
科目: 来源: 题型:
| A、-859 kJ?mol-1 | B、+859 kJ?mol-1 | C、-1403 kJ?mol-1 | D、-2491 kJ?mol-1 |
查看答案和解析>>
科目: 来源: 题型:
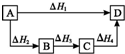
| A、△H1=△H2=△H3=△H4 | B、△H1+△H2=△H3+△H4 | C、△H1+△H2+△H3=△H4 | D、△H1=△H2+△H3+△H4 |
查看答案和解析>>
科目: 来源: 题型:
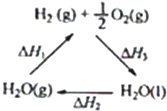 某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO.其过程如下:
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO.其过程如下:| 太阳能 |
| ① |
| 900℃ |
| ① |
| A、该过程中CeO2没有消耗 |
| B、该过程实现了太阳能向化学能的转化 |
| C、图中△H1=△H2+△H3 |
| D、以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH--2e-=CO32-+2H2O |
查看答案和解析>>
科目: 来源: 题型:
| 1 |
| 2 |
| A、碳的燃烧热大于110.5kJ/mol |
| B、浓硫酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
| C、氢气的燃烧热为241.8 kJ/mol |
| D、2H2(g)+O2(g)═2H2O(l)的反应热为△H=-571.6 kJ/mol |
查看答案和解析>>
科目: 来源: 题型:
| 1 |
| 2 |
| A、12g C燃烧生成CO时,放出221kJ热量 | ||
| B、碳的燃烧热△H=-393.5kJ/mol | ||
C、CO(g)+
| ||
| D、稀醋酸与稀NaOH溶液反应生成1mol水时,放出57.3kJ热量 |
查看答案和解析>>
科目: 来源: 题型:
| A、-10.4KJ?mol-1 | B、-125KJ?mol-1 | C、+10.4KJ?mol-1 | D、+125KJ?mol-1 |
查看答案和解析>>
科目: 来源: 题型:
| A、+3269.65kJ?mol-1 | B、+2821.6 kJ?mol-1 | C、+2821.6 kJ | D、+3896.92 kJ?mol-1 |
查看答案和解析>>
科目: 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| A、+131.3 kJ?mol-1 |
| B、-131.3 kJ?mol-1 |
| C、+352.3 kJ?mol-1 |
| D、-352.3 kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com