
科目: 来源: 题型:
| A、硫酸铜饱和溶液降低温度时有晶体析出 | B、(NH4)2CO3(s)═NH4HCO3(s)+NH3(g)△H=+74.9kJ/mol | C、CaO(s)+CO2(g)═CaCO3(s)△H=-175.7kJ/mol | D、2H2(g)+O2(g)═2H2O(l)△H=-285.8kJ/mol |
查看答案和解析>>
科目: 来源: 题型:
| A、△H>0,△S>0 | B、△H>0,△S<0 | C、△H<0,△S>0 | D、△H<0,△S<0 |
查看答案和解析>>
科目: 来源: 题型:
| A、凡是放热反应都是自发的,吸热反应都是非自发的 | B、自发反应的熵一定增大,非自发反应的熵一定减小或不变 | C、△H<0、△S<0的反应一定能自发进行 | D、△H>0、△S<0的反应一定不能自发进行 |
查看答案和解析>>
科目: 来源: 题型:
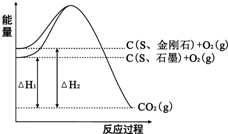 已知25℃、101kPa下,如图所示,石墨的燃烧热为393.5kJ/
已知25℃、101kPa下,如图所示,石墨的燃烧热为393.5kJ/| A、金刚石比石墨稳定 | B、C(s、石墨)=C(s、金刚石)△H=+1.5kJ/mol | C、△H1<△H2 | D、如果使用催化剂,△H1和△H2都变小 |
查看答案和解析>>
科目: 来源: 题型:
| A、反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 | B、电解精炼铜的过程中,每转移NA个电子时,阳极溶解铜的质量为32g | C、吸热反应“TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0 | D、HCl和NaOH反应的中和热△H=-57.3kJ?mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ?mol-1 |
查看答案和解析>>
科目: 来源: 题型:
| A、1mol H2O在不同状态时的熵值:S[H2O(s)]<S[H2O(g)] | B、△H<0的化学反应一定能自发进行 | C、CaCO3(s)?CaO(s)+CO2(g)△H>0,能否自发进行与温度有关 | D、△H<0,△S<0的反应高温下不易自发进行 |
查看答案和解析>>
科目: 来源: 题型:
| A、电解质的电离是在通电的条件下进行的 | B、用湿润的pH试纸测定溶液的pH | C、碳酸铵能自发分解是因为生成了易挥发的气体,使体系的熵增大 | D、H2O(g)═H2O(l)是放热反应 |
查看答案和解析>>
科目: 来源: 题型:
| A、放热反应都是自发的,吸热反应都非自发 | B、熵增大反应不一定自发,但自发反应熵一定增大 | C、判断反应进行的方向,应综合考虑体系的焓变和熵变 | D、自发反应是不可逆反应 |
查看答案和解析>>
科目: 来源: 题型:
| A、凡是放热反应都是自发的,吸热反应都是非自发的 | B、量热计可用于测定酸碱中和反应的反应热;pH计不能用于酸碱中和滴定终点的判断 | C、升高温度,可使单位体积内活化分子数增多,反应速率加快 | D、使用催化剂可降低反应的△H和反应的活化能,从而提高化学反应速率 |
查看答案和解析>>
科目: 来源: 题型:
| A、在温度、压强一定的条件下,焓因素和熵因素共同决定一个化学反应的方向 | B、温度、压强一定时,放热的熵增加反应不一定能自发进行 | C、反应焓变是决定反应能否自发进行的唯一因素 | D、固体的溶解过程与熵变无关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com