
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
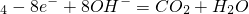
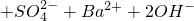 =BaSO4↓+2H2O
=BaSO4↓+2H2O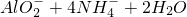
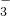 +H2O?
+H2O?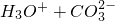
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
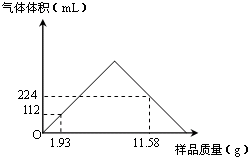 含钡化合物在实验室和工业生产中都有广泛的用途.
含钡化合物在实验室和工业生产中都有广泛的用途.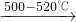 2BaO2.现有16.0吨的氧化钡在足量的氧气中加热反应后,固体的质量变为17.6吨.那么实际参加反应的氧化钡的质量为______吨.
2BaO2.现有16.0吨的氧化钡在足量的氧气中加热反应后,固体的质量变为17.6吨.那么实际参加反应的氧化钡的质量为______吨.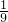 ,求该反应条件下混合气体的平均式量?
,求该反应条件下混合气体的平均式量?查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com