
科目: 来源:2013-2014学年高考化学二轮专题冲刺第16讲 物质结构与性质练习卷(解析版) 题型:填空题
A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大。第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素。D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满。请回答下列问题:
(1)A、B、C的第一电离能由小到大的顺序是________(用对应的元素符号表示);D原子的基态电子排布式为____________________________________________________。
(2)A的最高价氧化物对应的水化物分子中,其中心原子采取________杂化;BC的空间构型为________(用文字描述)。
(3)1 mol AB-中含有的π键个数为________。
(4)如图是金属Ca和D所形成的某种合金的晶胞结构示意图,则该合金中Ca和D的原子个数比是________。
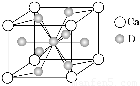
(5)镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力。已知镧镍合金LaNin晶胞体积为9.0×10-23 cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=________(填数值);氢在合金中的密度为________。
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮专题冲刺第16讲 物质结构与性质练习卷(解析版) 题型:填空题
已知:A、B、C、D、E、F六种元素,原子序数依次增大。A原子核外有两种形状的电子云,两种形状的电子云轨道上电子数相等;B是短周期中原子半径最大的元素;C元素3p能级半充满;E是所在周期电负性最大的元素;F是第四周期未成对电子最多的元素。
试回答下列有关的问题。
(1)写出F元素的电子排布式:___________________________________________。
(2)已知A元素的一种氢化物分子中含四个原子,则在该化合物的分子中A原子的杂化轨道类型为_____________________________________________________________。
(3)已知C、E两种元素形成的化合物通常有CE3、CE5两种。这两种化合物中一种为非极性分子,一种为极性分子,属于极性分子的化合物的分子空间构型是_________________。
(4)B、C、D、E的第一电离能由大到小的顺序是________(写元素符号)。四种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序是____________
______________________________________________________________(写化学式)。
(5)由B、E两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如下图所示为B、E形成化合物的晶胞结构图以及晶胞的剖面图:
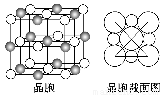
晶胞中距离一个B+最近的B+有________个。若晶体密度为ρ g·cm-3,阿伏加德罗常数的值用NA表示,则E-的离子半径为________cm(含NA与ρ的式子表达)。
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮专题冲刺第16讲 物质结构与性质练习卷(解析版) 题型:填空题
Ⅰ.CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
已知:①CuCl可以由CuCl2用适当的还原剂如SO2、SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O 2CuCl↓+4H++SO42-
2CuCl↓+4H++SO42-
2CuCl2+SnCl2=2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子:
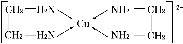
请回答下列问题:
(1)基态Cu原子的核外电子排布式为____________;H、N、O三种元素的电负性由大到小的顺序是_________________________________________________________。
(2)SO2分子的空间构型为________;与SnCl4互为等电子体的一种离子的化学式为________________________________________________________________________。
(3)乙二胺分子中氮原子轨道的杂化类型为________。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是_________________________________。
(4)②中所形成的配离子中含有的化学键类型有________(填字母)。
a.配位键 b.极性键 c.离子键 d.非极性键
Ⅱ.固体二氧化碳外形似冰,受热汽化无液体产生,俗称“干冰”,根据干冰晶胞结构回答:
(5)干冰中一个分子周围有________个紧邻分子。
(6)堆积方式与干冰晶胞类型相同的金属有________(从“Cu、Mg、K、Po”中选出正确的),其空间利用率为________。
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮专题冲刺第17讲 化学与技术练习卷(解析版) 题型:填空题
废旧硬质合金刀具中含碳化钨(WC)、金属钴(Co)及少量杂质铁,利用电解法可回收WC和Co。工艺流程简图如下:
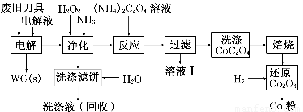
(1)电解时废旧刀具做阳极,不锈钢做阴极,HCl溶液为电解液。阴极主要的电极反应式为________________________________________________________________________。
(2)净化步骤所得滤饼的主要成分是________。回收的洗涤液代替水配制电解液,目的是回收利用其中的________。
(3)溶液Ⅰ的主要成分是________。洗涤CoC2O4不充分对最终产品纯度并无明显影响,但焙烧时会造成环境污染,原因是____________________________________________。
(4)将Co2O3还原成Co粉的化学反应方程式为____________________。
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮专题冲刺第17讲 化学与技术练习卷(解析版) 题型:填空题
水处理技术在生产、生活中应用广泛。
(1)工业上常用绿矾作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加入绿矾。请解释这一做法的原因:_______________________________________________________________________。
(用必要的离子方程式和文字做答)
(2)根据水中Ca2+、Mg2+的多少,把天然水分为硬水和软水,硬水必须经过软化才能使用。①硬水软化的方法通常有________、________和离子交换法。离子交换树脂使用一段时间后,逐渐由NaR型变为CaR2(或MgR2)型,而失去交换能力。把CaR2(或MgR2)型树脂置于________中浸泡一段时间,便可再生。
②当洗涤用水硬度较大时,洗衣粉与肥皂相比,________洗涤效果较好,原因是________________________________________________________________________。
(3)我国某地苯胺大量泄漏于生活饮用水的河道中,当地采取的应急措施之一是向河水中撒入大量的活性炭,活性炭的作用是________________________________________。
(4)若生活污水中含大量的氮化合物,通常用生物膜脱氮工艺进行处理。首先在硝化细菌作用下将NH4+氧化为NO3-:________NH4++________O2=________NO3-+________H++______H2O,然后,加入甲醇与NO3-生成N2:______NO3-+______CH3OH=________N2↑+________CO2↑+________H2O+________OH-。
试配平以上两个离子方程式。
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮专题冲刺第17讲 化学与技术练习卷(解析版) 题型:填空题
化学在材料的发展过程中起着很重要的作用,2012年度国家最高科学技术奖授予郑哲敏院士、王小谟院士,两人均在材料方面作出了巨大贡献,为国家创造出较大的经济效益。
(1)石灰石、生石灰和熟石灰均是重要的化工原料,下列工业生产中,不可能用到上述原料的是________(填序号)。
①炼铁;②炼钢;③从海水中提取镁;④铝的冶炼;⑤制水泥;⑥制玻璃;⑦制漂白粉;⑧烧制陶瓷
(2)神州八号与天宫一号的成功对接与分离,标志着我国航天工业发展进入了新阶段。下列选项中的描述与化学研究领域无关的是________。
A.燃料燃烧为神州八号升空提供动力
B.与地面指挥中心联系的无线电通讯
C.宇航服使用的合成纤维等新材料
D.太空舱中利用NiFeO4处理呼出的废气
(3)玻璃钢是将玻璃纤维和高分子材料复合而成的复合材料,它具有强度高、质量轻、耐腐蚀、抗冲击、绝缘性能好等优良性能,其中基体是__________,增强体是________。
(4)橄榄石型LiFePO4是一种锂离子电池正极材料,其中Fe元素显+2价。常向LiFePO4中加入少量活性炭黑,其作用除了可以改善LiFePO4的导电性能外,还能____________________。
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮专题冲刺第17讲 化学与技术练习卷(解析版) 题型:填空题
某自来水厂利用河水处理成自来水的工艺流程示意图如下图所示:
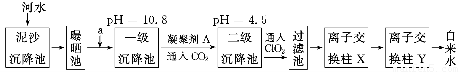
提供的试剂:饱和Na2CO3溶液、NaOH溶液、生石灰、CCl4、BaCl2溶液、KOH溶液
(1)为除去水中含有的Ca2+、Mg2+、HCO3-、Cl-、SO42-,试剂a代表两种化学物质,主要是除去水中SO42-、Mg2+和HCO3-,这两种试剂是________和________(只填化学式)。
(2)凝聚剂A常用FeSO4·7H2O,最终生成红褐色胶体沉淀,该胶状沉淀的化学式为________,可以除去其中的悬浮固体颗粒,该过程是________(填序号)。
A.只有物理变化,无化学变化
B.只有化学变化,无物理变化
C.既有化学变化,又有物理变化
(3)通入CO2的目的是__________和__________。
(4)传统的氧化剂是Cl2,现代工艺用ClO2取代Cl2,通入ClO2的作用是________________________;优点是________________________________。
(5)离子交换柱X、Y中有一种是H+型交换柱,另一种是OH-型离子交换柱,目的是除去水中残留的杂质离子,则X应是哪种交换柱?________(填“H+型”或“OH-型”);如果两个交换柱位置颠倒会产生什么后果?_______________________________________
________________________________________________________________________。
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮专题冲刺第17讲 化学与技术练习卷(解析版) 题型:填空题
工业上用铝土矿(成分为氧化铝、氧化铁)制取铝的流程如下:
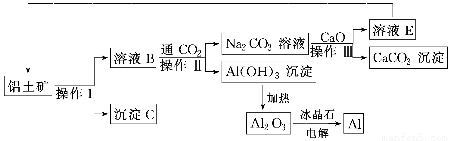
请回答下列问题。
(1)操作Ⅰ、操作Ⅱ、操作Ⅲ都用到的玻璃仪器有________________________________。
(2)写出由溶液B生成Al(OH)3的离子方程式:_________________________________________________________。
(3)工艺流程中涉及氧化还原反应的化学方程式为______________________________________________________________________。
(4)生产过程中,除NaOH、H2O可以循环使用外,还可以循环使用的物质有________(填化学式)。用此法制取铝的副产品是________(填化学式)。
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮专题冲刺第17讲 化学与技术练习卷(解析版) 题型:填空题
海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列。从海水中提取食盐和溴的过程如下:
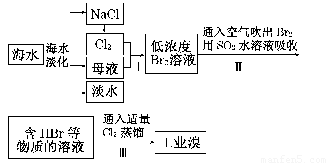
(1)请列举海水淡化的两种方法:________、________。
(2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、________、________或H2、________。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为____________________________________________________________________。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为
________________________________________________________________________。
由此反应可知,除环境保护外,在工业生产中应解决的主要问题是_________________________________________________________________。
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料:Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如下装置简图:
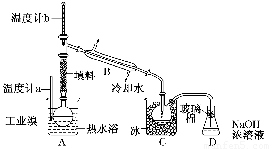
请你参与分析讨论:
①图中仪器B的名称________。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是____________________________________________________________。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件________________________________________________________________________。
查看答案和解析>>
科目: 来源:2013-2014学年高考化学二轮专题冲刺第17讲 化学与技术练习卷(解析版) 题型:填空题
如图是传统的工业生产金属铝的基本流程图。
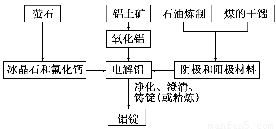
请回答:
(1)金属铝常用来制造容器,但铝制餐具不宜用来蒸煮或长时间存放酸性、碱性等食物,写出铝与氢氧化钠溶液反应的离子方程式:_____________________________________。
石油炼制和煤的干馏产品________(填物质名称)作电解铝的阴极和阳极材料。
(2)在冶炼过程中,阳极材料需要定期进行更换,原因是该极材料不断被消耗,产生这种现象的原因是____________________________________(用化学方程式表示)。
(3)工业上通过电解熔融的MgCl2制取金属镁,电解反应方程式为________________。镁和铝都是活泼金属,为什么在电解冶炼过程中,一个用氯化物,一个用氧化物,请说明理由。________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com