
科目: 来源:2013-2014学年福建省漳州市高三3月质检理综化学试卷(解析版) 题型:选择题
以NA代表阿伏加德罗常数的值,下列说法申正确的是
A.9g18O2含有的中子数为5NA
B.标准状况下,0.5NABr2所占的体积约为11.2L
C.常温下,1L0.1mol·L-1NH4NO3溶液中含有的NH4+数为0.1NA
D.一定条件下,lmol N2和3mol H2在密闭容器充分反应,生成N-H键的数目为6NA
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市高三3月质检理综化学试卷(解析版) 题型:选择题
根据水溶液中存在的平衡关系,判断下列说法正确的是
A.往水中滴加少量氢氧化钠稀溶液,Kw变小
B.往AgCl悬浊液中加入0.1mol·L-1NaI溶液,无明显现象产生
C.室温下,稀释0.1mol·L-1的醋酸,溶液中c(CH3COO-)·c(H+)不变
D.等体积等浓度的氨水与盐酸混合后所得溶液显酸性
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市高三3月质检理综化学试卷(解析版) 题型:选择题
下列图示的有关说法正确的是

A.装置①中负极反应式为H2+2e一=2H+
B.装置①工作时,外电路电子由a电极流向b电极
C.若采用装置②精炼铜,则d为粗铜,c为纯铜
D.若装置②用惰性电极电解稀H2SO4溶液,则溶液pH升高
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市高三3月质检理综化学试卷(解析版) 题型:选择题
下列图示与对应的叙述相符的是
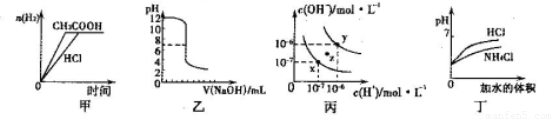
A.甲图曲线表示向等体积、等物质的量浓度的盐酸和醋酸溶液中分别加人足量镁粉产生H2的物质的量的变化
B.乙表示将0.01mol·L-lNaOH溶液滴人到稀盐酸中的滴定曲线
C.丙为水的电离曲线,从z点刭x点,可采用在水中加入适量NaOH固体的方法
D.丁中曲线表示将pH相同的NH4C1溶液和盐酸稀释相同倍数时,二者pH的变化
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市高三3月质检理综化学试卷(解析版) 题型:选择题
现有一份单质铁和氧化铁的混合物,其物质的量共a mol,加入一定量的盐酸后固体全部溶解,收集到b mol氢气。下列有关叙述中正确的是
A.反应后的溶液中加入氯水不变色
B.反应后的溶液可继续溶解金属铜
C.原混台物中氧化铁的物质的量为 (a-b)mol
(a-b)mol
D.原混合物中单质铁的物质的量为b mol
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市高三3月质检理综化学试卷(解析版) 题型:填空题
短周期元素R、Q、M、T在元素周期表中的相对位置如下表,已知R原子最外层电子数与次外层电子数之比为2:1。
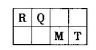
(1)人的汗液中台有T的简单离子,其离子结构示意图为_________________;元素M在元素周期表中的位置是___________________。
(2)R的最高价氧化物所含的化学键类型是__________键(选填“离子”或“共价”)。
(3)加热时,Q的最高价氧化物对应水化物的浓溶液与单质R反应的化学方程式为__________(用具体的化学式表示)。
(4)在一定条件下甲、乙、丙有如下转化:甲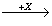 乙
乙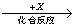 丙,若其中甲是单质,乙、丙为化合物,x是具有氧化性的无色气体单质,则甲的化学组成不可能是________(选填序号,下同)。
丙,若其中甲是单质,乙、丙为化合物,x是具有氧化性的无色气体单质,则甲的化学组成不可能是________(选填序号,下同)。
①R???? ②Q2?? ③M???? ④T2
(5)工业上,常利用。RO与MO2反应生成固态M单质和RO2,从而消除这两种气体对大气的污染。
已知:2RO(g)+O2(g)=2RO2(g)? △H=-akJ·mol-l
M(s)+O2(g)=MO2(g)????? △H=-bkJ·mol-l
则反应2RO(g)+MO2(g)=2RO2(g)+M(s)?? △H=___________。
(6)元素T的含氧酸HTO具有漂白性。往20mL 0.0lmol·L-l的HTO溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如下图所示。据此判断:该烧碱溶液的浓度为______________mol·L-l;下列有关说法正确的是_______________。
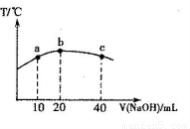
①HTO的电离常数:b点>a点
②由水电离出的c(OH—):b点<c点
③从a点到b点,混合溶液中可能存在:c(TO—)= c(Na+)
④从b点到c点,混合溶液中一直存在:c(Na+)>c(TO-)>c(OH-)>c(H+)
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市高三3月质检理综化学试卷(解析版) 题型:填空题
氧化铁在工业上具有广泛的应用。
I.据报道,一定条件下利用FeO2与甲烷反应可制取“纳米级”的金属铁。其反应如下:
Fe2O3(s)+3CH4(g)=2Fe(s)+3CO(g)+6H2(g)? △H>0
(1)若反应在2L的密闭容器中进行,5min后达到平衡,测得反应生成Fe的质量为l.12g。则该段时间内CH4的平均反应速率为 ________________。
(2)反应达到平衡后,保持其他条件不变,仅改变某一相关元素,下列说法正确的是___(选填序号)。
a.若加入催化剂,v正增大,平衡向右移动
b.若温度升高,平衡常数K减小
c.若增大Fe2O3的量,平衡向右移动
d.若从反应体系中移走部分CO,可提高CH4的转化率
Ⅱ.工业上利用硫铁矿烧渣(主要成分为Fe2O3、A12O3、SiO2等)为原料提取Fe2O3,工艺
流程如下:试回答下列问题:
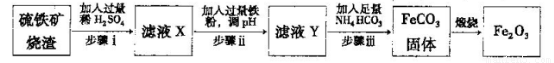
(3)步骤i烧渣中A12O3溶解的离子方程式为________________。
(4)步骤i、ⅱ、ⅲ都要进行的操作名称是__________________。
(5)结合下图,判断步骤ⅱ中调节溶液的pH不高于_________________。
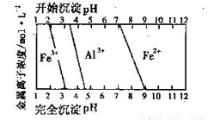
(6)已知

计算反应Fe2+(aq)+2HCO3-(aq) FeCO3(s)+H2CO3(aq)的平衡常数为_______。
FeCO3(s)+H2CO3(aq)的平衡常数为_______。
(7)在空气中煅烧FeCO3生成氧化铁的化学方程式为____________。
(8)结合所学化学知识,请你设计在实验室里从上述的硫铁矿烧渣中提取氧化铁的另一种简单方案。
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市高三3月质检理综化学试卷(解析版) 题型:实验题
(13分)某研究性学习小组欲探究Na2CO3溶液与MgCl2溶液反应产生白色沉淀的成分,小组成员做如下实验
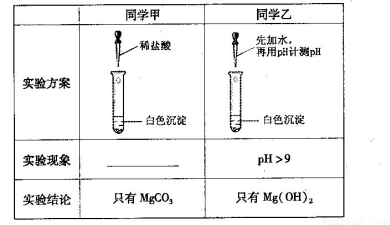
(1)若按所得的结论分析,甲观察到的实验现象是___________________________。
(2)在探究沉淀物成分前,甲、乙都将沉淀物从溶液中分离出来,洗涤并干燥。同学丙认为他们并未将沉淀洗涤干净,请用简单的实验证明丙的观点。
(3)同学丁认为甲结论不合理,理由是Ksp(MgCO3)___Ksp [Mg(OH)2](选填“<”或“>”),所以沉淀物未必是MgCO3。经查阅资料得知:该白色沉淀的组成应为Mgx(OH)y(CO3)z·nH2O。为确定沉
淀物的具体组成,他设计下图装置进行实验(所有夹持装置已省略)。
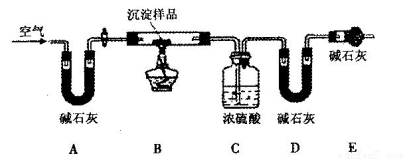
(4)请将丁设计的实验步骤补充完整:
①检查装置气密性;
②先装入药品,并称量相关装置的质量,后连接各装置;
③________________________________________________________;
④停止加热,持续通入空气直至实验结束,再次称量步骤②中相关装置的质量。
(5)装置E中碱石灰的作用是_________________________________________________。
三次实验所得数据如下:(部分数据已换算为相应的物质的量)
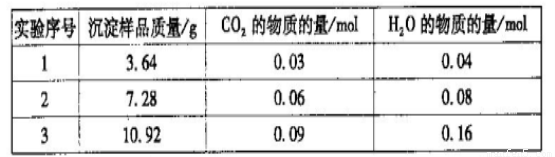 ??
??
(6)分析实验数据可知,第_________组出现误差较大的数据,应舍去。由实验数据计算
得该白色沉淀物的组成为___________(选填序号)。
a.Mg2(OH)2CO3·3H2O?????? b.Mg(OH)2(CO3)2·3H2O
c.Mg4(OH)2(CO3)3·3H2O??? d.Mg5(OH)4(CO3)3·2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com