
科目: 来源:2013-2014学年福建省漳州市七校高三第二次联考化学试卷(解析版) 题型:实验题
碳铵是一种较常使用的化肥,它在常温下易分解。某化学兴趣小组对碳铵的成分存在疑问,进行了如下探究。
【定性实验】检验溶液中的阴、阳离子。
取少量固体放入试管中,加入盐酸,把生成的气体通入澄清石灰水中,有白色沉淀生成。再另取少量碳铵放入试管中,加入浓NaOH溶液,加热,用湿润的红色石蕊试纸检验生成的气体,石蕊试纸变蓝色。
(1)根据实验现象,推测碳铵中所含有阴离子可能是 和 。
(2)据实验现象,碳铵与足量NaOH溶液加热反应的离子方程式可能是 ???????? 。
【定量实验】测定碳铵中C元素和N元素质量比。
该兴趣小组准确称取ag碳铵,加热使之分解,并把产物通入碱石灰中,如下图所示。

(1)碳铵固体应放在 中进行加热。
A.试管 B.蒸发皿 C.烧瓶 D.坩埚
(2)从安全的角度考虑,尾气处理的装置可以选用 。

????????????? A????????? B???????????? C??? D
(3)若灼烧后没有固体残余,称量U形管在实验前后的质量差为bg。由此测得N元素的质量是 g。
(4)为了测定碳铵中碳元素的质量,他们设计的实验方案是将ag碳铵完全溶解于水,加入过量BaCl2,然后测定生成沉淀质量。请你评价该方案是否合理。 (填“合理”“不合理”),理由是 ?????????????????????? ???????????? 。
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市八校高三第三次联考理综化学试卷(解析版) 题型:选择题
下列实验现象与对应结论均正确的是(???? )
选项操作现象结论
A常温下将Cu片放入浓H2SO4中生成刺激性气味气体Cu与浓H2SO4反应生成SO2
BAl2(SO4)3溶液中滴加过量氢氧化钡溶液生成白色沉淀Al(OH)3不溶于氢氧化钡溶液
C向某溶液中加入KSCN溶液,再向溶液中加入新制氯水溶液先不显红色,加入氯水后变红色该溶液中含有Fe2+
D向某溶液中加入CCl4,振荡后静置液体分层,下层呈紫红色该溶液中存在I-
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市八校高三第三次联考理综化学试卷(解析版) 题型:选择题
下列说法正确的是(??? )
A.1L 1mol?L-1的NH4Cl溶液中一定含有NA个NH4+
B.常温常压下,22.4L乙烯中含共价键数为5 NA
C.6.8g熔融的KHSO4中含有0.05 NA个阳离子
D.1mol冰醋酸和lmo1乙醇在浓硫酸加热下反应可生成NA个H2O
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市八校高三第三次联考理综化学试卷(解析版) 题型:选择题
对①乙醇②淀粉③油脂④蛋白质的说法,不正确的是(???? )
A.等质量的②和③在人体内充分消化吸收时,③释放的能量更大
B.①能使④失去生理活性而变性
C.①可由②水解的最终产物反应制得
D.③和④在人体内的最终代谢产物相同
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市八校高三第三次联考理综化学试卷(解析版) 题型:选择题
在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正确的是(??? )
A.含等物质的量的AlO2-、OH-、CO32-的溶液中,逐滴加入盐酸:AlO2-、OH-、CO32-
B.含等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I-、Br-、Fe2+
C.含等物质的量的Ba(OH)2、KOH的溶液中,缓慢通入CO2:KOH、Ba(OH)2、K2CO3、BaCO3
D.含等物质的量的Fe3+、Cu2+、H+的溶液中加入锌粉:Fe3+、Cu2+、H+、Fe2+
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市八校高三第三次联考理综化学试卷(解析版) 题型:选择题
X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6。下列说法正确的是(???? )
A.Y元素最高价氧化物对应的水化物化学式H2YO4
B.原子半径由大到小的顺序为:Z>Y> W
C.X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定
D.X与W形成的两种化合物中,阴、阳离子物质的量之比均为1︰2
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市八校高三第三次联考理综化学试卷(解析版) 题型:选择题
某小组设计电解饱和食盐水的装置如图,通电后两极均有气泡产生,下列叙述正确的是(???? )
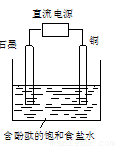
A.铜电极附近观察到黄绿色气体?
B.石墨电极附近溶液呈红色
C.溶液中的Na+向石墨电极移动
D.铜电极上发生还原反应
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市八校高三第三次联考理综化学试卷(解析版) 题型:选择题
一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:
2X(g)+Y(g) Z(g)△H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是(???? )
Z(g)△H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是(???? )
A.以Y浓度变化表示的反应速率为0.0005 mol/(L·s)
B.其他条件不变,将容器体积扩大至20 L,则Z的平衡浓度变为原来的1/2
C.其他条件不变,将容器体积缩小至5L,平衡正向移动,平衡常数增大
D.其他条件不变,升高温度逆反应速率加快,正反应速率减慢
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市八校高三第三次联考理综化学试卷(解析版) 题型:填空题
氮氧化物是大气污染物之一,消除氮氧化物的方法有多种。
(1)利用甲烷催化还原氮氧化物。已知:
①CH4 (g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)?? △H =-574 kJ/mol
②CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g)? △H =-1160 kJ/mol
则CH4 将NO2 还原为N2 的热化学方程式为:??????????? ???????????? 。
 (2)利用NH3催化还原氮氧化物(SCR技术)。该技术是目前应用最广泛的烟气氮氧化物脱除技术。 反应的化学方程式为:
(2)利用NH3催化还原氮氧化物(SCR技术)。该技术是目前应用最广泛的烟气氮氧化物脱除技术。 反应的化学方程式为: 为提高氮氧化物的转化率可采取的措施是???????? ????????????????????????? (写出1条即可)。
为提高氮氧化物的转化率可采取的措施是???????? ????????????????????????? (写出1条即可)。
(3)利用ClO2 氧化氮氧化物。其转化流程如下:? NO NO2
NO2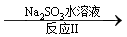 N2。已知反应Ⅰ的化学方程式为2NO+ ClO2 + H2O =NO2 + HNO3 + HCl,则反应Ⅱ的化学方程式是???????? ????? ;若生成11.2 L N2(标准状况),则消耗ClO2 ??????? g 。
N2。已知反应Ⅰ的化学方程式为2NO+ ClO2 + H2O =NO2 + HNO3 + HCl,则反应Ⅱ的化学方程式是???????? ????? ;若生成11.2 L N2(标准状况),则消耗ClO2 ??????? g 。
(4)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g) N2 (g)+CO2 (g)△H.某研究小组向某密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2 (g)+CO2 (g)△H.某研究小组向某密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度/mol?L-1/ 时间/min | NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
50 | 0.032 | 0.034 | 0.017 |
①T1℃时,该反应的平衡常数K= ????????? (保留两位小数).②30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是 ????????????? .③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则该反应的△H ?? 0(填“>”、“=”或“<”).
查看答案和解析>>
科目: 来源:2013-2014学年福建省漳州市八校高三第三次联考理综化学试卷(解析版) 题型:填空题
某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用工艺设计如下:
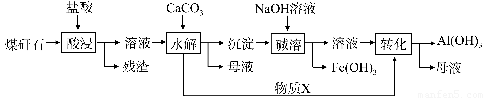
(1)“酸浸”过程中主要反应的离子方程式为__________?? 、____________。
(2)“酸浸”时铝浸出率的影响因素可能有_____? ________、_____? ______。(写出两个)
(3)物质X的化学式为___________。“碱溶”时反应的主要离子方程式为:Fe3++3OH- = Fe(OH)3↓;??????????????????? ????????????????? 。
(4)已知Fe3+开始沉淀和沉淀完全的pH分别为2.1和3.2,Al3+开始沉淀和沉淀完全的pH分别为4.1和5.4为了获得产品Al(OH)3,从煤矸石的盐酸浸取液开始,若只用CaCO3一种试剂,后续操作过程是?????????????????????? 。
(5)以煤矸石为原料还可以开发其他产品,例如在煤矸石的盐酸浸取液除铁后,常温下向AlCl3溶液中不断通入HCl气体,可析出大量AlCl3·6H2O晶体,结合化学平衡移动原理解释析出晶体的原因:???????????????????????????????????????? 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com