
科目: 来源:2013-2014学年湖北省孝感市高三第二次统考理综化学试卷(解析版) 题型:选择题
分子式为C5H10N2O3的二肽在酸性条件下可水解为氨基酸(不考虑H2N-COOH和立体异构),这些氨基酸重新组合可形成的二肽共有
A.3种????????? B.6种?????????? C.9种?????????? D.12种
查看答案和解析>>
科目: 来源:2013-2014学年湖北省孝感市高三第二次统考理综化学试卷(解析版) 题型:选择题
气体的自动化检测中常常应用原电池原理的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。则下列说法中正确的是

待测气体 | 部分电极反应产物 |
NO2 | NO |
Cl2 | HCl |
CO | CO2 |
H2S | H2SO4 |
A.上述气体检测时,敏感电极均作电池正极
B.检测Cl2气体时,敏感电极的电极反应为:Cl2 + 2e-= 2Cl-
C.检测H2S气体时,对电极充入空气,对电极上的电极反应式为O2 + 2H2O+ 4e- = 4OH-
D.检测H2S和CO体积分数相同的两份空气样本时,传感器上产生的电流大小相同
查看答案和解析>>
科目: 来源:2013-2014学年湖北省孝感市高三第二次统考理综化学试卷(解析版) 题型:实验题
硫酸亚铁是重要的亚铁盐,在农业上用作农药,主要治小麦黑穗病,还可以用作除草剂;在工业上用于染色、制造蓝黑墨水和木材防腐等。
(1)新制的绿矾(FeSO4·7H2O)是浅绿色的,但在空气中极易变成黄色或铁锈色的碱式硫酸铁[Fe(OH)SO4],写出该反应的化学方程式:??????????????????????????????????????????????? 。
(2)已知FeSO4在不同条件下分解得到产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2;
SO3熔点是16.8℃,沸点是44.8℃。
某研究性学习小组拟用下列装置进行实验探究“在加热条件下FeSO4的分解产物”。
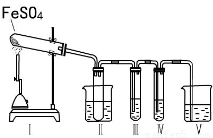
上述装置Ⅲ和Ⅳ用来检验气体产物。试回答下列问题:
①Ⅱ装置烧杯中水的温度应控制在????? (选填“0℃、25℃、50℃”),装置Ⅱ的作用是??????????? 。
②装置Ⅲ中的试剂可以是??????? (选填序号,下同),现象是????????????? ,则证明气体产物中含有SO2; 装置Ⅳ中的试剂可以是????????? 。
A. 2 mol/LNa2CO3溶液
B. 品红溶液
C. 0.5 mol/L BaCl2溶液?
D. 0.5 mol/LBa(NO3)2
E. 0.01 mol/L KMnO4溶液
F. 淀粉碘化钾溶液
③装置V中试剂为NaOH溶液,发生反应的离子方程式为??????????????????????????? 。
④为了检验固体产物成分,取反应后的固体于试管中,加稀硫酸溶解,将所得溶液分成两份,进行如
下实验:
操作步骤 | 预期实验现象 | 预期实验结论 |
向其中一份溶液中加入??? ?????????? 。 | ? ????????????????????????? | ????? 固体中含有Fe2O3 |
向另一份溶液中滴加2滴黄色K3[Fe(CN)6]溶液。 | ???????? 产生蓝色沉淀 | ?????????????????????????? |
⑤若用22.8 g FeSO4固体做实验,完全分解后,得到11.2 g固体,其中Fe2O3的质量分数=??????????
(精确到0.1%)
查看答案和解析>>
科目: 来源:2013-2014学年湖北省孝感市高三第二次统考理综化学试卷(解析版) 题型:填空题
丙烷在燃烧时能放出大量的热,它也是液化石油气的主要成分,作为能源应用于人们的日常生产和生活。已知:
①2C3H8(g) +7O2(g) = 6CO(g)+8H2O(g)?? △H = -2389.8 kJ/mol
②2CO(g) + O2(g) = 2CO2(g)????????????? △H = -566 kJ/mol
③H2O(l) = H2O(g)???? △H = + 44.0 kJ/mol
(1)写出C3H8燃烧时燃烧热的热化学方程式???????????????????????????????????????????? 。
(2)C3H8在不足量的氧气里燃烧,生成CO、CO2、H2O(g),将所有的产物通入一个体积固定的密闭
容器中,在一定条件下发生如下可逆反应: CO(g) +? H2O(g) CO2(g) +? H2(g)
CO2(g) +? H2(g)
该反应的平衡常数与温度的关系如下表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
保持温度为800℃,在甲、乙两个恒容密闭容器中,起始时按照下表数据进行投料,充分反应直至达到平衡。
| H2O | CO | CO2 | H2 |
甲 (质量/g) | 1.8 | 8.4 | a | 1 |
乙 (质量/g) | 1.8 | 2.8 | 0 | 0 |
①起始时,要使甲容器中反应向正反应方向进行,则a的取值范围是????????????????? ;达到平衡
时,乙容器中CO的转化率为???????? 。
②如图表示上述甲容器中反应在t1时刻达到平衡,在t2时刻因改变某一个条件而发生变化的情况。则t2时刻改变的条件可能是???????????????????????????? 、??????????????????? (答两个要点即可)。

(3)CO2可用NaOH溶液吸收得到Na2CO3或NaHCO3。
① Na2CO3溶液中离子浓度由大到小的顺序为 ?????????? ??? ;
② 已知25℃时,H2CO3的电离平衡常数K1 = 4.4×10-7 mol/L、K2 = 4.7×10-11 mol/L,当Na2CO3溶液的pH为11时, 溶液中c(HCO3-)∶c(CO32-) = ?????????? 。
③ 0.1 mol/L Na2CO3溶液中c(OH-) - c(H+ ) = ?????????????????????? [用含c(HCO3-)、c(H2CO3)的符号表示]。
查看答案和解析>>
科目: 来源:2013-2014学年湖北省孝感市高三第二次统考理综化学试卷(解析版) 题型:填空题
MnO2、KMnO4等是中学化学中的常用试剂。请回答下列问题:
(1)MnO2在H2O2分解反应中作催化剂。若将MnO2加入酸化的H2O2溶液中,MnO2 溶解产生Mn2+,反应的离子方程式是??????????????????????????????????????????????? 。
(2)用MnO2制KMnO4的工艺流程如图
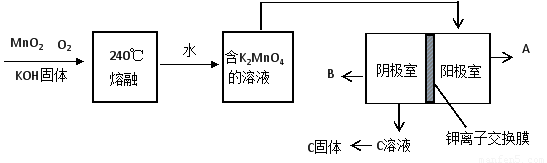
电解池中两极材料均为碳棒,在水或酸性溶液中K2MnO4发生歧化而变成MnO2和KMnO4。
①写出240℃熔融时发生反应的化学方程式????????????????????????????????????? ,投料时必须满足n(KOH):n(MnO2) ?????????? 。
②阳极的电极反应为??????????????????????????????????? 。
③B物质是????????? (写化学式,下同),可以循环使用的物质是???????????????????? 。
④钾离子交换膜的一种材料是聚丙烯酸钾(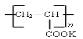 ),聚丙烯酸钾单体的结构简式为??????????? 。
),聚丙烯酸钾单体的结构简式为??????????? 。
⑤上述制得的KMnO4产品0.165 g,恰好与0.335 g经硫酸酸化的Na2C2O4反应完全,该KMnO4的
纯度是??????????? (精确到0.1%)。
查看答案和解析>>
科目: 来源:2013-2014学年湖北省孝感市高三第二次统考理综化学试卷(解析版) 题型:填空题
世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效“绿色”消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时要避免光照、震动或加热。实验室以电解法制备ClO2的流程如下:请回答下列问题。

(1)ClO2中所有原子?????? (填“是”或“不是”)都满足8电子结构。上图所示电解法制得的产物中杂质气体B能使石蕊试液显蓝色,除去杂质气体可选用?????? 。
A.饱和食盐水????? B.碱石灰??????? C.浓硫酸??????? D.蒸馏水
(2)稳定性二氧化氯是为推广二氧化氯而开发的新型产品,下列说法正确的是????? 。
A.二氧化氯可广泛用于工业和饮用水处理
B.应用在食品工业中能有效地延长食品贮藏期
C.稳定性二氧化氯的出现大大增加了二氧化氯的使用范围
D.在工作区和成品储藏室内,要有通风装置和监测及警报装置
(3)欧洲国家主要采用氯酸钠氧化浓盐酸制备,化学反应方程式为??????????????????????????? ,此法缺点主要是产率低、产品难以分离,还可能污染环境。
(4)我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式是????????????????????????? ,此法相比欧洲方法的优点是????????????????????????? 。
(5)科学家最近又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学反应方程式为????????????????????????????????????????????????????? ,此法提高了生产及储存、运输的安全性,原因是??????????????????????????????????????????????????? 。
查看答案和解析>>
科目: 来源:2013-2014学年湖北省孝感市高三第二次统考理综化学试卷(解析版) 题型:填空题
Q、R、X、Y、Z为周期表中原子序数依次递增的前四周期元素。已知:
①Q为元素周期表中原子半径最小的元素;
②R的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;
③Y的基态原子的核外成对电子数是未成对电子数的3倍;
④Z有“生物金属”之称,Z4+离子和氩原子的核外电子排布相同。
请回答下列问题(答题时,Q、R、X、Y、Z用所对应的元素符号表示):
(1)Q、R、Y三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,化合物M的空间构型为???????????? ,其中心原子采取??????? 杂化;Q、R两种元素组成的原子个数比为1:1的化合物N是中学化学中常见的有机溶剂,化合物N在固态时的晶体类型为?????????????? 。
(2)R、X、Y三种元素的第一电离能由小到大的顺序为?????????????????????? 。
(3)由上述一种或多种元素组成的与RY2互为等电子体的分子为????????? (写分子式)。
(4)由R、X、Y三种元素组成的RXY-离子在酸性条件下可与NaClO溶液反应,生成X2、RY2等物
质,该反应的离子方程式为?????????????????????????????????? 。
(5)Z原子基态时的外围电子排布式为???????????????????? ;已知Z的一种含氧酸钡盐的密度为ρ g.cm-3,其晶胞的结构如图所示,则晶?? 体中氧原子与钡原子的最近距离为?????????? cm。(只要求列算式,? 不必计算出数值。阿伏伽德罗常数为NA)

查看答案和解析>>
科目: 来源:2013-2014学年湖北省孝感市高三第二次统考理综化学试卷(解析版) 题型:填空题
HPE是合成苯氧基丙酸类除草剂的重要中间体,其合成路线如下:

已知:①? 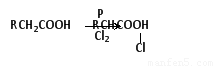 ②
②
据此回答下列问题:
(1)B中含有的官能团名称为???????????? ,D的结构简式为?????????? 。
(2)C + E F的反应类型为?????????? 。
F的反应类型为?????????? 。
(3)M的核磁共振氢谱中各吸收峰的面积之比为????????????? 。
(4)写出G + M HPE的化学方程式????????????????????????????????????????????????? 。
HPE的化学方程式????????????????????????????????????????????????? 。
(5)X是G的同分异构体,其中满足以下条件的X共有?????? 种,写出其中一种X的结构简式 ???????????????????????????????????????? 。
A.苯环上有3个取代基且苯环上的一氯取代物有两种
B.遇FeCl3溶液发生颜色反应
C.X不能与NaHCO3反应产生CO2
D.1 mol X最多能和3 mol NaOH反应
查看答案和解析>>
科目: 来源:2013-2014学年湖北省武汉市新洲区高三上学期期末目标检测理综化学试卷(解析版) 题型:选择题
下列说法均摘自学生的作业本,你认为无科学性错误的是
A.煤的气化、液化都是化学变化,可为人类提供清洁高效的燃料
B.氯化氢、氯气、二氧化氮、生石灰溶于水都有化学键被破坏的变化,都属于化学变化
C.苯酚、纯碱、胆矾和OF2分别属于酸、碱、盐和氧化物
D.二氧化碳、氨气、氯气都是非电解质
查看答案和解析>>
科目: 来源:2013-2014学年湖北省武汉市新洲区高三上学期期末目标检测理综化学试卷(解析版) 题型:选择题
研究人员最近发现了一种“水”电池,这种电池能利用淡水和海水之间含盐量的差别进行发电,在海水中电池总反应可表示为5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是
A.Ag发生还原反应
B.正极反应式:5MnO2+2e- =Mn5O102-
C.每生成1mol AgCl转移2mol电子
D.Cl—不断 向“水”电池的正极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com