
科目: 来源:2013-2014学年江苏省南通市高三第二次调研化学试卷(解析版) 题型:填空题
金属表面处理、皮革鞣制、印染等都可能造成铬污染。六价铬比三价铬毒性高,更易被人体吸收且在体内蓄积。
⑴工业上处理酸性含Cr2O72-废水的方法如下:
①向含Cr2O72-的酸性废水中加入FeSO4溶液,使Cr2O72-全部转化为Cr3+。写出该反应的离子方程式:??? 。
②调节溶液的pH,使Cr3+完全沉淀。实验室粗略测定溶液pH的方法为??? ;25℃,若调节溶液的pH=8,则溶液中残余Cr3+的物质的量浓度为??? mol/L。(已知25℃时,Ksp[Cr(OH)3]=6.3×10-31)
⑵铬元素总浓度的测定:准确移取25.00mL含Cr2O72-和Cr3+的酸性废水,向其中加入足量的(NH4)2S2O8溶液将Cr3+氧化成Cr2O72-,煮沸除去过量的(NH4)2S2O8;向上述溶液中加入过量的KI溶液,充分反应后,以淀粉为指示剂,向其中滴加0.015mol/L的Na2S2O3标准溶液,终点时消耗Na2S2O3溶液20.00mL。
计算废水中铬元素总浓度(单位:mg·L-1,写出计算过程)。
已知测定过程中发生的反应如下:
①2Cr3++3S2O82-+7H2O =Cr2O72-+6SO42-+14H+
②Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O
③I2+2S2O32-=2I-+S4O62-
查看答案和解析>>
科目: 来源:2013-2014学年江苏省南通市高三第二次调研化学试卷(解析版) 题型:填空题
三氯化铁是合成草酸铁的重要原料。
⑴利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)3·5H2O]的实验流程如下图所示:
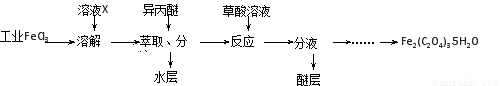
①为抑制FeCl3水解,溶液X为??? 。
②上述流程中FeCl3能被异丙醚萃取,其原因是??? ;检验萃取、分液后所得水层中是否含有Fe3+的方法是??? 。
③所得Fe2(C2O4)3·5H2O需用冰水洗涤,其目的是??? 。
④为测定所得草酸铁晶体的纯度,实验室称取a g样品,加硫酸酸化,用KMnO4标准溶液滴定生成的H2C2O4,KMnO4标准溶液应置于如图所示仪器????? (填“甲”或“乙”)中。下列情况会造成实验测得Fe2(C2O4)3·5H2O含量偏低的是????? 。

a.盛放KMnO4的滴定管水洗后未用标准液润洗
b.滴定管滴定前尖嘴部分有气泡,滴定后消失
c.滴定前仰视读数,滴定后俯视读数
⑵某研究性学习小组欲从蚀刻镀铜电路板所得废液(溶质为FeCl2、CuCl2、FeCl3)出发,制备单质铜和无水FeCl3,再由FeCl3合成Fe2(C2O4)3·5H2O。请补充完整由蚀刻废液制备单质铜和无水FeCl3的实验步骤(可选用的试剂:铁粉、盐酸、NaOH溶液和H2O2溶液):向废液中加入足量铁粉,充分反应后过滤;????? ;调节溶液pH,将溶液蒸发浓缩、冷却结晶、过滤、洗涤干燥得FeCl3·6H2O;????? ,得到无水FeCl3。
查看答案和解析>>
科目: 来源:2013-2014学年江苏省南通市高三第二次调研化学试卷(解析版) 题型:填空题
催化剂是化工技术的核心,绝大多数的化工生产均需采用催化工艺。
⑴人们常用催化剂来选择反应进行的方向。如图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去]。
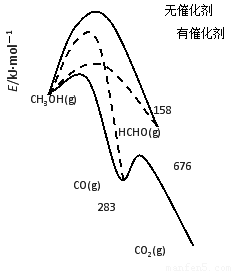
①在有催化剂作用下,CH3OH与O2反应主要生成????? (填“CO、CO2或HCHO”)。
②2HCHO(g)+O2(g)=2CO(g)+2H2O(g)? △H=????? 。
③在稀硫酸催化下,HCHO可以通过反应生成分子式为C3H6O3的环状三聚甲醛分子,其分子中同种原子的化学环境均相同。写出三聚甲醛的结构简式:????? 。
④甲醇制取甲醛可用Ag作催化剂,含有AgCl会影响Ag催化剂的活性,用氨水可以溶解除去其中的AgCl,写出该反应的离子方程式:????? 。
⑵一种以铜作催化剂脱硫有如下两个过程:
①在铜的作用下完成工业尾气中SO2的部分催化氧化,所发生反应为:
2SO2+2n Cu+(n+1)O2+(2-2 n) H2O=2n CuSO4+(2-2n) H2SO4
从环境保护的角度看,催化脱硫的意义为????? ;每吸收标准状况下11.2L SO2,被SO2还原的O2的质量为????? g。
②利用下图所示电化学装置吸收另一部分SO2,并完成Cu的再生。写出装置内所发生反应的离子方程式????? 。

查看答案和解析>>
科目: 来源:2013-2014学年江苏省南通市高三第二次调研化学试卷(解析版) 题型:填空题
元素X的基态原子中的电子共有7个能级,且最外层电子数为1,X原子的内层轨道全部排满电子。在气体分析中,常用XCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:
2XCl+2CO+2H2O=X2Cl2·2CO·2H2O
⑴X基态原子的电子排布式为????? 。
⑵C、H、O三种原子的电负性由大到小的顺序为????? 。
⑶X2Cl2·2CO·2H2O是一种配合物,其结构如图所示:

①与CO为互为等电子体的分子是????? 。
②该配合物中氯原子的杂化方式为????? 。
③在X2Cl2·2CO·2H2O中,每个X原子能与其他原子形成3个配位键,在图中用“→”标出相应的配位键????? 。
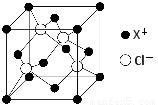
⑷XCl的晶胞如图所示,距离每个X+最近的Cl—的个数为????? 。
查看答案和解析>>
科目: 来源:2013-2014学年江苏省南通市高三第二次调研化学试卷(解析版) 题型:实验题
2-苯基-2-丁醇是重要的有机合成中间体,以溴苯为原料合成该中间体的反应原理如下:

【实验装置】
 ??????
?????? 
装置Ⅰ?????????????????????????? 装置Ⅱ
【实验步骤】
步骤1:将镁条置于装置Ⅰ的三颈烧瓶中,加入100 mL乙醚(ρ=0.71g·cm-3),在冷却条件下缓缓滴入溴苯,微热并加入一小块碘引发反应①。
步骤2:滴加14.2 mL丁酮和30 mL乙醚混合物,发生反应②;滴加入20%的NH4Cl水溶液,发生反应③。
步骤3:分出油层,用水洗涤至中性,用无水CaCl2干燥。
步骤4:用装置Ⅱ先蒸出乙醚,再蒸馏出产品。
⑴步骤1中加入碘的作用是????? 。
⑵装置Ⅰ中滴加液体所用的仪器的名称是????? ,反应②需将三颈烧瓶置于冰水中,且逐滴加入丁酮和乙醚,其目的是????? 。
⑶步骤三中分离出油层的具体实验操作是????? 。
⑷装置Ⅱ采用的是减压蒸馏,实验时需将吸滤瓶需连接????? ;采用这种蒸馏方式的原因是????? 。
查看答案和解析>>
科目: 来源:2013-2014学年江苏省南通市高三第一次调研测试化学试卷(解析版) 题型:选择题
2013年11月江苏在大部分地市推广使用含硫量大幅减少的苏V汽油。下列有关汽油的说法正确的是
A.汽油属于可再生能源?????????????????? B.将原油通过萃取、分液可获得汽油
C.使用苏V汽油可降低酸雨发生率??????? D.苏V汽油只含C、H、O三种元素
查看答案和解析>>
科目: 来源:2013-2014学年江苏省南通市高三第一次调研测试化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.水的电子式: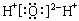
B.中子数为20的氯原子:
C.聚丙烯的结构简式: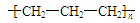
D.钠原子的结构示意图: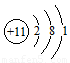
查看答案和解析>>
科目: 来源:2013-2014学年江苏省南通市高三第一次调研测试化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.0.1 mol·L-1盐酸的澄清透明溶液:Fe3+、K+、SO42- 、Br-
B.含有NaNO3的溶液:H+、Fe2+、SO42- 、Cl-
C.能使石蕊变红的溶液:Cu2+、Na+、AlO2-、Cl-
D.由水电离出的c(H+)·c(OH-)=10-22的溶液:Na+、Ca2+、HCO3- 、NO3-
查看答案和解析>>
科目: 来源:2013-2014学年江苏省南通市高三第一次调研测试化学试卷(解析版) 题型:选择题
下列有关物质性质或应用的说法正确的是
A.医疗上,常用碳酸钠治疗胃酸过多
B.在海轮外壳上安装锌块以减缓船体腐蚀
C.液氨汽化放出大量的热,可用作制冷剂
D.明矾具有强氧化性,常用于自来水的杀菌消毒
查看答案和解析>>
科目: 来源:2013-2014学年江苏省南通市高三第一次调研测试化学试卷(解析版) 题型:选择题
粗略测定草木灰中碳酸钾的含量并检验钾元素的存在,需经过称量、溶解、过滤、蒸发、焰色反应等操作。下列图示对应的操作不规范的是
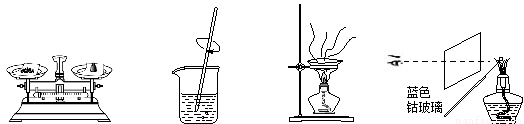
A.称量???? ???????? B.溶解????? ???? C.蒸发??? ???? D.焰色反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com