
科目: 来源:2013-2014学年广东省韶关市高三调研测试理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列叙述正确的是
A.1 L 1 mol/L氯化铜溶液中含有NA个Cu2+
B.标准状况下,22.4 L O2参加任何化学反应转移的电子数都是4NA
C.1 mol Zn与足量稀HNO3反应,转移2NA个电子??????
D.1 mol H3O+所含电子数为8NA
查看答案和解析>>
科目: 来源:2013-2014学年广东省韶关市高三调研测试理综化学试卷(解析版) 题型:选择题
下列有关离子组的评价及相关离子方程式均正确的是:
选项????????????? 离子组????????????? 评价及离子方程式
A????????????? H+、Fe2+、NO3-、Cl-????????????? 不能大量共存于同一溶液中,因为发生反应:Fe2+ + 2H+ = Fe3+ + H2↑
B????????????? Na+、K+、HCO3-、OH-????????????? 不能大量共存于同一溶液中,因为发生反应:HCO3- + OH- = H2O + CO2↑
C????????????? Ca2+、NH4+、CO32-、Cl-????????????? 能大量共存于同一溶液中
D????????????? Na+、 NH4+、SO42-、Cl-????????????? 能大量共存于同一溶液中
查看答案和解析>>
科目: 来源:2013-2014学年广东省韶关市高三调研测试理综化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.向明矾溶液中加入过量NaOH溶液会产生大量白色沉淀
B.Na2O2用作呼吸面具的供氧剂
C.氯水中通入SO2后溶液的酸性减弱
D.N2与O2在放电条件下直接化合生成NO2
查看答案和解析>>
科目: 来源:2013-2014学年广东省韶关市高三调研测试理综化学试卷(解析版) 题型:选择题
四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法不正确的是
|
| Y | Z |
M | X |
|
|
A.原子半径Z<M
B.Y的最高价氧化物对应水化物的酸性比X的弱
C.非金属性:X<Z
D.M元素最高价氧化物对应水化物具有两性
查看答案和解析>>
科目: 来源:2013-2014学年广东省韶关市高三调研测试理综化学试卷(解析版) 题型:选择题
对处于平衡状态的反应2A(g)+B(g) 2C(g)??? △H<0,下列叙述正确的是
2C(g)??? △H<0,下列叙述正确的是
A.增大A浓度的瞬间,V正 增大,V逆不变
B.升高温度,V正 减小,V逆增大
C.增大压强. V正 增大,V逆 减小
D.加入催化剂,V正、V逆 都增大
查看答案和解析>>
科目: 来源:2013-2014学年广东省韶关市高三调研测试理综化学试卷(解析版) 题型:选择题
常温下,浓度均为0.1mol/L的三种溶液:①CH3COOH溶液②NaOH溶液③CH3COONa溶液,下列说法中正确的是(忽略混合前后溶液体积变化)
A.溶液的pH值:②>③>①
B.水电离出的c(OH-):③>①=②
C.①和③等体积混合后的溶液:c(CH3COOH)+ c(CH3COO-)=0.1mol/L
D.②和③等体积混合后的溶液:c(Na+)=c(CH3COOH)+c(CH3COO-)
查看答案和解析>>
科目: 来源:2013-2014学年广东省韶关市高三调研测试理综化学试卷(解析版) 题型:选择题
下列实验现象、解释与结论均正确的是
编号????????????? 实验操作????????????? 实验现象????????????? 解释与结论
A????????????? 铜与浓硝酸反应,生成气体用湿润KI-淀粉试纸检验????????????? 试纸变蓝????????????? NO2为酸性气体
B????????????? 向某溶液中加入稀盐酸酸化的BaCl2溶液????????????? 有白色沉淀产生????????????? 该沉淀可能是BaSO4,该溶液中可能含有SO42-
C????????????? 向甲苯中滴入少量浓溴水,振荡,静置????????????? 溶液分层,上层呈橙红色,下层几乎无色????????????? 甲苯和溴水发生取代反应,使溴水褪色
D????????????? 在稀AgNO3溶液中先加入过量0.1mol/L NaCl溶液,再加入少量0.1mol/L NaI溶液 ????????????? 先产生白色沉淀,后出现黄色沉淀????????????? 说明Ksp(AgCl)>Ksp(AgI)
查看答案和解析>>
科目: 来源:2013-2014学年广东省韶关市高三调研测试理综化学试卷(解析版) 题型:填空题
工业上用甲苯生产对羟基苯甲酸乙酯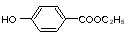 ,生产过程如下图:
,生产过程如下图:

(1)对羟基苯甲酸乙酯的分子式为??????? ;1mol 该物质与NaOH溶液完全反应,最多消耗___? ___molNaOH。
(2)化合物A中的官能团名称是_________,反应④的反应类型属_____? ___。
(3)反应①的化学方程式________ _______。
(4)在合成线路中,设计第③和⑥这两步反应的目的是__________。
(5)有机物C(分子构型为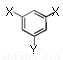 ,-X、-Y为取代基)是对羟基苯甲酸乙酯的同分异构体且能发生银镜反应,则-X的结构简式可能是????????? 、????????? 。
,-X、-Y为取代基)是对羟基苯甲酸乙酯的同分异构体且能发生银镜反应,则-X的结构简式可能是????????? 、????????? 。
查看答案和解析>>
科目: 来源:2013-2014学年广东省韶关市高三调研测试理综化学试卷(解析版) 题型:填空题
(1)已知: C(s)+O2(g)=CO2(g)???????? ΔH1=-393.5 kJ/mol
C(s)+H2O(g)=CO(g)+H2(g)? ΔH2=+131.3 kJ/mol
则反应CO(g)+H2(g) +O2(g)= H2O(g)+CO2(g),ΔH= ____? ___kJ/mol。
(2)在一恒容的密闭容器中,由CO和H2合成甲醇:CO(g)+2H2(g) CH3OH(g)? ΔH
CH3OH(g)? ΔH
①下列情形不能说明该反应已达到平衡状态的是_______(填序号)。
A.每消耗1 mol CO的同时生成2molH2
B.混合气体总物质的量不变
C.生成CH3OH的速率与消耗CO的速率相等
D.CH3OH、CO、H2的浓度都不再发生变化
②CO的平衡转化率(α)与温度、压强的关系如图所示。A、B两点的平衡常数K(A)_______K(B)(填“>”、“=”或“<”,下同);由图判断ΔH _____0。
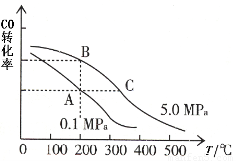
③某温度下,将2.0 mol CO和6.0 molH2充入2 L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.25 mol/L,则CO的转化率=?????????? ,此温度下的平衡常数K=????????????? (保留二位有效数字)。
(3)工作温度650℃的熔融盐燃料电池,用煤炭气(CO、H2)作负极反应物,空气与CO2的混合气体为正极反应物,催化剂镍作电极,用一定比例的Li2CO3和Na2CO3低熔点混合物作电解质。负极的电极反应式为:CO+H2-4e-+2CO32-=3CO2+H2O;则该电池的正极反应式为???????????????????????? 。
查看答案和解析>>
科目: 来源:2013-2014学年广东省韶关市高三调研测试理综化学试卷(解析版) 题型:填空题
工业上生产高氯酸(沸点:90°C)时还同时生产了亚氯酸钠,其工艺流程如下:
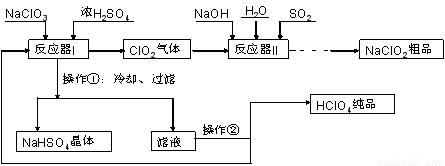
(1)实验室进行过滤操作的常用玻璃仪器有???????????? 。
(2)反应器I中的温度最佳为???????? (填序号);操作②的名称为????????? 。
A. 0°C ;????????? B. 20°C ;??????? C. 80°C ;????????? D. 120°C??
(3)反应器II中发生反应的离子方程式为?????????????? 。
(4)加快反应器II中反应速率的措施有?????????????? (写出一种措施即可)等。从反应器II中获得NaClO2?? 粗品的实验操作依次是???????? (填序号,下同),进一步提纯的操作名称为???????? 。
A.过滤? B.重结晶? C.蒸馏? D.蒸发浓缩? E.蒸干灼烧? F.冷却结晶? G.萃取分液
(5)上述流程中可循环使用的物质为???????? ,副产品除NaClO2、NaHSO4外还有???????? (填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com