
科目: 来源:2013-2014学年广东省广州市毕业班综合测试一(一模)理综化学试卷(解析版) 题型:填空题
硝酸铈铵[(NH4)2Ce(NO3)6]广泛应用于电子、催化工业,其合成路线如下:

(1)已知(NH4)2Ce(NO3)6受热易分解,某科研小组认为反应原理如下,请补充完整:(NH4)2Ce(NO3)6 CeO2·8OH + 8_____↑;CeO2·8OH
CeO2·8OH + 8_____↑;CeO2·8OH CeO2+ 4H2O↑+2O2↑。
CeO2+ 4H2O↑+2O2↑。
在空气中加热(NH4)2Ce(NO3)6,除固体颜色有变化外,还可观察到的现象是_________。
(2)步骤Ⅰ中,将Ce(NO3)3·6H2O配成溶液,保持pH到4~5,缓慢加入H2O2溶液搅拌混合均匀,再加入氨水调节溶液pH,得到Ce(OH)4沉淀。该过程中参加反应的氧化剂与还原剂物质的量之比为___________。
(3)298K时,Ksp[Ce(OH)4]=1×10—29。Ce(OH)4的溶度积表达式为Ksp=___________。
为了使溶液中Ce4+沉淀完全,即残留在溶液中的c(Ce4+)小于1×10—5mol·L-1,需调节pH为______以上。
(4)为了研究步骤Ⅲ的工艺条件,科研小组测定了(NH4)2Ce(NO3)6在不同温度、不同浓度硝酸中的溶解度,结果如图。从图中可得出三条主要规律:
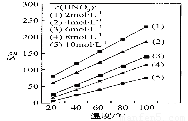
① (NH4)2Ce(NO3)6在硝酸中的溶解度随温度升高而增大;
② _____________________________________________;
③ _____________________________________________。
查看答案和解析>>
科目: 来源:2013-2014学年广东省广州市毕业班综合测试一(一模)理综化学试卷(解析版) 题型:填空题
某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用工艺设计如下:
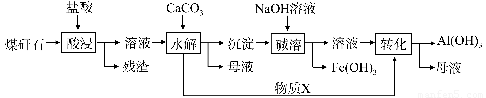
(1)“酸浸”过程中主要反应的离子方程式为_____________、_________________。
(2)“酸浸”时铝浸出率的影响因素可能有_____________、___________。(写出两个)
(3)物质X的化学式为___________。“碱溶”时反应的离子方程式为____________。
(4)已知Fe3+开始沉淀和沉淀完全的pH分别为2.1和3.2,Al3+开始沉淀和沉淀完全的pH分别为4.1和5.4。为了获得产品Al(OH) 3,从煤矸石的盐酸浸取液开始,若只用CaCO3一种试剂,后续操作过程是____________________。
(5)以煤矸石为原料还可以开发其他产品,例如在煤矸石的盐酸浸取液除铁后,常温下向AlCl3溶液中不断通入HCl气体,可析出大量AlCl3·6H2O晶体,结合化学平衡移动原理解释析出晶体的原因:_______________________。
查看答案和解析>>
科目: 来源:2013-2014学年广东省广州市毕业班综合测试一(一模)理综化学试卷(解析版) 题型:实验题
硫化碱法是工业上制备Na2S2O3的方法之一,反应原理为:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2?? (该反应△H>0)
某研究小组在实验室用硫化碱法制备Na2S2O3·5H2O流程如下。
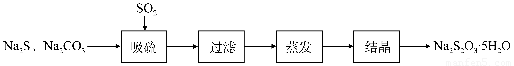
(1)吸硫装置如图所示。
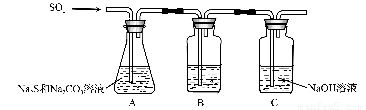
①装置B的作用是检验装置A中SO2的吸收效率,B中试剂是 ???????? ,表明SO2吸收效率低的实验现象是B中溶液 ????????? 。
②为了使SO2尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是 ??????????????? 、?????????????? 。(写出两条)
(2)假设本实验所用的Na2CO3含少量NaCl、NaOH,设计实验方案进行检验。(室温时CaCO3饱和溶液的pH=10.2)
限选试剂及仪器:稀硝酸、AgNO3溶液、CaCl2溶液、Ca(NO3)2溶液、酚酞溶液、蒸馏水、pH计、烧杯、试管、滴管
序号 | 实验操作 | 预期现象 | 结论 |
① | 取少量样品于试管中,加入适量蒸馏水,充分振荡溶解,___________________。 | _______________ | 样品含NaCl |
② | 另取少量样品于烧杯中,加入适量蒸馏水,充分搅拌溶解,___________________。 | _______________ | 样品含NaOH |
(3)Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:准确称取a g KIO3(化学式量:214)固体配成溶液,加入过量KI固体和H2SO4溶液,滴加指示剂,用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液的体积为V mL。则c(Na2S2O3)=_________mol·L-1。(只列出算式,不作运算)
已知:IO3-+5I-+6H+== 3I2+3H2O???? 2S2O32-+I2==S4O62-+2I-
查看答案和解析>>
科目: 来源:2013-2014学年广东省等高三下学期2月联考理综化学试卷(解析版) 题型:选择题
化学与能源、环保、资源利用、食品安全等密切相关,下列说法正确的是(??? )
A.石油液化气、汽油和石蜡的主要成分都是碳氢化合物
B.核电站泄漏的放射性碘-131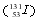 、铯-137
、铯-137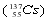 互称同位素,可使蛋白质变性
互称同位素,可使蛋白质变性
C.某雨水样品放置一段时间后pH由4.68变为4.28,是因为水中溶解的CO2增多
D.“地沟油”、“塑化剂”(邻苯二甲酸酯类物质)均属于高分子化合物,都对健康有害。
查看答案和解析>>
科目: 来源:2013-2014学年广东省等高三下学期2月联考理综化学试卷(解析版) 题型:选择题
以NA表示阿伏加德罗常数的值,下列说法正确的是(??? )
A.0.1mol Fe与足量盐酸反应,转移的电子数为0.3NA
B.28gCO中所含的原子数为2NA????
C.1L 0.1mol/LNa2CO3溶液中,含有CO32— 数为0.1NA
D.22.4LH2的分子数为NA
查看答案和解析>>
科目: 来源:2013-2014学年广东省等高三下学期2月联考理综化学试卷(解析版) 题型:选择题
下列离子反应方程式正确的是(??? )
A.氨水吸收过量的SO2:OH-+SO2=HSO3-
B.FeSO4溶液被氧气氧化:4Fe2++O2+2H2O=4Fe3++4OH-
C.NaAlO2溶液中加入过量稀硫酸:AlO2-+H++H2O=Al(OH)3↓
D.Cl2与稀NaOH溶液反应:Cl2+2OH-=Cl-+ClO-+ H2O
查看答案和解析>>
科目: 来源:2013-2014学年广东省等高三下学期2月联考理综化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍。下列说法正确的是(??? )
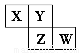
A.元素W的最高价氧化物对应水化物的酸性最强
B.单核阴离子半径的大小顺序为:r(W)>r(Z) >r(Y)
C.元素Y和元素Z的氢化物中均只存在极性共价键
D.元素Y和元素Z的最高正化合价相同
查看答案和解析>>
科目: 来源:2013-2014学年广东省等高三下学期2月联考理综化学试卷(解析版) 题型:选择题
下列实验操作或事实与预期实验目的或所得结论一致的是(??? )
选项????????????? 实验操作或事实????????????? 实验目的或结论
A????????????? 取少量试液于试管中,加入用HNO3酸化的BaCl2溶液,产生白色沉淀????????????? 说明试液中一定含有SO42-
B????????????? 分别向两支试管中加入等体积、等浓度的过氧化氢溶液,再在其中一支试管中加入少量MnO2????????????? 研究催化剂对过氧化氢分解速率的影响
C????????????? 将NaHCO3与HCl两种溶液相互滴加????????????? 可以鉴别这两种溶液
D????????????? C2H5Br与AgNO3溶液混合加热????????????? 检验C2H5Br中的溴元素
查看答案和解析>>
科目: 来源:2013-2014学年广东省等高三下学期2月联考理综化学试卷(解析版) 题型:选择题
下列说法都正确的是(??? )
①江河入海口三角洲的形成通常与胶体的性质有关? ②建筑使用了大量钢材,钢材是合金? ③“钡餐”中使用的硫酸钡是弱电解质? ④太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置? ⑤常用的消毒剂有氯气和二氧化硫,两者都有强氧化性 ⑥水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物
A.①②③④?? B.①②④⑥? C.①②⑤⑥? D.③④⑤⑥
查看答案和解析>>
科目: 来源:2013-2014学年广东省等高三下学期2月联考理综化学试卷(解析版) 题型:选择题
下列实验装置设计正确、且能达到目的的是(??? )
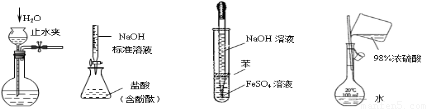
Ⅰ??????? Ⅱ??????????????? Ⅲ??????????????? Ⅳ
A.实验I: 检查装置的气密性
B.实验II:测定未知盐酸的浓度
C.实验III:制取并观察Fe(OH)2沉淀
D.实验IV:配置一定的物质的量浓度的稀硫酸溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com