
科目: 来源:2013-2014学年广东省、广雅高三四校联考理综化学试卷(解析版) 题型:选择题
水溶液中能大量共存的一组离子是(???? )
A.Na+、Al3+、Cl-、HCO3-???? ? B.H+、Fe2+、NO3-、SO42-
C.H+、 Mg2+、Cl-、NO3-??? ?? D.K+、Ag+、OH-、SO42-
查看答案和解析>>
科目: 来源:2013-2014学年广东省、广雅高三四校联考理综化学试卷(解析版) 题型:选择题
设nA为阿佛加德罗常数的数值,下列说法正确的是(???? )
A.等物质的量的H2和N2所含分子数均为nA
B.标准状况下,11.2L的己烷含有分子数为0.5nA
C.常温常压下,46gNO2含有原子数为3nA
D.1mol SiO2晶体中含nA个SiO2分子
查看答案和解析>>
科目: 来源:2013-2014学年广东省、广雅高三四校联考理综化学试卷(解析版) 题型:选择题
下列离子方程式正确的是(???? )
A.Al与NaOH溶液反应:2Al + 2OH- + 2H2O = 2AlO2- + 3H2↑
B.FeBr2溶液中通入少量Cl2:2Fe2++2Br-+Cl2=2Fe3++Br2+2Cl-
C.稀硝酸除银镜:Ag+2H++NO3- =Ag++NO2↑+H2O
D.烧碱溶液中通入过量SO2:2OH-+SO2=SO32-+H2O
查看答案和解析>>
科目: 来源:2013-2014学年广东省、广雅高三四校联考理综化学试卷(解析版) 题型:选择题
关于下列各实验装置的叙述中,不正确的是(???? )
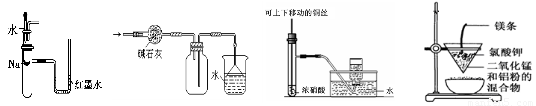
①???????????????????? ②?????????????? ③???????????????????? ④
A.装置①可用于验证Na与H2O反应是否放热
B.装置②可用于干燥、收集NH3,并吸收多余的NH3
C.装置③可用于制备并收集少量NO2
D.装置④可制得金属锰
查看答案和解析>>
科目: 来源:2013-2014学年广东省、广雅高三四校联考理综化学试卷(解析版) 题型:选择题
某小组设计如图装置(盐桥中盛有浸泡了KNO3溶液的琼脂)研究电化学原理。下列叙述正确的是(???? )
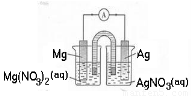
A.银片为负极,发生的反应为:Ag++e-= Ag
B.进行实验时,琼脂中K+移向Mg(NO3)2溶液
C.用稀硫酸代替AgNO3溶液,可形成原电池
D.取出盐桥,电流表依然有偏转
查看答案和解析>>
科目: 来源:2013-2014学年广东省、广雅高三四校联考理综化学试卷(解析版) 题型:选择题
已知短周期元素R、W、X、Y、Z的原子序数依次增大,其氢化物中上述元素的化合价如下表,下列说法正确的是(???? )
元素 | R | W | X | Y | Z |
化合价 | –4 | +1 | –4 | –2 | –1 |
A.离子还原性:Y2->Z-
B.离子半径W+>Z-
C.气态氢化物稳定性:RH4<XH4
D.酸性:H2YO4<HZO4
查看答案和解析>>
科目: 来源:2013-2014学年广东省、广雅高三四校联考理综化学试卷(解析版) 题型:选择题
常温时,下列各溶液中有关粒子浓度的说法正确的是(???? )
A.pH=5的NaHSO3溶液:c(HSO3-) > c(SO32-)> c(H2SO3)
B.pH=3的盐酸跟pH=11的氨水等体积混合: c(H+)>c(OH-)
C.pH<7的CH3COONa和CH3COOH的混合溶液 c(Na+)> c(CH3COO-)> c(H+)>c(OH-)
D.pH=12的NaOH溶液中:c(OH-)水电离=1.0×10-12 mol/L
查看答案和解析>>
科目: 来源:2013-2014学年广东省、广雅高三四校联考理综化学试卷(解析版) 题型:填空题
脱羧反应形成新的C-C键为有机合成提供了一条新的途径,例如:

(1)化合物I的分子式为_________,化合物I含有的官能团名称是______________,1mol化合物I完全燃烧需要消耗_____mol O2。
(2)化合物III与新制氢氧化铜反应的化学方程式为??????????????????? ??????????????? 。
(3)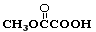 与
与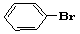 也可以发生类似反应①的反应,有机产物的结构简式为:________。
也可以发生类似反应①的反应,有机产物的结构简式为:________。
(4)化合物I有多种同分异构体,请写出任意2种符合下列条件的同分异构体的结构简式: ______________。(要求:①能与FeCl3溶液发生显色反应;②苯环上一氯取代产物有2种)
查看答案和解析>>
科目: 来源:2013-2014学年广东省、广雅高三四校联考理综化学试卷(解析版) 题型:填空题
煤制备CH4是一种有发展前景的新技术。
I. 煤炭气化并制备CH4包括以下反应:
C(s)+H2O(g)=CO(g)+H2 (g) ? ΔH 1 = +131 kJ/mol
CO(g) + H2O(g)=CO2 (g)+ H2(g) ? ΔH 2 = ?41 kJ/mol
CO(g) + 3H2 (g)=CH4 (g)+ H2O(g) ? ΔH 3 = ?206 kJ/mol
(1)写出煤和气态水制备CH4(产物还有CO2)的热化学方程式??????????????????????????????????? 。
(2)煤转化为水煤气(CO和H2)作为燃料和煤直接作为燃料相比,主要的优点有???????????????????? 。
(3)写出甲烷—空气燃料电池(电解质溶液为KOH溶液)中负极的电极反应式?????????????????????? 。
II. 对以上反应CO(g) + H2O(g)  CO2 (g)+ H2(g) ΔH 2 = ?41 kJ/mol,起始时在密闭容器中充入1.00 molCO和1.00 molH2O,分别进行以下实验,探究影响平衡的因素(其它条件相同且不考虑任何副反应的影响)。实验条件如下表:
CO2 (g)+ H2(g) ΔH 2 = ?41 kJ/mol,起始时在密闭容器中充入1.00 molCO和1.00 molH2O,分别进行以下实验,探究影响平衡的因素(其它条件相同且不考虑任何副反应的影响)。实验条件如下表:
实验编号 | 容器体积/L | 温度/°C |
① | 2.0 | 1200 |
② | 2.0 | 1300 |
③ | 1.0 | 1200 |
(1)实验①中c(CO2)随时间变化的关系见下图,请在答题卡的框图中,画出实验②和③中c(CO2)随时间变化关系的预期结果示意图。
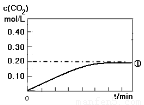
(2)在与实验①相同的条件下,起始时充入容器的物质的量:n(CO)=n(H2O)=n(CO2) =n( H2)=1.00mol。通过计算,判断出反应进行的方向。(写出计算过程。)
查看答案和解析>>
科目: 来源:2013-2014学年广东省、广雅高三四校联考理综化学试卷(解析版) 题型:填空题
钛有强度高和质地轻的优点,广泛应用于飞机制造业等。工业上利用钛铁矿,其主要成分为钛酸亚铁(FeTiO3)制备钛金属,工业流程如下: 已知:Ti与TiO2化学性质稳定,不溶于稀硫酸、稀盐酸等。
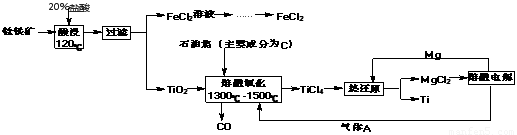
(1)请写出FeTiO3与稀盐酸反应的离子方程式:?????????????????????????????? ????? ????? 。
(2)请写出“熔融氧化”的化学方程式:???????????????????????????????????????? ?????? ???? 。
(3)电解氯化镁的阴极反应式为:???????????????????????????????????????????????? ,可循环利用的物质为:?????????????????????????????? (填化学式)。
(4)热还原法中能否改用钠代替镁作还原剂:???? (填“能”或“不能”);原因为:?????? ????????????????????????????????????? ? ?????????????????? 。
(5)用此方法制备得到的Ti金属常混有MgCl2和Mg,除杂试剂是????????? (填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com