
科目: 来源:2013-2014学年山东省烟台市高三3月模拟化学试卷(解析版) 题型:推断题
下图为某药物合成路线的一部分。
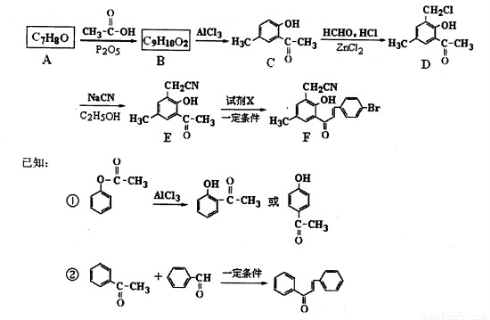
(1)A B的化学方程式为?????????????????????????????????????? 。E中的含氧官能团名称为????????????? 、? ????????? ? 。
B的化学方程式为?????????????????????????????????????? 。E中的含氧官能团名称为????????????? 、? ????????? ? 。
(2)若②的反应历程经历了中间产物 ,则该反应历程先后经历的反应类型为? ??????? ? 、???????? 。试剂X的结构简式为?? ????????? 。
,则该反应历程先后经历的反应类型为? ??????? ? 、???????? 。试剂X的结构简式为?? ????????? 。
(3)写出两种满足下列要求的D的同分异构体的结构简式。
①分子中有4种化学环境不同的氢原子;
②可发生水解反应,一种产物可发生银镜反应,另一种能与FeCl3发生显色反应;
③分子中的氯原子不与苯环直接相连。?????????????????????? ,??????????????????????? 。
查看答案和解析>>
科目: 来源:2013-2014学年山东省菏泽市高三3月模拟(一模)考试理综化学试卷(解析版) 题型:选择题
化学与生活、科学、技术、环境密切相关,下列说法正确的是
A.PM 2.5是指大气中直径接近于2.5×10-6m的细颗粒物,这些细颗粒物分散在空气中形成的混合物具有丁达尔效应
B.酒精可用来消毒是由于其具有强氧化性
C.废弃的金属、纸制品、塑料、玻璃均是可回收利用的资源
D.制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料
查看答案和解析>>
科目: 来源:2013-2014学年山东省菏泽市高三3月模拟(一模)考试理综化学试卷(解析版) 题型:选择题
设NA代表阿伏加德罗常数的数值,下列说法中正确的是
A.1.8 g重水(D2O)中含有的质子数和电子数均为1.0 NA
B.含4 mol Si-O键的二氧化硅晶体中,氧原子数为2NA
C.标准状况下,22.4 L NO 和22.4 L O2 混合后所得气体中分子总数为1.5 NA
D.将11.2 L Cl2 通入足量的石灰乳中制备漂白粉,转移的电子数为0.5 NA
查看答案和解析>>
科目: 来源:2013-2014学年山东省菏泽市高三3月模拟(一模)考试理综化学试卷(解析版) 题型:选择题
下列离子方程式的书写及评价均合理的是
选项????????????? 离子方程式????????????? 评价
A????????????? 将1molCl2通入到含1molFeI2的溶液中:
2Fe2++2I-+2Cl2 =2Fe3++4Cl-+I2????????????? 正确;Cl2过量,可将
Fe2+ 、I-均氧化
B????????????? Mg(HCO3)2溶液与足量的NaOH溶液反应:
Mg2++ HCO3-+ OH-=MgCO3↓+ H2O????????????? 正确;酸式盐与碱反应
生成正盐和水
C????????????? 过量SO2通入到NaClO溶液中:
SO2 + H2O + ClO-= HClO+HSO3-????????????? 正确;说明酸性:
H2SO3强于HClO
D????????????? 1mol/L的Na [Al(OH)4]溶液和2.5mol/L的HCl溶
液等体积互相均匀混合:2[Al(OH)4] -+ 5H+ =
Al3+ +Al(OH)3↓+ 5H2O????????????? 正确;[Al(OH)4] -与
Al(OH)3消耗的H+的物
质的量之比为2:3
查看答案和解析>>
科目: 来源:2013-2014学年山东省菏泽市高三3月模拟(一模)考试理综化学试卷(解析版) 题型:选择题
下列与有机物的结构、性质有关的叙述正确的是
A.乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色
B.乙酸与乙醇可以发生酯化反应,又均可与金属钠发生置换反应
C.葡萄糖、纤维素和蛋白质在一定条件下都能发生水解反应
D.石油经过分馏得到多种烃,煤经过分馏可制得焦炭、煤焦油等产品
查看答案和解析>>
科目: 来源:2013-2014学年山东省菏泽市高三3月模拟(一模)考试理综化学试卷(解析版) 题型:选择题
利用如图装置,完成很多电化学实验。下列有关此装置的叙述中,正确的是(?? )
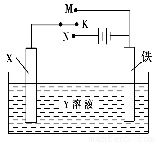
A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阴极保护法
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阴离子向铁电极移动
C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小
查看答案和解析>>
科目: 来源:2013-2014学年山东省菏泽市高三3月模拟(一模)考试理综化学试卷(解析版) 题型:选择题
归纳法是高中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结,归纳正确的是
①常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则有
c (Na+) + c(H+)=c(OH-) + c(CH3COO-)
②对已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,生成物的百分含量一定增加
③常温下,AgCl在同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同
④常温下,已知醋酸电离平衡常数为Ka,醋酸根水解平衡常数为Kh,水的离子积为Kw,则有:
Ka ∶Kh=Kw
A.①④?????????? B.①②④???????? C.②③?????? D.③④
查看答案和解析>>
科目: 来源:2013-2014学年山东省菏泽市高三3月模拟(一模)考试理综化学试卷(解析版) 题型:选择题
仅用下表提供的仪器(夹持仪器和试剂任选)不能实现相应实验目的的是
选项????????????? 实验目的????????????? 仪器
A????????????? 除去氢氧化铝胶体中的泥沙????????????? 漏斗(带滤纸)、烧杯、玻璃棒
B????????????? 从食盐水中获得NaCl晶体????????????? 坩埚、玻璃棒、酒精灯、泥三角
C????????????? 用0.10mol·L-1的盐酸测定未知浓度的NaOH溶液浓度????????????? 碱式滴定管、酸式滴定管、锥形瓶、胶
头滴管、烧杯
D????????????? 用MnO2和浓盐酸制取干燥、纯净
的Cl2????????????? 圆底烧瓶、分液漏斗、酒精灯、洗气瓶、
集气瓶、导管、石棉网
查看答案和解析>>
科目: 来源:2013-2014学年山东省菏泽市高三3月模拟(一模)考试理综化学试卷(解析版) 题型:填空题
工业制硫酸的过程中利用反应2SO2(g)+O2(g) 2SO3(g);△H<0,将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收。请回答下列问题:
2SO3(g);△H<0,将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收。请回答下列问题:
(1)一定条件下,向一带活塞的密闭容器中充入2 mol SO2和1mol O2发生反应,则下列说法正确的是??????????????????? 。
A.若反应速率v (SO2) ﹦v (SO3),则可以说明该可逆反应已达到平衡状态
B.保持温度和容器体积不变,充入2 mol N2,化学反应速率加快
C.平衡后仅增大反应物浓度,则平衡一定右移,各反应物的转化率一定都增大
D.平衡后移动活塞压缩气体,平衡时SO2、O2的百分含量减小,SO3的百分含量增大
E.平衡后升高温度,平衡常数K增大
F.保持温度和容器体积不变,平衡后再充入2molSO3,再次平衡时各组分浓度均比原平衡时的浓度大
(2)将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行反应得到如下表中的两组数据:
实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
SO2 | O2 | SO2 | O2 | |||
1 | T1 | 4 | 2 | x | 0.8 | 6 |
2 | T2 | 4 | 2 | 0.4 | y | 9 |
①实验1从开始到反应达到化学平衡时,v(SO2)表示的反应速率为??????? ,? 表中y? ﹦?????? 。
②T1????????????????? T2 ,(选填“>”、“<”或“=”), 实验2中达平衡时 O2的转化率为???????????????? 。
(3)尾气SO2用NaOH溶液吸收后会生成Na2SO3。现有常温下0.1 mol/L Na2SO3溶液,实验测定其pH约为8,完成下列问题:
① 该溶液中c(Na+)与 c(OH-) 之比为???????????????????????????????????????? 。
② 该溶液中c(OH-) = c(H+)+ ???????????? + ????????????? (用溶液中所含微粒的浓度表示)。
③ 当向该溶液中加入少量NaOH固体时,c(SO32-)???????????????? , 水的离子积Kw? ??? ??????????????? 。(选填“增大”、“减小”或“不变”)
(4)如果用含等物质的量溶质的下列各溶液分别来吸收SO2,则理论吸收量由多到少的顺序是 ????????????????????????????????????????????? 。
A. Na2CO3???????? ?? B. Ba(NO3)2 ??????????? C.Na2S???????? D.酸性KMnO4
查看答案和解析>>
科目: 来源:2013-2014学年山东省菏泽市高三3月模拟(一模)考试理综化学试卷(解析版) 题型:填空题
下图是某研究性学习小组设计的对一种废旧合金的各成分(含有Cu、Fe、Si 三种成分)进行分离、回收再利用的工业流程,通过该流程将各成分转化为常用的单质及化合物。
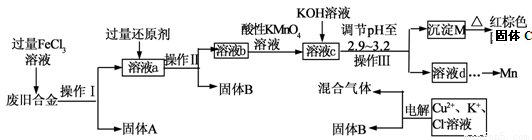
已知:298K时,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38, Ksp[Mn(OH)2] =1.9×10-13,
根据上面流程回答有关问题:
(1)操作Ⅰ、Ⅱ、Ⅲ指的是????????????????????????????????????? 。
(2)加入过量FeCl3溶液过程中可能涉及的化学方程式:???????????????????? 。
(3)过量的还原剂应是???????????????????????????????????????????????????????? 。
(4)①向溶液b中加入酸性KMnO4溶液发生反应的离子方程式为????????????????????? 。
②若用X mol/L KMnO4溶液处理溶液b,当恰好将溶液中的阳离子完全氧化时消耗KMnO4溶液YmL,则最后所得红棕色固体C的质量为????????????????? g(用含X、Y的代数式表示)。
(5)常温下,若溶液c中所含的金属阳离子浓度相等,向溶液c中逐滴加入KOH溶液,则三种金属阳离子沉淀的先后顺序为:????????????? ﹥??????????? ﹥??????????? 。(填金属阳离子)
(6)最后一步电解若用惰性电极电解一段时间后,析出固体B的质量为Z g,同时测得阴阳两极收集到的气体体积相等,则标况下阳极生成的最后一种气体体积为????? L(用含Z的代数式表示);该电极的反应式为???????????????????????????????????????????????????????????? .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com