
科目: 来源:2013-2014学年山东省德州市高三上学期期末考试化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.恒温时,向水中加入少量固体硫酸氢钠,c(H+)增大,水的离子积常数Kw不变
B.0.1mol/LCH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.对于N2(g)+3H2(g) 2NH3(g),其他条件不变,充入N2,正反应速率增大,逆反应速率减小
2NH3(g),其他条件不变,充入N2,正反应速率增大,逆反应速率减小
D.在硫酸钡悬浊液中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3)
查看答案和解析>>
科目: 来源:2013-2014学年山东省德州市高三上学期期末考试化学试卷(解析版) 题型:选择题
在一定温度下,固定体积为2L密闭容器中,发生反应:2SO2(g)+O2(g)  2SO3(g) △H<0,n(SO2)随时间的变化如表:
2SO3(g) △H<0,n(SO2)随时间的变化如表:
时间/min | 0 | 1 | 2 | 3 | 4 | 3 |
n(SO2)/mol | 0.20 | 0.1 6 | 0.13 | 0.11 | 0.08 | 0.08 |
则下列说法正确的是
A.当v(SO2)=v(SO3)时,说明该反应已达到平衡状态
B.用O2表示0~4min内该反应的平均速率为0.005mol/(L·min)
C.若升高温度,则SO2的反应速率会变大,平衡常数K值会增大
D.平衡时再通入O2,平衡右移,O2转化率减小,SO2转化率增大
查看答案和解析>>
科目: 来源:2013-2014学年山东省德州市高三上学期期末考试化学试卷(解析版) 题型:选择题
对下列装置的叙述错误的是

A.X如果是HCl,则不论a和b用导线连接还是a和b分别连接直流电源正、负极时,H+的移动方向均相同
B.X如果是硫酸铜,a和b分别连接直流电源正、负极,一段时间后铁片质量增加
C.X如果是硫酸铁,则不论a和b是否用导线连接,铁片均发生氧化反应
D.X如果是NaCl,则a和b连接时,该装置可模拟生铁在食盐水中被腐蚀的过程
查看答案和解析>>
科目: 来源:2013-2014学年山东省德州市高三上学期期末考试化学试卷(解析版) 题型:填空题
I:化学是一门以实验为主的科学,化学实验是学习探究物质性质的基本方法之一。(1)化学实验中,常将溶液或试剂进行酸化,下列酸化处理的措施中正确的是
A.定性检验SO32-,可用HNO3酸化的BaCl2溶液
B.配制FeCl2溶液时通常加少量HNO3酸化,减小其水解程度
C.检验某溶液中是否含Cl-,用HNO3酸化的AgNO3溶液
D.酸性高锰酸钾溶液经常用盐酸酸化
(2)下列有关说法中正确的有??????? ?
①用pH试纸测得氯水的pH为3.5
②用瓷坩埚高温熔融NaOH固体
③加入浓NaOH溶液,加热产生使湿润的红色石蕊试纸变蓝的气体,则原溶液中一定含有NH4+
④向溶液中加入少量双氧水,再加几滴KSCN溶液后溶液变红,则原溶液中一定含有Fe2+
⑤实验时不慎被玻璃划破手指,引起轻微流血时,可用三氯化铁溶液涂抹止血
II:(1)某温度下,纯水中c(H+)=2.0×10-7mol·L-1.该温度下,0.9mol·L-1NaOH溶液与0.1mol·L-1 HCl溶液等体积混合(不考虑溶液体积变化)后,溶液的pH= ???? 。
(2)向含有0.020 molCH3COOH的溶液中加入0.020mol CH3COONa固体,溶液pH增大,主要原因是 ?? ?? ;已知该混合溶液中c(Na+)<c(CH3COO-),则c(CH3COOH)?????? c(CH3COO-)(用“>”、“<”、“=”符号填空)。
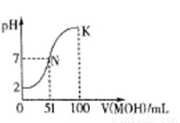
(3)常温下,向100 mL 0.01mol·L-1HA溶液逐滴加入0.02mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。
回答下列问题:
①由图中信息可知HA为??? 酸(填“强”或“弱”)。
②K点对应的溶液中,c(M+)+c(MOH)=???? mol·L-1。
查看答案和解析>>
科目: 来源:2013-2014学年山东省德州市高三上学期期末考试化学试卷(解析版) 题型:填空题
碳和氮的许多化合物在工农业生产和生活中有重要的作用。
(1)工业上生产硝酸所需要的一氧化氮常用氨气来制备,该反应的化学方程式为 ?????????????????????????????????????????????????????????????????? 。
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2 NH4(s)??? ? △H=-l59.5 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)? △H=+116.5 kJ·mol-1
③H2O(1)=H2O(g)? ??????????????????? △H=+44.0kJ·mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式?????????????????
(3)以氨气代替氢气研发氨燃料电池是当前科研的一个热点,已知氨燃料电池使用的电解质溶液是2mol·L-1的KOH溶液,电池反应为:4NH3+3O2=2N2+6H2O。该电池负极的电极反应式为??????????????? ;每消耗3.4g NH3转移的电子数为??????????????? (阿伏加德罗常数的值用NA表示)。
(4)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g) N2(g)+CO2(g)? △H=Q kJ·mol-1。
N2(g)+CO2(g)? △H=Q kJ·mol-1。
在T1℃时,反应进行到不同时间测得各物质的浓度如下:
???????? 时间(Min) 浓度(mol·L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①T1℃时,该反应的平衡常数K= ????? ;
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是? ?? ? (填字母编号)。
a.加入一定量的活性炭 ???? b.通人一定量的NO
c.适当缩小容器的体积?????? d.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则Q ??? 0(填“>”或“<”)。?
查看答案和解析>>
科目: 来源:2013-2014学年山东省德州市高三上学期期末考试化学试卷(解析版) 题型:实验题
以电石渣(主要成分是Ca(OH)2,含SiO2以及其它少量杂质)为原料生产氯酸钾联合生产碳酸钙的流程如下:
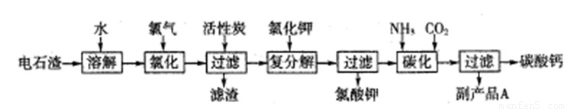
回答下列问题:
(1)电石渣溶于水形成电石渣浆时发生的主要反应的化学方程式为:????????????
(2)氯化过程的温度控制在75~80℃,该过程主要反应的离子方程式为:?????????
(3)该流程中加入活性炭的作用是??????????????????????????
(4)碳化过程中,先向溶液中通入氨气,再通入CO2。
①实验室通常采用加热氯化铵和氢氧化钙混合物的方法制取氨气。某学习小组选取下图所给部分装置制取并收集纯净的氨气。
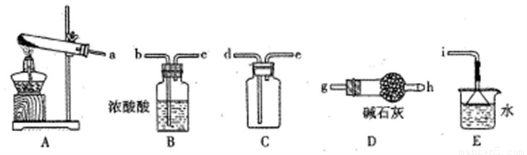
如果按气流方向连接各仪器接口,你认为正确的顺序为a→ ? ? 、????? → ???? 、????? →i。其中与i相连漏斗的作用是?? ????????????? 。
②实验室中还可用固体氢氧化钠和浓氨水制取少量氨气,下列最适合完成该实验的简易装置是 ??? ?? (填编号)
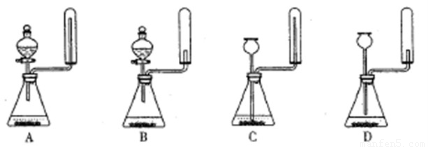
(5)副产品A的化学式为 ????????? 。
查看答案和解析>>
科目: 来源:2013-2014学年山东省德州市高三上学期期末考试化学试卷(解析版) 题型:填空题
)2013年全国各地连续出现了严重的雾霾天气,给人们的出行及身体造成了极大的危害,因此研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
I.脱硫技术能有效控制SO2对空气的污染。
(1)海水呈弱碱性,主要含有Na+、K+、Ca2+、Mg2+、CI-、SO42-、Br-、HCO3-等离子。含SO2的烟气可利用海水脱硫,其工艺流程如下图所示:
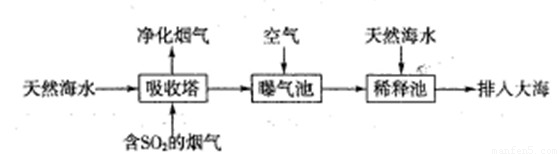
①向曝气池中通入空气的目的是 ???????????????????????
②通入空气后曝气池中海水与天然海水相比,浓度没有明显变化的离子是??? 。
a.Cl-? B.SO42-? C.HCO3-
(2)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示。(电极材料为石墨)
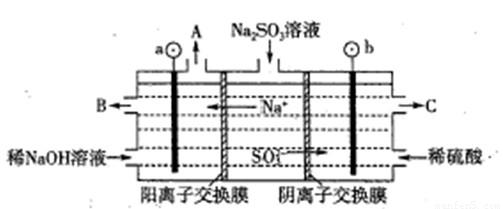
①图中b极要连接电的(填“正”或“负”) ?? 极,C口流出的物质是? ?????? 。
②SO32-放电的电极反应式为???????????????????????? ??
③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因 ?? ? 。
II.我国的能消费结构以燃煤为主,将煤气化可减少环境污染,但煤气化过程中能产生有害气体H2S,用足量的Na2CO3溶液可吸收,该反应的离子方程式为 ? 。
(已知:H2S Kal=9.1×10-8;Ka2=1.1 ×10-12;H2CO3? Kal=4.30×10-7;Ka2=5.61 ×10-11)
查看答案和解析>>
科目: 来源:2013-2014学年山东省德州市高三模拟检测(一模)理综化学试卷(解析版) 题型:选择题
化学与社会、生产、生活密切相关。下列说法正确的是
A.日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应
B.神舟10号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是单晶硅
C.棉、麻、合成纤维完全燃烧都只生成CO2和H2O
D.工业上获得大量的乙烯、丙烯、丁二烯的方法是石油裂化
查看答案和解析>>
科目: 来源:2013-2014学年山东省德州市高三模拟检测(一模)理综化学试卷(解析版) 题型:选择题
萜品醇可作为消毒剂、抗氧化剂和溶剂。已知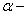 萜品醇的结构简式如下式,则下列说法错误的是
萜品醇的结构简式如下式,则下列说法错误的是
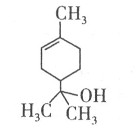
A.1mol该物质最多能和lmol氢气发生加成反应
B.分子中含有的官能团为羟基和碳碳双键
C.该物质能和乙酸发生酯化反应
D.分子式为C9H18O
查看答案和解析>>
科目: 来源:2013-2014学年山东省德州市高三模拟检测(一模)理综化学试卷(解析版) 题型:选择题
W、X、Y、Z是短周期元素,其部分性质如下表
W | 单质是淡黄色固体 |
X | 在地壳中的含量居第二位 |
Y | 原子最外层电子数是电子总数的2/3 |
Z | 第三周期原子半径最小的金属 |
下列说法正确的是
A.Z的氧化物属于碱性氧化物
B.最高价氧化物对应水化物的酸性:Y>X
C.离子半径:Z>W
D.气态氢化物的热稳定性:X>W
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com