
科目: 来源:2013-2014学年上海市闵行区高三上学期期末教学质量检测化学试卷(解析版) 题型:选择题
向mg镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。向反应后的溶液中加入c mol/L氢氧化钾溶液VmL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系正确的是
A. B.
B. C.n=m+17Vc
D.
C.n=m+17Vc
D. <p<
<p<
查看答案和解析>>
科目: 来源:2013-2014学年上海市闵行区高三上学期期末教学质量检测化学试卷(解析版) 题型:填空题
在一百多种化学元素中,非金属占了23种。80%的非金属元素在社会中占重要位置。如C、N、O、Si、Cl等。
(1)氯元素原子最外电子层上有 种能量不同的电子,该元素的简单阴离子核外电子排布式是 。
(2)由氮元素与硅元素组成的物质,可用于制造发动机的耐热部件,因为它属于 晶体,请写出该化合物的化学式 。
(3)下列事实能说明氯与氧两元素非金属性相对强弱的有 。(选填编号)
a.Cl原子最外层电子数比氧多
b.酸性:HCl>H2O
c.ClO2中氯元素为+4价,氧元素为−2价
d.沸点:H2O>HCl
与Cl2相比较,ClO2处理水时被还原成Cl-,不生成有机氯代物等有害物质。工业上可用亚氯酸钠和稀盐酸为原料制备ClO2,反应如下:NaClO2 +HCl ClO2↑+___________________(没有配平)
ClO2↑+___________________(没有配平)
(4)上述方程式中,缺项物质是___________,配平方程式,并在下面补全反应物系数。____NaClO2 +____HCl
(5)该反应中氧化剂和还原剂的物质的量之比是 。生成0.2 mol ClO2转移电子的物质的量为 _______ mol。
(6)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某污水中含CN-a mg/L,现用ClO2将CN-氧化,只生成两种无毒气体。处理100m3这种污水,至少需要ClO2 _______ mol 。
查看答案和解析>>
科目: 来源:2013-2014学年上海市闵行区高三上学期期末教学质量检测化学试卷(解析版) 题型:填空题
某兴趣小组探究以芒硝Na2SO4·10H2O和CaO为原料制备Na2CO3。
(1)将CaO水化后,与芒硝形成Na2SO4-Ca(OH)2-H2O三元体系,反应后过滤,向滤液中通入CO2,期望得到Na2CO3。三元体系中反应的离子方程式为: SO42-+ Ca(OH)2(s)+2H2O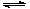 CaSO4·2H2O(s)+2 OH-
CaSO4·2H2O(s)+2 OH-
该反应的平衡常数表达式K=_________________________。
往Na2SO4-Ca(OH)2-H2O三元体系中添加适量的某种酸性物质,控制pH=12.3 [即c(OH-)=0.02mol/L],可使反应在常温下容易进行。反应后过滤,再向滤液中通入CO2,进一步处理得到Na2CO3。
(2)在Na2SO4-Ca(OH)2-H2O三元体系中不直接通入CO2,其理由是_______________________________________________________________。
(3)添加的酸性物质须满足的条件(写出两点)是_____________、______________。
(4)用平衡移动原理解释添加酸性物质的理由:____________________________________;以HA表示所添加的物质,则总反应的离子方程式可写为_______________________。
(5)Na2CO3溶液中存在水解平衡:CO32-+H2O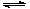 HCO3-+OH-。下列说法错误的是_________。
HCO3-+OH-。下列说法错误的是_________。
a.加水稀释,溶液中所有离子的浓度都减小
b.通入CO2,溶液pH减小
c.加入NaOH固体, 减小
减小
d.稀释溶液,平衡常数增大
查看答案和解析>>
科目: 来源:2013-2014学年上海市闵行区高三上学期期末教学质量检测化学试卷(解析版) 题型:实验题
如图1所示是实验室中制取气体的一种简易装置。
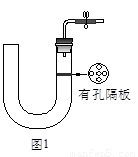
(1)请简述检验它的气密性的方法_______________________。
(2)利用如图1所示装置可以制取(填反应物状况及发生反应是否需要的条件)________________________气体。
某同学设计如图2所示装置,用粗铁粒与16.9%稀硝酸反应制取NO气体并探究产物中铁的价态。请回答有关问题。
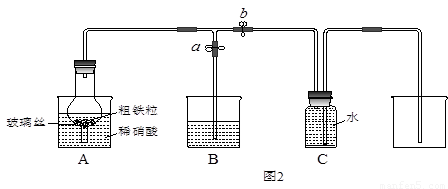
(3)已知16.9%稀硝酸的密度为1.10g/cm3,则其物质的量浓度为____________(计算结果保留两位小数)。用若用63%的硝酸配制16.9%稀硝酸500mL,所需的玻璃仪器有玻璃棒、烧杯和 。
(4)当打开止水夹a、关闭止水夹b时,A装置的干燥管中观察到的现象是_______________________。B装置烧杯中液体的作用是__________________________________。当A装置中气体几乎无色时,打开止水夹b,关闭止水夹a,可用C装置收集NO气体。
(5)已知下列反应可以发生:Fe2O3+3KNO3+4KOH 2K2FeO4+3KNO2+2H2O,而A装置中的稀硝酸即使换成浓硝酸,也不能生成+6价的铁的化合物,其原因是________。
2K2FeO4+3KNO2+2H2O,而A装置中的稀硝酸即使换成浓硝酸,也不能生成+6价的铁的化合物,其原因是________。
a.HNO3 的氧化性比KNO3弱
b.反应的温度不够
c.HNO3 的热稳定性比KNO3差
d.FeO42-不能存在于酸性溶液中
(6)现有仪器和药品:试管和胶头滴管,0.1mol/LKSCN溶液、0.2mol/L酸性KMnO4溶液、0.1mol/LKI溶液、氯水等。请你设计一个简单实验,探究A装置烧杯里完全反应后含铁可能的价态,填写下列实验报告:
|
实验步骤 |
操作 |
现象与结论 |
|
第一步 |
取少量液体装于试管,向试 管中滴入几滴KSCN溶液。 |
|
|
第二步 |
|
若溶液紫色褪去,则说明含有Fe2+; 若无明显变化,则说明不含Fe2+。 |
查看答案和解析>>
科目: 来源:2013-2014学年上海市闵行区高三上学期期末教学质量检测化学试卷(解析版) 题型:填空题
氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下:
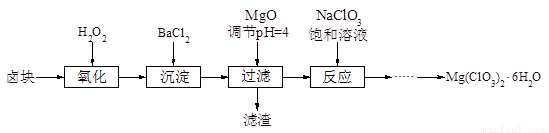
已知:
①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
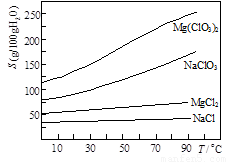
②几种化合物的溶解度(S)随温度(T)变化曲线如图。
(1)加MgO后过滤所得滤渣的主要成分为 。
(2)加入BaCl2的目的是除去SO42-,如何检验SO42-已沉淀完全? 。
(3)加入NaClO3饱和溶液会发生如下反应:
MgCl2+2NaClO3 Mg(ClO3)2+2NaCl↓,
Mg(ClO3)2+2NaCl↓,
请利用该反应,结合右图,制取Mg(ClO3)2·6H2O的实验步骤依次为:
①取样,加入NaClO3饱和溶液充分反应,② ;③ ;④ ;⑤过滤、洗涤,获得Mg(ClO3)2·6H2O晶体。
产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量3.50g产品溶解定容成100mL溶液。
步骤2:取10mL于锥形瓶中,加入10mL稀硫酸和20mL1.000mol/L的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100mol/LK2Cr2O7溶液滴定至终点,此过程中反应的离子方程式为:Cr2O72-+6Fe2++14H+ 2Cr3++6Fe3++7H2O。
2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7溶液15.00mL。
(4)上述产品测定中需要检查是否漏液的仪器有 。
步骤3中若滴定前不用标准液润洗滴定管,会导致最终结果偏 。(填“大”或“小”)。
(5)产品中Mg(ClO3)2·6H2O的质量分数为 。(计算结果保留两位小数)
查看答案和解析>>
科目: 来源:2013-2014学年上海市闵行区高三上学期期末教学质量检测化学试卷(解析版) 题型:填空题
Diels-Alder反应为共轭双烯与含烯键或炔键的化合物相互作用生成六元环状化合物的
反应,最简单的Diels-Alder反应是 +
+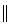

 。
。
氯丁橡胶是理想的电线电缆材料,其单体2-氯-1,3-丁二烯也是一种重要的有机合成中间体,该单体的一种合成路线及有关转化关系图如下。
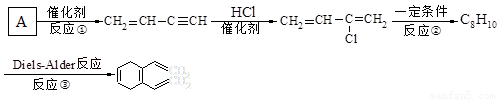
已知:CH2=CH-C≡CH由A二聚得到。
回答下列问题:
(1)A的结构式为_____________________,反应①的反应类型是________________。
(2)A在一定条件下可以四聚成环状化合物C8H8,其结构简式为_________________。
(3)C8H8的一种同分异构体属于芳香烃,该芳香烃与1,3-丁二烯可以合成丁苯橡胶,写出此合成反应的化学方程式_________________________________________________。
(4)写出反应③的化学方程式_________________________________________________。
(5)2-氯-1,3-丁二烯的另一种制法是由1,3-丁二烯通过两步反应制得,写出有关的化学方程式。
查看答案和解析>>
科目: 来源:2013-2014学年上海市闵行区高三上学期期末教学质量检测化学试卷(解析版) 题型:填空题
瘤突胡椒具有抗肿瘤和调节血脂功能,其合成路线如下。

回答下列问题:
(1)化合物A中的含氧官能团的名称为________________________。
(2)B→C的反应类型是___________,G→H的反应类型是___________,
(3)写出同时满足下列条件的E的一种同分异构体的结构简式_______________________。
①是苯的同系物的衍生物
②能发生银镜反应,其中一种水解产物也能发生银镜反应
③有四种化学环境不同的氢原子,其数目比为6∶3∶2∶1。
(4)写出B与足量的碳酸钠溶液反应的化学方程式_________________________________。
(5)已知:R1-CH=CH-R2 R1-CHO+R2-CHO。
R1-CHO+R2-CHO。
化合物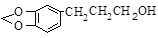 是一种合成药物的中间体,请写出以CH2(COOH)2、CH2Cl2 及
是一种合成药物的中间体,请写出以CH2(COOH)2、CH2Cl2 及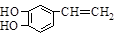 为原料制备该化合物的合成路线流程图(无机试剂任用)。
为原料制备该化合物的合成路线流程图(无机试剂任用)。
(合成路线常用的表示方式为:A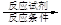 B……
B……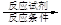 目标产物)
目标产物)
查看答案和解析>>
科目: 来源:2013-2014学年上海市闵行区高三上学期期末教学质量检测化学试卷(解析版) 题型:填空题
闪锌矿(主要成份为ZnS)是含锌主要矿物之一,空气中高温加热闪锌矿生成ZnO和SO2。ZnO用于冶炼金属锌,SO2可制亚硫酸盐或硫酸。回答下列问题(以下计算保留2位小数)
(1)取1.56 g闪锌矿样品,在空气中高温加热(杂质不反应),充分反应后,冷却,得到残留
固体的质量为1.32 g,样品中含硫化锌的质量分数是_________。
(2)取1.95 g锌加入到12.00 mL 18.4 mol/L的浓硫酸中(反应中只生成一种还原产物),充分反应后,小心地将溶液稀释到1000 mL,取出15.00 mL,以酚酞为指示剂,用0.25 mol/L的NaOH溶液中和余酸,耗用NaOH溶液的体积为21.70 mL。
①反应后溶液中多余的硫酸是____________ mol。
②通过计算确定浓硫酸被还原的产物是________________________。
(3)将标况下4.48 L SO2气体慢慢通入200 mL一定浓度NaOH溶液中,SO2气体全部被吸收,将反应后的溶液在空气中小心蒸干(不考虑酸式盐的分解),得到不超过两种物质的无水晶体26.8g。通过计算确定所得晶体的成分与物质的量。
查看答案和解析>>
科目: 来源:2013-2014学年上海市静安区高三上学期期末考试化学试卷(解析版) 题型:选择题
2013年度诺贝尔化学奖再次授予计算化学领域的科学家。以下基于结构理论进行繁难计算得出的是
A.天然气的热值 B.合成氨的原子利用率
C.尿素的含氮量 D.p轨道电子云的形状
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com