
科目: 来源:2015届福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强,下列说法正确的是
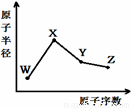
A.化合物XZW既含离子键也含共价键
B.对应气态氢化物的稳定性Y>Z
C.对应简单离子半径:X>W
D.Y的氧化物能与Z或X的最高价氧化物对应的水化物反应
查看答案和解析>>
科目: 来源:2015届福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
下列关于价电子构型为3s23p4的粒子描述正确的是
A.它的元素符号为O
B.它的核外电子排布式为1s22s22p63s23p4
C.它可与H2生成液态化合物
D.其电子排布轨道式为: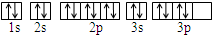
查看答案和解析>>
科目: 来源:2015届福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示,单位为kJ·mol-1)。
|
|
I1 |
I2 |
I3 |
I4 |
…… |
|
R |
740 |
1 500 |
7 700 |
10 500 |
…… |
下列关于元素R的判断中一定正确的是
A.R的最高正价为+3价 B.R元素位于元素周期表中第ⅡA族
C.R元素的原子最外层共有4个电子 D.R元素基态原子的电子排布式为1s22s2
查看答案和解析>>
科目: 来源:2015届福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
短周期元素X、Y的原子序数相差2。下列有关叙述错误的是
A.X与Y可能位于同一主族
B.X与Y可能形成离子化合物XY
C.X与Y可能形成共价化合物XY
D.X与Y是属于同一周期的两种元素
查看答案和解析>>
科目: 来源:2015届福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.非金属元素呈现的最高化合价不超过该元素原子的最外层电子数
B.非金属元素呈现的最低化合价,其绝对值等于该元素原子的最外层电子数
C.最外层有2个电子的原子都是金属原子
D.最外层有5个电子的原子都是非金属原子
查看答案和解析>>
科目: 来源:2015届福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
下列叙述正确的是
①两种原子构成的共价化合物分子中的化学键都是极性键;
②两种不同非金属元素原子间形成的化学键都是极性键;
③含有非极性键的化合物一定是共价化合物;
④只要是离子化合物,其熔点就比共价化合物的熔点高;
⑤难失去电子的原子,易形成阴离子;
⑥单质分子中不存在化学键,化合物的分子中才存在化学键;
⑦离子化合物中一定含有离子键。
A.只有②⑦ B.只有①⑦ C.只有⑦ D.只有①⑤⑦
查看答案和解析>>
科目: 来源:2015届福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
A、B、C、D四种元素,已知A元素是地壳中含量最多的元素;B元素为金属元素,它的原子核外K、L层上电子数之和等于M、N层电子数之和;C元素是第3周期第一电离能最小的元素;D元素在第3周期中第一电离能最大。下列有关叙述错误的是
A.四种元素A、B、C、D分别为O、Ca、Na、Ar
B.元素A、B、C两两组成的化合物可为CaO、CaO2、Na2O、Na2O2等
C.元素A、C简单离子的半径大小关系为A<C
D.元素B、C电负性大小关系为B>C
查看答案和解析>>
科目: 来源:2015届福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
近年来,科学家合成了一系列具有独特化学特性的(AlH3)n氢铝化合物。已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如图。下列有关说法肯定错误的是
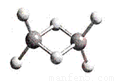
A.化合物Al2H6中存在分子间作用力
B.氢铝化合物可能成为未来的储氢材料和火箭燃料
C.Al2H6在空气中完全燃烧,产物为氧化铝和水
D.Al2H6中含有离子键和极性共价键
查看答案和解析>>
科目: 来源:2015届福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
有关甲醛( )、苯、二氧化碳及水说法不正确的是
)、苯、二氧化碳及水说法不正确的是
A.苯与B3N3H6互为等电子体,且分子中原子共平面
B.甲醛、苯和二氧化碳中碳原子均采用sp2杂化
C.苯、二氧化碳是非极性分子,水和甲醛是极性分子
D.水的沸点比甲醛高得多,是因为水分子间能形成氢键,而甲醛分子间不能形成氢键
查看答案和解析>>
科目: 来源:2015届福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
按要求填空
(1)a、e属于短周期的同族元素,a的原子半径最小,e的原子半径最大(稀有气体除外),写出它们组成化合物的化学式__________,其化学键的类型是 。
(2)C、N、O的第一电离能由大到小的顺序为
。NH3·H2O的电离方程式为 NH3·H2O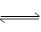 NH4++OH-,试判断溶于水后,形成的合理结构是______。(填图中的字母)
NH4++OH-,试判断溶于水后,形成的合理结构是______。(填图中的字母)

AsH3空间形状为______________;(CH3)3 Ga为非极性分子,则其中镓原子的杂化方式为__________;CaC2中C22―、N2与O22+互为等电子体,O22+的电子式可表示为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com