
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 碳酸钠可用于治疗胃酸过多 | Na2CO3与盐酸反应 | Ⅰ对,Ⅱ对,有 |
| B | 将Na2O2溶于水,立刻在所得溶液中滴入酚酞,溶液变红色 | Na2O2与水反应生成氢氧化钠 | Ⅰ对,Ⅱ错,有 |
| C | 铝制品很耐腐蚀 | 铝在常温下很难被氧气氧化 | Ⅰ对,Ⅱ对,有 |
| D | 氯气可用于自来水消毒、杀菌 | 氯气与水反应生成次氯酸 | Ⅰ对,Ⅱ对,有 |
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
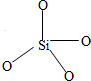 分子筛是一类具有多孔性的铝硅酸钠盐.分子筛晶体中的骨架是由SiO4四面体和AlO4四面体通过顶角的氧原子连接而成的,经测定硅铝比(SiO2-Al2O3的物质的量之比)为6:3,AlO4四面体带一个单位负电荷.SiO4可表示为右图:
分子筛是一类具有多孔性的铝硅酸钠盐.分子筛晶体中的骨架是由SiO4四面体和AlO4四面体通过顶角的氧原子连接而成的,经测定硅铝比(SiO2-Al2O3的物质的量之比)为6:3,AlO4四面体带一个单位负电荷.SiO4可表示为右图:查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com