
科目: 来源:2015届安徽省高二上学期期中考试化学试卷(解析版) 题型:选择题
乙烯酮(CH2=C=O)在一定条件下能与含活泼氢的化合物发生加成反应,反应可表示为CH2=C=O + HA → CH3—CO—A。乙烯酮在一定条件下可与下列试剂加成,其产物不正确的是
A.与HCl加成生成CH3COCl
B.与H2O加成生成CH3COOH
C.与CH3COOH加成生成CH3COOCOCH3
D.与CH3OH加成生成CH3COCH2OH
查看答案和解析>>
科目: 来源:2015届安徽省高二上学期期中考试化学试卷(解析版) 题型:选择题
戊二醛(OHCCH2CH2CH2CHO)在pH为7.5~8.5时,杀菌消毒的作用最强,可杀灭细菌的繁殖体和芽孢、真菌、病毒,其作用较甲醛强2~10倍。下列有关说法正确的是
A.戊二醛的消毒原理与漂白粉、臭氧等消毒剂相同
B.1 mol 戊二醛分子可被1 mol Cu(OH)2完全氧化
C.CH3CH=CHCH2COOH与戊二醛互为同分异构体
D.10g戊二醛完全燃烧需消耗0.5 mol O2
查看答案和解析>>
科目: 来源:2015届安徽省高二上学期期中考试化学试卷(解析版) 题型:选择题
如图为某有机物的结构简式。又知酯类在铜铬氧化物(CuO·CuCrO4)催化下,与氢气反应得到醇,羰基双键可同时被还原,但苯环在催化氢化过程中不变,其反应原理如下:
 关于该化合物的下列说法中,正确的是
关于该化合物的下列说法中,正确的是

A.该有机物的化学式为C20H14O5
B.1mol该有机物与浓溴水反应,消耗5molBr2
C.与足量氢氧化钠溶液充分反应,所得产物中相对分子质量较小的钠盐为HCOONa
D.1mol该有机物在铜铬氧化物催化下能与2mol氢气发生反应
查看答案和解析>>
科目: 来源:2015届安徽省高二上学期期中考试化学试卷(解析版) 题型:填空题
A、B、C三种有机物的分子式均为C3H6O2,分子中都含有甲基。做有关实验并记录反应情况如下表:
|
|
NaOH溶液 |
银氨溶液,加热 |
新制Cu(OH)2 |
金属钠 |
|
A |
中和反应 |
无银镜 |
溶解 |
产生氢气 |
|
B |
不反应 |
有银镜 |
加热,有红色沉淀 |
产生氢气 |
|
C |
水解反应 |
有银镜 |
加热,有红色沉淀 |
不反应 |
则A、B、C三种有机物的结构简式分别为:
A_______________________,B_________________________,C_______________________________。
查看答案和解析>>
科目: 来源:2015届安徽省高二上学期期中考试化学试卷(解析版) 题型:填空题
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
|
实 验 步 骤 |
解 释 或 实 验 结 论 |
|
(1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍。 |
试通过计算填空: (1)A的相对分子质量为: 。 |
|
(2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g。 |
(2)A的分子式为: 。 |
|
(3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。 |
(3)用结构简式表示A中含有的官能团: 。 |
|
(4)A的核磁共振氢谱如下图:
|
(4)A中含有 种氢原子。 |
|
(5)综上所述,A的结构简式 。 |
查看答案和解析>>
科目: 来源:2015届安徽省高二上学期期中考试化学试卷(解析版) 题型:实验题
下面是某化学学习小组的同学进行研究性学习的过程,请你参与并协助他们完成相关学习任务。
I.课本介绍了乙醇氧化的实验:把一端弯成螺旋状的铜丝放在酒精灯外焰加热,待铜丝表面变黑后立即把它插入盛有约2 mL乙醇的试管里,反复操作几次。注意闻生成物的气味,并观察铜丝表面的变化。
(1)小赵同学用化学方法替代“闻生成物的气味”来说明生成物的出现,该化学方法中所另加的试剂及出现的主要现象是: 。(用所学的知识回答)。
(2)小赵同学在探究“闻生成物的气味”的替代方法时,偶然发现向溴水中加入足量的乙醛溶液,可以看到溴水褪色。该同学为解释上述现象,提出三种猜想:(注:褪色原因只有一种)
①溴与乙醛发生取代反应;② ;③由于醛基具有还原性,溴将乙醛氧化为乙酸。
为探究哪种猜想正确,小李同学提出了
如下两种实验方案:
方案一:用pH试纸检测溴水褪色后溶液的酸碱性;
方案二:测定反应前溴水中Br2的物质的量和反应后溶液中Br—离子的物质的量。
(3)根据方案一,若 ,则猜想②不成立。
(4)小李同学认为:假设测得反应前溴水中Br2的物质的量为amol,若测得反应后n(Br—)= mol,则说明溴与乙醛发生取代反应。
(5)小吴同学设计如下实验方案:①按物质的量之比为1:5配制KBrO3—KBr溶液,加合适的适量的酸,完全反应并稀至1L,生成0.5molBr2。②取上述溶液10mL加入足量乙醛溶液,使之褪色,然后将所得溶液稀释为100mL,准确量取其中10mL。③加入过量的AgNO3溶液,过滤、洗涤、干燥后称量得到淡黄色固体0.188g。若已知CH3COOAg易溶于水。
试通过计算判断:溴与乙醛发生反应的化学方程式为 ;
小张同学认为合适的酸既不是硫酸也不是盐酸,这是为什么? 。
Ⅱ.小钱同学利用下图装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物),图中铁架台等装置已略去。实验时,先加热玻璃管中的铜丝,约lmin后鼓入空气。
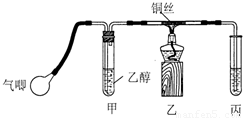
请填写下列空白:
(1)乙醇发生催化氧化的化学方程式为 。
(2)实验时,小钱同学将甲装置浸在70℃~80℃的水浴中,目的是 _。
小孙同学认为:由于小钱同学装置设计上的缺陷,实验进行时可能会 ____________。
(3)反应发生后,移去酒精灯,利用反应自身放出的热量可维持反应继续进行。进一步探究表明,鼓气速度与反应体系的温度关系曲线如图所示。
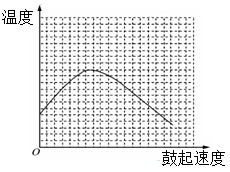
请你解释鼓气速度过快,反应体系温度反而下降的原因是: 。
你认为该实验中“鼓气速度”这一变量可用 来计量。
查看答案和解析>>
科目: 来源:2015届安徽省高二上学期期中考试化学试卷(解析版) 题型:填空题
龙胆酸甲酯是制取抗心律失常药物——氟卡尼的中间体。
I.已知龙胆酸甲酯结构如右图 所示:
所示:
(1)龙胆酸甲酯的含氧官能团名称为 。
(2)下列有关龙胆酸甲酯的描述,不正确的是 (填字母)。
A.不能发生消去反应 B.难溶于水 C.与苯酚互为同系物 D.能与溴水反应 E.1 mol龙胆酸甲酯在镍催化下加氢最多需要4molH2 F.能与碳酸钠溶液反应产生二氧化碳
(3)龙胆酸甲酯与足量氢氧化钠溶液反应的化学方程式是 。(不用写反应条件)
II.已知X及其他几种有机物存在如下转化关系,且测得A中含三个甲基:
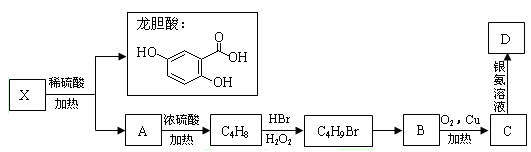
回答以下问题:
(4)X的结构简式为 ;C4H9Br的系统命名是 。
(5)写出下列反应的化学方程式(用结构简式表示),并在括号内指出反应类型:
C4H9Br→B ;( )
C→D 。 ( )
(6)写出满足下列条件的龙胆酸的一种同分异构体的结构简式 。
①能发生银镜反应 ②能使FeCl3溶液显色 ③酯类 ④苯环上的一氯代物只有两种
查看答案和解析>>
科目: 来源:2015届安徽省宿州市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列说法或表示方法中正确的是
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.由C(金刚石)→C(石墨)ΔH= -1.9KJ/mol 可知,金刚石比石墨稳定
C.在101KPa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l) ΔH=+285.8KJ/mol
D.稀溶液中:H+(aq)+OH—(aq)=H2O(l) ΔH= —53.7KJ/mol ,若将含0.5 molH2SO4的浓溶液与含1 molNaOH的溶液混合,放出的热量大于53.7KJ
查看答案和解析>>
科目: 来源:2015届安徽省宿州市高二上学期期末考试化学试卷(解析版) 题型:选择题
有A、B、C、D四种金属。将A与B用导线连接起来,浸入电解质溶液中,B不易腐蚀。将A、D分别投入等浓度盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化。如果把铜浸入C的盐溶液里,有金属C析出。据此判断它们的活动性由强到弱的顺序是
A.D>C>A>B B.D>A>B>C
C.D>B>A>C D.B>A>D>C
查看答案和解析>>
科目: 来源:2015届安徽省宿州市高二上学期期末考试化学试卷(解析版) 题型:选择题
已知蓄电池在充电时作电解池,放电时作原电池。铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“—”。关于标有“+”的接线柱,下列说法中正确的是
A.充电时作阳极,放电时作负极
B.充电时作阳极,放电时作正极
C.充电时作阴极,放电时作负极
D.充电时作阴极,放电时作正极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com