
科目: 来源:2013-2014学年辽宁省五校协作体高三上学期期中考试化学试卷(解析版) 题型:选择题
已知A、B、C均为短周期的元素,A、B同周期,A、C的最低价离子分别为A2- 和C—,B2+和C—具有相同的电子层结构,下列说法正确的是
A.离子半径:A2->C—>B2+ B.C元素的最高正价一定为+7价
C.对应气态氢化物的稳定性A>C D.还原性:A2-<C-
查看答案和解析>>
科目: 来源:2013-2014学年辽宁省五校协作体高三上学期期中考试化学试卷(解析版) 题型:选择题
CuSO4是一种重要的化工原料,其有关制备途径如图所示。下列说法不正确的是
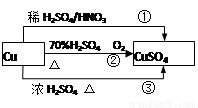
(已知:2Cu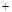 O2
O2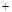 2H2SO4=2CuSO4
2H2SO4=2CuSO4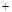 2H2O)
2H2O)
A.相对于途径①、③,途径②更好地体现了绿色化学思想
B.途径③中,1mol Cu与足量浓硫酸反应会产生64g SO2气体
C.途径①所用混酸中H2SO4与HNO3物质的量之比最好为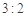
D.1mol Cu分别按照途径②、③中,被还原的H2SO4的质量之比为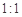
查看答案和解析>>
科目: 来源:2013-2014学年辽宁省五校协作体高三上学期期中考试化学试卷(解析版) 题型:选择题
已知:H2(g)
+I2(g)  2HI(g) ΔH = -14.9 kJ/mol。在甲、乙两个体积相同密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008 mol/L。
下列判断正确的
2HI(g) ΔH = -14.9 kJ/mol。在甲、乙两个体积相同密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008 mol/L。
下列判断正确的
|
起始浓度 |
c(H2) / mol/L |
c(I2) / mol/L |
c(HI) / mol/L |
|
甲 |
0.01 |
0.01 |
0 |
|
乙 |
0.02 |
0.02 |
0 |
A.平衡时,乙中H2的转化率是甲中的2倍
B.平衡时,甲中混合物的颜色比乙中深
C.平衡时,甲、乙中热量的变化值相等
D.该温度下,反应的平衡常数K=0.25
查看答案和解析>>
科目: 来源:2013-2014学年辽宁省五校协作体高三上学期期中考试化学试卷(解析版) 题型:选择题
已知某反应aA(g)
+bB(g)  cC(g) ΔH =Q 在密闭容器中进行,在不同温度(T1 和T2 )及压强(P1 和P2 )下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是
cC(g) ΔH =Q 在密闭容器中进行,在不同温度(T1 和T2 )及压强(P1 和P2 )下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是
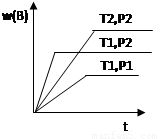
A.T1<T2, P1<P2 ,a+b>c ,Q>0
B.T1>T2 ,P1<P2 ,a+b<c ,Q<0
C.T1<T2 ,P1>P2 ,a+b<c, Q>0
D. T1<T2 ,P1>P2 ,a+b>c ,Q<0
查看答案和解析>>
科目: 来源:2013-2014学年辽宁省五校协作体高三上学期期中考试化学试卷(解析版) 题型:选择题
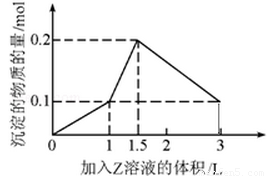
1 L某混合溶液中,溶质X、Y浓度都为0.1mol·L—1,向混合溶液中滴加0.1 mol·L—1某溶液Z,所得沉淀的物质的量如图所示,则X、Y、Z分别是
A.氯化铝、氯化镁、氢氧化钠
B.偏铝酸钠、氢氧化钡、硫酸
C.氯化铝、氯化铁、氢氧化钠
D.偏铝酸钠、氯化钡、硫酸
查看答案和解析>>
科目: 来源:2013-2014学年辽宁省五校协作体高三上学期期中考试化学试卷(解析版) 题型:选择题
如下图所示,其中甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O

下列说法正确的是
A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B.甲池通入CH3OH的电极反应为CH3OH-6e-+2H2O=CO32-+8H+
C.甲池中消耗280 mL(标准状况下)O2,此时丙池中理论上最多产生1.45g固体
D.反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度
查看答案和解析>>
科目: 来源:2013-2014学年辽宁省五校协作体高三上学期期中考试化学试卷(解析版) 题型:选择题
用4种溶液进行实验,下表中“操作及现象”与“溶液”不符的是
选项 操作及现象 溶液
A 通入SO2,溶液不变浑浊,再加氯水,变浑浊 BaCl2溶液
B 通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 Ca(ClO)2溶液
C 通入SO2,溶液变浑浊,继续通SO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊 Ca(OH)2溶液
D 通入NH4HCO3受热分解产生的气体,溶液变浑浊,继续通入该气体,浑浊消失 Ca(OH)2溶液
查看答案和解析>>
科目: 来源:2013-2014学年辽宁省五校协作体高三上学期期中考试化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率
B.含1 mol Ba(OH)2的稀溶液和含1 mol H2SO4的稀溶液反应释放热量akJ,则表示该反应中和热的热化学反应方程式为:
OH-(aq)+H+(aq)=H2O(l) ∆H = -a kJ·mol-1
C.电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小
D.对于2HI(g)  H2(g)+I2(g)平衡体系,增大平衡体系的压强可使颜色变深,符合勒夏特列原理解释。
H2(g)+I2(g)平衡体系,增大平衡体系的压强可使颜色变深,符合勒夏特列原理解释。
查看答案和解析>>
科目: 来源:2013-2014学年辽宁省五校协作体高三上学期期中考试化学试卷(解析版) 题型:填空题
如下图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X和H是固体,B和G是液体,其余均为气体, 1 mol X分解得到A、B、C各1 mol。
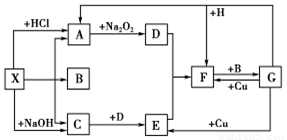
试回答下列各题:
(1)写出下列物质的化学式:X________,B________。
(2)写出下列反应的化学方程式:
①H+G―→A+F:__________________________________________________________。
②C+D―→E:__________________________________________________________。
(3)写出下列反应的离子方程式:
G+Cu―→E:___________________________________________________________。
查看答案和解析>>
科目: 来源:2013-2014学年辽宁省五校协作体高三上学期期中考试化学试卷(解析版) 题型:填空题
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%。目前,消除大气污染有多种方法。
(1)处理NOx的一种方法是利用甲烷催化还原NOx。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol—1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol—1
则甲烷直接将NO2还原为N2的热化学方程为 。
(2)降低汽车尾气的方法之一是在排气管上安装催化 转化器,发生如下反应:
2NO(g)+2CO(g) N2(g)+2CO2(g)
△H<0。
N2(g)+2CO2(g)
△H<0。
若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示,该反应的化学平衡常数为K= 。
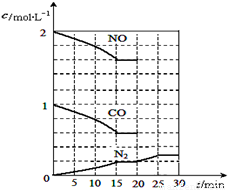
若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将 移动(填“向左”、 “向右”或“不”)。
20min时,若改变反应条件,导致N2浓度发生如上图所示的变化,则改变的条件可能是 (填序号)。
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO2的量
(3)肼(N2H4)用亚硝酸(HNO2)氧化可生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977。写出肼与亚硝酸反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com