
科目: 来源:2013-2014学年湖南省衡阳市高三上学期第三次月考化学试卷(解析版) 题型:选择题
某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图3中每个“·”代表一种元素,其中O点代表氢元素。下列说法中错误的是
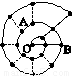
A.离O点越远的元素原子半径越大
B.虚线相连的元素处于同一族
C.B元素是图中金属性最强的元素
D.A、B组成的化合物中可能含有共价键
查看答案和解析>>
科目: 来源:2013-2014学年湖南省衡阳市高三上学期第三次月考化学试卷(解析版) 题型:选择题
X、Y、M、Z四种短周期主族元素的原子半径依次减小,X、Y、Z的电子层数之和为5,X元素原子的最外层电子数是它的电子层数的2倍,Y元素原子的最外层电子数是X和Z两元素原子最外层电子数的总和,M是地壳中含量最多的元素。下列说法不正确的是
A.化合物YZ3极易溶解于水
B.Z与M可以形成含有非极性键的化合物
C.12 g14X中含有中子的物质的量为8 mol
D.由上述四种元素组成的离子化合物受热易分解
查看答案和解析>>
科目: 来源:2013-2014学年湖南省衡阳市高三上学期第三次月考化学试卷(解析版) 题型:选择题
已知下列热化学方程式,则③中的Q3值为
Zn(s)+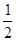 O2(g)= ZnO (s) △H= - Q1 kJ• mol-1
①
O2(g)= ZnO (s) △H= - Q1 kJ• mol-1
①
Hg(l) +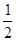 O2(g)= HgO (s) △H= -Q2 kJ• mol-1
②
O2(g)= HgO (s) △H= -Q2 kJ• mol-1
②
Zn(s) +HgO (s) = Hg(l)+ ZnO (s) △H= -Q3 kJ• mol-1 ③
A.Q2 -Q1 B.Q1 +Q2 C.Q1- Q2 D.-Q1- Q2
查看答案和解析>>
科目: 来源:2013-2014学年湖南省衡阳市高三上学期第三次月考化学试卷(解析版) 题型:选择题
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期, Z、M同主族;X+与M2—具有相同的电子层结构;离子半径:Z2—>W—;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中,正确的是
A.X、M两种元素只能形成X2M型化合物
B.由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低
C.元素Y、Z、W的单质晶体属于同种类型的晶体
D.元素W和M的某些单质可作为水处理中的消毒剂
查看答案和解析>>
科目: 来源:2013-2014学年湖南省衡阳市高三上学期第三次月考化学试卷(解析版) 题型:填空题
X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
⑴ L的元素符号为________;M在元素周期表中的位置为____________;
⑵ Z、X两元素按原子数目比2∶4构成分子则其结构式为____________。
⑶ 硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则其最高价氧化物对应的水化物化学式为_______。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下:
a.+99.7 mol·L-1 b.+29.7 mol·L-1 c.-20.6 mol·L-1 d.-241.8 kJ·mol-1
其中表示生成1 mol硒化氢反应热的是__________(填字母代号)。
查看答案和解析>>
科目: 来源:2013-2014学年湖南省衡阳市高三上学期第三次月考化学试卷(解析版) 题型:实验题
某研究小组利用下图装置探究SO2和Fe(NO3)3溶液的反应。已知:1.0 mol·L-1的Fe(NO3)3溶液的pH=1

请回答:
(1)装置A中反应的化学方程式是______________________________;
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是_______________________________;
(3)装置B中产生了白色沉淀,其成分是________;
(4)分析B中产生白色沉淀的原因:
猜想1:SO2与Fe3+、酸性条件下NO3-都反应;
猜想2:SO2与Fe3+反应;
猜想3:在酸性条件下SO2与NO3-反应;
①按猜想2,装置B中反应的离子方程式是_________,证明该猜想正确应进一步确认生成了________;
②按猜想3,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验。应选择的试剂是________(填字母)。
a.0.1 mol·L-1稀硝酸
b.1.5 mol·L-1Fe(NO3)2溶液
c.6.0 mol·L-1 NaNO3和0.2 mol·L-1盐酸等体积混合的溶液
查看答案和解析>>
科目: 来源:2013-2014学年湖南省衡阳市高三上学期第三次月考化学试卷(解析版) 题型:填空题
黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
(1)冶炼铜的反应为8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。
(2)上述冶炼过程中产生大量SO2。下列处理方案合理的是 (填代号)。
a.高空排放 b.用于制备硫酸 c.用纯碱溶液吸收制Na2SO3 d.用浓硫酸吸收
(3)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧。
据以上信息回答下列问题:
a.除去Al3+的离子方程式是 。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水。所选试剂为 。证明炉渣中含有FeO的实验现象为 。
查看答案和解析>>
科目: 来源:2013-2014学年湖南省衡阳市高三上学期第三次月考化学试卷(解析版) 题型:填空题
U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)V的单质分子的结构式为 ;XW的电子式为 ;
(2)Z元素在周期表中的位置是 ;
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式) ;
(4)写出X的单质在UW2中燃烧的化学方程式,并表示电子的转移方向和数目为 。
查看答案和解析>>
科目: 来源:2013-2014学年湖南省衡阳市高三上学期第三次月考化学试卷(解析版) 题型:填空题
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量铝粉和铁粉的混合物与一定体积某浓度的稀硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入5 mol·L-1的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量关系如图所示。则

(1)B与A的差值为________mol;
(2)原硝酸溶液中含硝酸的物质的量为________mol;
(3)铝粉和铁粉的混合物中铝粉与铁粉的物质的量之比为________;
(4)写出铝与该浓度硝酸反应的离子方程式____________。
查看答案和解析>>
科目: 来源:2013-2014学年湖南省高三11月联考化学试卷(解析版) 题型:选择题
“化学,我们的生活,我们的未来”曾经是2011年“国际化学年”的主题。你认为下列行为中,不符合这一主题的是
A.控制含磷洗涤剂的生产和使用,防止水体富营养化,保护水资源
B.研究采煤、采油新技术,尽量提高产量以满足工业生产的快速发展
C.开发太阳能、水能、风能等新能源、减少使用煤、石油等化石燃料
D.实现资源的“3R”利用,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、提高资源的循环利用(Recycle)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com