
科目: 来源:2013-2014学年湖南省高三第二次联考(10月)化学试卷(解析版) 题型:选择题
下列反应的离子方程式正确的是( )
A.氢氧化钠溶液中通入少量二氧化硫:SO2+OH-=HSO3-
B.碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O
C.盐酸滴入氨水中:H++OH-=H2O
D.碳酸钙溶解于稀硝酸中:CO32-+2H+=CO2↑+H2O
查看答案和解析>>
科目: 来源:2013-2014学年湖南省高三第二次联考(10月)化学试卷(解析版) 题型:选择题
可用下图装置制取(必要时可加热)、净化、收集的气体是( )

A.铜和稀硝酸制一氧化氮
B.亚硫酸钠与浓硫酸制二氧化硫
C.锌和稀硫酸制氢气
D.生石灰与浓氨水制氨气
查看答案和解析>>
科目: 来源:2013-2014学年湖南省高三第二次联考(10月)化学试卷(解析版) 题型:选择题
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:

下列有关叙述正确的是( )
A.贝诺酯分子中有三种含氧官能团
B.可用FeCl3 溶液区别乙酰水杨酸和对乙酰氨基酚
C.乙酰水杨酸和对乙酰氨基酚均能与NaHCO3 溶液反应
D.贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
查看答案和解析>>
科目: 来源:2013-2014学年湖南省高三第二次联考(10月)化学试卷(解析版) 题型:选择题
如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体是( )

①CO、O2②Cl2、CH4③NO2、O2④N2、H2
A.①② B.②④ C.③④ D.②③
查看答案和解析>>
科目: 来源:2013-2014学年湖南省高三第二次联考(10月)化学试卷(解析版) 题型:选择题
一定条件下,在体积为10L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g)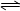 Z(g),60s达到平衡,生成0.3molZ,下列说法正确的是(
)
Z(g),60s达到平衡,生成0.3molZ,下列说法正确的是(
)
A.以X浓度变化表示的反应速率为0.001mol/(L·s)
B.将容器体积变为20L,Z的平衡浓度变为原来的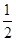
C.若增大压强,则物质Y的转化率减小
D.若升高温度,X的体积分数增大,则该反应的△H>0
查看答案和解析>>
科目: 来源:2013-2014学年湖南省高三第二次联考(10月)化学试卷(解析版) 题型:选择题
在25℃、101kPa 下:①2Na(s)+1/2O2(g)=Na2O(s) △H1=-414KJ/mol
②2Na(s)+O2(g)=Na2O2(s) △H2=-511KJ/mol
下列说法正确的是( )
A.①和②产物的阴阳离子个数比不相等
B.①和②生成等物质的量的产物,转移电子数不同
C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D.25℃、101kPa 下,Na2O2(s)+2 Na(s)= 2Na2O(s) △H=-317kJ/mol
查看答案和解析>>
科目: 来源:2013-2014学年湖南省高三第二次联考(10月)化学试卷(解析版) 题型:选择题
有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份均为100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是( )
A.K+一定存在 B.100mL溶液中含0.01mol CO32-
C.Cl-一定存在 D.Ba2+一定不存在,Mg2+可能存在
查看答案和解析>>
科目: 来源:2013-2014学年湖南省高三第二次联考(10月)化学试卷(解析版) 题型:填空题
某课外小组对一些金属单质和化合物的性质进行研究。
(1)下表为“铝与氯化铜溶液反应”实验报告的一部分:
|
实验步骤 |
实验现象 |
|
①将打磨过的铝片(过量)放入一定浓度的CuCl2溶液中。 |
产生气泡,析出疏松的红色固体,溶液逐渐变为无色。 |
|
②反应结束后分离出溶液备用。 |
|
|
③红色固体用蒸馏水洗涤后,置于潮湿空气中。 |
一段时间后固体由红色变为绿色[视其主要成分为Cu2(OH)2CO3]。 |
按实验中发生反应的现象写出下列化学方程式(是离子反应的只写离子方程式)
①析出疏松的红色固体 ;
③一段时间后固体由红色变为绿色 。
(2)用石墨作电极,电解上述实验分离出的溶液,两极产生气泡。持续电解,在阴极附近的溶液中还可观察到的现象是 。
解释此现象的离子方程式是 、 。
(3)工业上可用铝与软锰矿(主要成分为MnO2)反应来治炼金属锰。
①用铝与软锰矿冶炼锰的原理是(用化学方程式表示)
。
②MnO2在H2O2分解反应中作催化剂。若将适量MnO2加入酸化后的H2O2溶液中,MnO2溶解产生Mn2+,该反应的离子方程式是 。
查看答案和解析>>
科目: 来源:2013-2014学年湖南省高三第二次联考(10月)化学试卷(解析版) 题型:填空题
A、B、C、D、E是中学常见的几种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。
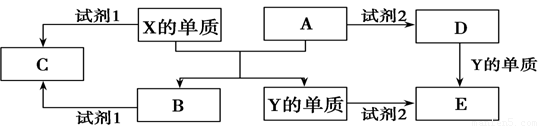
回答下列问题:
(1)X的单质与A反应的化学方程式是________________________________。
(2)若C溶液显碱性,则试剂1是 ____溶液(写化学式);若C溶液显酸性,则显酸性的原因是(用离子方程式表示) 。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是 ;
②写出D→E反应的离子方程式 ;
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠(NaNO2)为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是: 。
查看答案和解析>>
科目: 来源:2013-2014学年湖南省高三第二次联考(10月)化学试卷(解析版) 题型:实验题
二氯化二硫(S2Cl2)在工业上用于橡胶的硫化。为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品。
②有关物质的部分性质如下表:
|
物质 |
熔点/℃ |
沸点/℃ |
化学性质 |
|
S |
112.8 |
444.6 |
略 |
|
S2Cl2 |
-77 |
137 |
S2Cl2+Cl2 |
设计实验装置图如下:
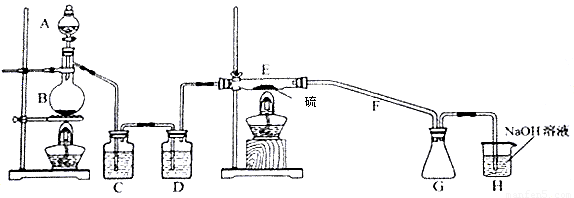
(1)上图中气体发生和尾气处理装置不够完善,请你提出改进意见 。利用改进后的正确装置进行实验,请回答下列问题:
(2)B中反应的离子方程式: 。E中反应的化学方程式: 。
(3)C中的试剂是 。
(4)仪器B的名称是 。F的作用是 。
(5)如果在加热E时温度过高,对实验结果的影响是 。
(6)S2Cl2粗品中可能混有的杂质是(填写两种) ,为了提高S2Cl2的纯度,关键的操作是控制好温度和 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com