
科目: 来源:2013-2014学年湖北省咸宁市高三上学期期末考试理综化学试卷(解析版) 题型:选择题
对下列物质中的杂质(括号内为杂质)的检验、除杂所使用的试剂均正确的是( )
选项 物质及杂质 检验 除杂
A 乙酸乙酯(乙酸) Na2CO3溶液 NaOH溶液
B NaHCO3溶液(Na2CO3) Ca(OH)2溶液 过量CO2
C CO2(HCl) AgNO3溶液(含稀硝酸) 饱和NaHCO3溶液
D CO(NO2) 观察颜色或湿润的淀粉KI试纸 水
查看答案和解析>>
科目: 来源:2013-2014学年湖北省咸宁市高三上学期期末考试理综化学试卷(解析版) 题型:选择题
分子式为C5H12O且可与钠反应放出氢气的有机化合物共有(不考虑立体异构)( )
A.6种 B.7种 C.8种 D.9种
查看答案和解析>>
科目: 来源:2013-2014学年湖北省咸宁市高三上学期期末考试理综化学试卷(解析版) 题型:填空题
甲醇汽油是由10%一25%的甲醇与其他化工原料、添加剂合成的新型车用燃料,可达到国标汽油的性能和指标。甲醇是一种可再生能源,具有广泛的开发和应用前景。
Ⅰ、工业上合成甲醇一般采用下列反应:CO(g)+2 H2(g) CH3 OH(g) △H=a
kJ/mol,
CH3 OH(g) △H=a
kJ/mol,
下表是该反应在不同温度下的化学平衡常数(K):
|
温度/0C |
250 |
310 |
350 |
|
K |
2.041 |
0.250 |
0.012 |
(1)由表中数据判断△H a 0(填“>”、“=”或“<”)。
(2)某温度下,将2 mol CO和6 mol H2充入2 L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.5 mol·L-1,则此时的温度为 0C。
(3)在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
|
浓度mol/L 时间/min |
c(CO) |
c(H2) |
c(CH3OH)
|
|
0 |
0.8 |
1.6 |
0 |
|
2 |
0.6 |
1.2 |
0.2 |
|
4 |
0.3 |
0.6 |
0.5 |
|
6 |
0.3 |
0.6 |
0.5 |
①反应从2 min到4 min之间,H2的反应速率为 。
②反应达到平衡时CO的转化率为 。
③反应在第2 min时改变了反应条件,改变的条件可能是 (填序号)。
A.使用催化剂 B.降低温度 C.增加H2的浓度
(4)向容积相同、温度分别为T1和T2的两个密闭容器中均充入1 molCO和2 mol H2,发生反应CO(g)+2 H2(g)  CH3 OH(g)△H=a kJ/mol。恒温恒容下反应相同时间后,分别测得体系中CO的百分含量分别为w1和w2;已知T1<T2,则
CH3 OH(g)△H=a kJ/mol。恒温恒容下反应相同时间后,分别测得体系中CO的百分含量分别为w1和w2;已知T1<T2,则
w1 w2(填序号)。
A.大于 B.小于 C.等于 D.以上都有可能
Ⅱ、甲醇在化学电源方面也有着重要应用。写出以甲醇为燃料,氢氧化钠溶液为电解质溶液的原电池中负极的电极反应式: 。
查看答案和解析>>
科目: 来源:2013-2014学年湖北省咸宁市高三上学期期末考试理综化学试卷(解析版) 题型:实验题
高锰酸钾是一种典型的强氧化剂,无论在实验室还是在化工生产中都有重要的应用。
下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。
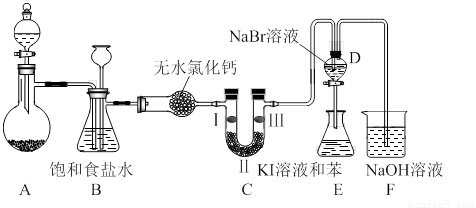
(1)制备氯气选用的药品为:高锰酸钾和浓盐酸,相应的离子方程式为: 。
(2)装置B的作用是 ,监测实验进行时C中可能发生堵塞,请写出发生堵塞时B中的现象 。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入 。(选a或b或c)
|
|
a |
b |
c |
|
I |
干燥的有色布条 |
湿润的有色布条 |
湿润的有色布条 |
|
II |
碱石灰 |
浓硫酸 |
无水氯化钙 |
|
III |
湿润的有色布条 |
干燥的有色布条 |
干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。当向D中缓缓通入足量氯气时,可以看到无色溶液逐渐变为红棕色,说明氯的非金属性大于溴。打开活塞,将D中的少量溶液加入E中,振荡E。观察到的现象是 。该现象 (填“能”或“不能”)说明溴的非金属性强于碘,原因是 。
查看答案和解析>>
科目: 来源:2013-2014学年湖北省咸宁市高三上学期期末考试理综化学试卷(解析版) 题型:填空题
高铁酸盐在能源、环保等方面有着广泛的用途。湿法、干法制备高铁酸盐的原理如下表所示。
(1)工业上用湿法制备高铁酸钾(K2FeO4)的流程如下图所示:
|

①洗涤粗品时选用异丙醇而不用水的理由是: 。
②反应I的化学方程式为 。
③反应II的离子方程式为 。
④已知25℃时Fe(OH)3的Ksp = 4.0×10-38,反应II后的溶液中c(Fe3+)=4.0×10-5 mol/L,则需要调整pH= 时,开始生成Fe(OH)3(不考虑溶液体积的变化)。
(2)由流程图可见,湿法制备高铁酸钾时,需先制得高铁酸钠,然后再向高铁酸钠中加入饱和KOH溶液,即可析出高铁酸钾。
①加入饱和KOH溶液的目的是: 。
②由以上信息可知:高铁酸钾的溶解度比高铁酸钠 (填“大”或“小”)。
|
湿法 |
强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
|
干法 |
Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
(3)干法制备K2FeO4的反应中氧化剂与还原剂的物质的量之比为 。
查看答案和解析>>
科目: 来源:2013-2014学年湖北省咸宁市高三上学期期末考试理综化学试卷(解析版) 题型:实验题
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
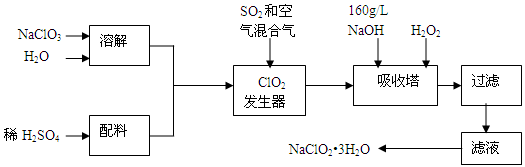
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③160 g/L NaOH溶液是指160 g NaOH固体溶于水所得溶液的体积为1L。
(1)160 g/L NaOH溶液的物质的量浓度为 。若要计算该溶液的质量分数,还需要的一个条件是 (用文字说明)。
(2)发生器中鼓入空气的作用可能是 (选填序号)。
a.将SO2氧化成SO3,增强酸性; b.稀释ClO2以防止爆炸;
c.将NaClO3氧化成ClO2
(3)吸收塔内反应的离子方程式为 。
吸收塔的温度不能超过20℃,其目的是 。
(4)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是 。
(5)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是 (选填序号)。
a.Na2O2 b.Na2S c.FeCl2
(6)从滤液中得到NaClO2•3H2O粗晶体的实验操作依次是 (选填序号)。
a.蒸馏 b.蒸发浓缩 c.灼烧 d.过滤洗涤 e.冷却结晶
要得到更纯的NaClO2•3H2O晶体必须进行的操作是 (填操作名称)。
查看答案和解析>>
科目: 来源:2013-2014学年湖北省咸宁市高三上学期期末考试理综化学试卷(解析版) 题型:填空题
材料是人类赖以生存的重要物质基础。铜、镍等金属材料在现代社会中有着重要应用。请回答下列问题:
(1)铜在元素周期表中的位置为 ,镍的基态电子排布式为 。
(2)在配离子[Ni(NH3)4]2+中,配体中N元素与它相邻的C和O元素的第一电离能由大到小的顺序为 ,这三种元素电负性由大到小的顺序为 ;配体NH3中N原子的杂化方式为 。
(3)据报道,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的结构可看作由镁原子和镍原子在一起进行面心立方最密堆积,如图,晶体中每个镁原子周围距离最近的镍原子有 个,若已知晶胞的边长为a pm,阿伏伽德罗常数为NA,则该晶体的密度的数学表达式为 g•cm-3(用a和NA表示,只列式,可不用化简)。
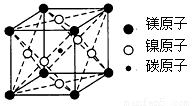
查看答案和解析>>
科目: 来源:2013-2014学年湖北省咸宁市高三上学期期末考试理综化学试卷(解析版) 题型:填空题
苯酚是重要的化工原料,通过下列流程可合成阿司匹林、香料和一些高分子化合物。
已知: 乙酸酐用AS表示,其结构式为


(1)C中含有官能团的名称为 。
(2)写出反应⑦的化学方程式 。
(3)写出G的结构简式 。
(4)写出反应类型:① ④ 。
(5)下列可检验阿司匹林样品中混有水杨酸的试剂是 。
A. 三氯化铁溶液 B. 碳酸氢钠溶液 C.石蕊试液
(6)任意写出一种符合下列条件的B的同分异构体
(a)苯环上只有两个取代基
(b)能发生银镜反应
(c)苯环上的一溴代物有两种
(d)加入NaHCO3溶液能产生使澄清石灰水变浑浊的气体
查看答案和解析>>
科目: 来源:2013-2014学年湖北省孝感市三年级第一次统一考试化学试卷(解析版) 题型:选择题
化学与科学、技术、社会、环境密切相关。下列有关说法中正确的是
A.糖类、蛋白质、油脂都属于天然高分子化合物
B.煤经气化、液化和干馏三个物理变化过程,可变为清洁能源
C.乙醇、过氧化氢、次氯酸钠等消毒液均可以将病毒氧化而达到消毒的目的
D.使用含有氯化钠的融雪剂会加快桥梁的腐蚀
查看答案和解析>>
科目: 来源:2013-2014学年湖北省孝感市三年级第一次统一考试化学试卷(解析版) 题型:选择题
X、Y、Z、W、R是原子序数依次增大的五种短周期元素,化合物XZ、Y2W能破坏水的电离平衡,XR能抑制水的电离,则Y元素为
A.Li B.F C.Na D.S
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com