
科目: 来源:2013-2014学年河北衡水中学高三上学期期中考试化学试卷(解析版) 题型:填空题
下表为元素周期表的一部分,其中编号代表对应的元素。
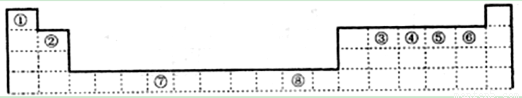
请回答下列问题:
(1)写出元素⑦的基态原子外围电子排布式 ,元素⑧位于 区。
⑤元素原子的价层电子的轨道表示式为 ,
(2)若元素①③⑤形成的某化合物显酸性,经测定这三种元素的质量比为1:6:16,该化合物对氢气的相对密度为23,则其中所有杂化原子的杂化方式分别为 和 。
(3)元素③④⑤⑥的第一电离能由大到小的顺序是 (用元素符号表示)。请写出由④和⑤两种元素形成的与N3ˉ互为等电子体的分子的化学式 ,
(写出一种即可)其VSEPR构型为 。
查看答案和解析>>
科目: 来源:2013-2014学年河北衡水中学高三上学期期中考试化学试卷(解析版) 题型:填空题
(一)、某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5um的悬浮颗粒物)其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)对PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
|
离子 |
K+ |
Na+ |
NH4+ |
SO42- |
NO3- |
Cl- |
|
浓度/mol.L |
4x10ˉ6 |
6x 10ˉ6 |
2x10ˉ5 |
4x10ˉ5 |
3x10ˉ5 |
2x10ˉ5 |
根据表中数据判断PM2.5为 , (填“酸性”、“中性”或“碱性”)
(2)为减少SO2的排放,常采取的措施有:将煤转化为清洁气体燃料。已知:
H2(g)+1/2O2(g)=H2O(g)
 H= -241.8KJ/mol C(s)+1/2O2(g)=CO(g)
H= -241.8KJ/mol C(s)+1/2O2(g)=CO(g)
 H= -110.5KJ/mol
H= -110.5KJ/mol
写出焦炭与水蒸气反应的热化学方程式
(3)洗涤含SO2的烟气,以下物质可作洗涤剂的是 (填编号)
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(二)A、B、C、D、E五种短周期元素(A、B、C、D、E分别代表元素符号),它们的原子序数依次增大;A是元素周期表中原子半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐X;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的=3/4倍;C与E同主族。
请回答下列问题:
(1)X的化学式______
(2)下列各项中,能说明元素C比E非金属性强的事实有______(填序号)。
①氢化物H2E的酸性比H2C强
②氢化物H2C的热稳定性比H2E强
③氢化物H2E的水溶液放置在空气中会变浑浊
④C与E组成化合物,C显负价
(3) 将由BC和BC2组成的混合气体通入下图所示装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强。

已知(ⅰ)浓硝酸能将气体BC氧化成BC2,而稀硝酸不能氧化BC。
(ⅱ)NaOH溶液与BC2反应的化学方程式为:
2NaOH+2BC2=NaBC2+NaBC+H2O
NaOH溶液与BC气体不反应装置②、③中盛放的药品依次是______、______。
(4)通入混合气体之前,应先通入一段时间某另外一种气体,试推测先通入的该气体可以是______(填一种气体的化学式)。
查看答案和解析>>
科目: 来源:2013-2014学年河北衡水中学高三上学期期中考试化学试卷(解析版) 题型:填空题
许多含氯物质与生活密切相关,如HC10、C102、NaClO2等都是重要的杀菌消毒剂和漂白剂。下列是重要的含氯漂白剂NaClO2的工业合成流程图。

已知:纯ClO2易发生爆炸。请回答下列问题:
(1) 在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是____________。
(2)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中,除用H2O2外,还可以选择的还原剂是______(填代号)。
a.Na2O2 b.Na2S c.FeCl2 d.铁粉
(3)NaClO2溶液与FeCl2溶液相遇,有大量红褐色沉淀产生,该反应的离子方程式为______
(4)为了测定NaClO2 • 3H2O的纯度,取上述合成产品10 g溶于水配成500 mL溶液,取出10 mL溶液于锥形瓶中,再加人足量酸化的KI溶液,充分反应后加人2 ~3滴淀粉溶液,用0.264
mol/L Na2S2O3标准液滴定,锥形瓶中溶液______(填颜色变化),且半分钟内不发生变化,说明滴定达终点,用去标准液20.OOmL,试样纯度是否合格______(填“合格”或“不合格”,合格纯度在90%以上)。提示: 。
。
查看答案和解析>>
科目: 来源:2013-2014学年河南省原名校高三上学期期联考化学试卷(解析版) 题型:选择题
下列有关说法中,不正确的是( )
A.“光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关
B.根据分散质微粒直径大小可以将分散系分为溶液、胶体和浊液
C.可用于制造光导纤维,其性质稳定,不溶于强酸、强碱
D.焰火的五彩缤纷是某些金属元素性质的展现
查看答案和解析>>
科目: 来源:2013-2014学年河南省原名校高三上学期期联考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,则下列说法正确的是( )
A.常温下,0.1 mol碳酸钠晶体中含有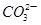 的数目小于0.1 NA
的数目小于0.1 NA
B.36gCaO2中含有的离子数目为0.15 NA
C.100 g 98%的浓硫酸中,氧原子总数为4NA
D.标准状况下,14.2 g氯气与足量石灰乳充分反应转移电子数为0.2NA
查看答案和解析>>
科目: 来源:2013-2014学年河南省原名校高三上学期期联考化学试卷(解析版) 题型:选择题
下列说法在一定条件下可以实现的是( )
①酸性氧化物与碱发生反应
②弱酸与盐溶液反应可以生成强酸
③没有水生成,也没有沉淀和气体生成的复分解反应
④两种酸充分反应后溶液体系为中性
⑤有单质参加的非氧化还原反应
⑥两种氧化物反应有气体生成
A.①②③④⑤⑥ B.除⑥外 C.除④外 D.除②外
查看答案和解析>>
科目: 来源:2013-2014学年河南省原名校高三上学期期联考化学试卷(解析版) 题型:选择题
一定条件下,下列物质均可通过化合反应制得的有( )种
①小苏打 ②硫酸铝 ③氯化亚铁 ④磁性氧化铁 ⑤氢氧化铜 ⑥氢氧化铁
A.3 B.4 C.5 D.6
查看答案和解析>>
科目: 来源:2013-2014学年河南省原名校高三上学期期联考化学试卷(解析版) 题型:选择题
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列条件下关于离子存在的说法中正确的是( )
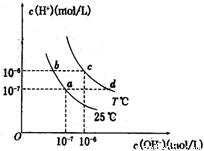
A.c点对应的溶液中大量存在:Na+、Ba2+、Cl-、Fe2+
B.b点对应的溶液中大量存在: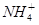 、K+、Cl-、
、K+、Cl-、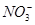
C.d点对应的溶液中大量存在:Al3+、K+、ClO-、Cl-
D.a点对应的溶液中大量存在: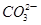 、Na+、Cl-、
、Na+、Cl-、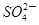
查看答案和解析>>
科目: 来源:2013-2014学年河南省原名校高三上学期期联考化学试卷(解析版) 题型:选择题
描述或解释下列现象的离子方程式,不正确的是( )
A.氢氧化钠溶液中滴入紫色石蕊试液,再通入CO2,溶液有蓝变红:CO2+2OH-= +H2O
+H2O
B.漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3ClO-+3H2O=Fe(OH)3↓+3HClO
C.Cl2通入FeBr2溶液中,Cl2与FeBr2物质的量之比4︰5:10Fe2++6Br-+8Cl2=10Fe3++3Br2+16Cl-
D.碳酸氢铵溶液中加足量澄清石灰水: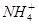 +
+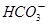 +Ca2++2OH-=CaCO3↓+NH3·H2O+H2O
+Ca2++2OH-=CaCO3↓+NH3·H2O+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com