
科目: 来源: 题型:单选题
| 物质的检验、制备和用途及实验现象 | 解释 | |
| ① | 在一定浓度的乙酸溶液中加入少量乙酸钠固体,溶液pH增大 | 完全是由于乙酸根水解所致 |
② | 向少量未知溶液中滴加氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
③ | 常温下可用铁或铝制容器来盛装浓硫酸或浓硝酸 | 铁、铝表面发生了钝化现象 |
④ | 向饱和NaCl溶液中通入足量的NH3和CO2,有NaHCO3固体析出 | NaHCO3是难溶于水的盐 |
查看答案和解析>>
科目: 来源: 题型:多选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
查看答案和解析>>
科目: 来源: 题型:单选题
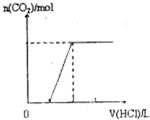
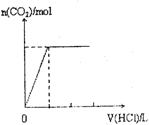
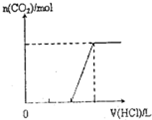
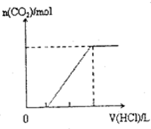
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 3Fe+4CO2,若有1.5mol Fe3O4参加反应,转移电子的物质的量是______.
3Fe+4CO2,若有1.5mol Fe3O4参加反应,转移电子的物质的量是______.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com