
科目: 来源:2013-2014学年广东省惠州市高三第三次调研考试化学试卷(解析版) 题型:填空题
100℃时,在1L恒温恒容的密闭容器中,通入0.1
mol N2O4,发生反应:N2O4(g)
 2NO2(g);△H= +57.0 kJ·mol-1,NO2和N2O4的浓度如图甲所示。NO2和N2O4的消耗速率与其浓度的关系如乙图所示,
2NO2(g);△H= +57.0 kJ·mol-1,NO2和N2O4的浓度如图甲所示。NO2和N2O4的消耗速率与其浓度的关系如乙图所示,
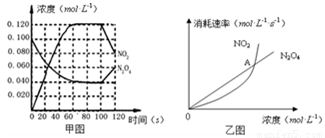
(1)在0~60s内,以N2O4表示的平均反应速率为 mol·L-1·s-1 。
(2)根据甲图中有关数据,计算100℃时该反应的平衡常数K1= =0.36mol.L-1.S-1
若其他条件不变,升高温度至120℃,达到新平衡的常数是k2 ,则k1 k2 (填“>”、“<”或“=”)。(3)反应进行到100s时,若有一项条件发生变化,变化的条件可能是 。
A.降低温度 B.通入氦气使其压强增大 C.又往容器中充入N2O4 D.增加容器体积
(4)乙图中, 交点A表示该反应的所处的状态为 。
A.平衡状态 B.朝正反应方向移动 C.朝逆反应方向移动 D.无法判断
(5)已知N2(g)+2O2(g)=2NO2(g) △H= +67.2 kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H= -534.7 kJ·mol-1
N2O4(g)  2NO2(g)
△H= +57.0 kJ·mol-1
2NO2(g)
△H= +57.0 kJ·mol-1
则2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) △H= kJ·mol-1
查看答案和解析>>
科目: 来源:2013-2014学年广东省惠州市高三第三次调研考试化学试卷(解析版) 题型:填空题
硫酸亚锡(SnSO4)可用于镀锡工业.某小组设计SnSO4制备路线为:

查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化.
Ⅱ.SnCl2易水解生成碱式氯化亚锡
(1)锡原子的核电荷数为50,与碳元素同处ⅣA族,锡位于周期表的第 周期(1分)
(2)操作Ⅰ是 过滤、洗涤等(2分)
(3)溶解SnCl2粉末需加浓盐酸,原因是
(4)加入Sn粉的作用有两个:①调节溶液pH ②
(5)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是
(6)酸性条件下,SnSO4与双氧水去反应的离子方程式是
(7)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn+2HCl═SnCl2+H2↑;
②加入过量的FeCl3;
③用已知浓度的K2Cr2O7滴定②生成的Fe2+,再计算锡粉的纯度,请配平方程式:
FeCl2 + K2Cr2O7
+ HCl = FeCl3
+ KCl + CrCl2+

查看答案和解析>>
科目: 来源:2013-2014学年广东省惠州市高三第三次调研考试化学试卷(解析版) 题型:实验题
Na2SO3在空气中易被氧化而变质。某同学为证明Na2SO3有还原性,从一瓶实验室长期存放的Na2SO3固体中取出少量溶于水,滴入一定量的烧碱溶液和少许溴水,振荡后溶液变为无色。
(1)在碱性溶液中Br2和Na2SO3反应的离子方程式 。
(2)反应后的溶液含有SO32-、SO42-、Br-、OH-等阴离子,下表是某同学鉴定其中SO32-、SO42-和Br-的实验报告,请完成未填完的部分。
限选试剂:2 mol·L-1HCl;1 mol·L-1 H2SO4;l mol·L-1BaCl2;l mol·L-1Ba(NO3)2;1 mol·L-1 KMnO4、CCl4;新制饱和氯水;品红溶液。
|
编号 |
实验操作 |
预期现象和结论 |
|
步骤①
|
取少量待测液加入试管中,加入过量2mol·L-1HCl,再滴加适量1 mol·L-1BaCl2 溶液。 |
有白色沉淀生成,证明待测液中含有、SO42- 。 |
|
步骤②
|
|
|
|
步骤③
|
|
|
(3)为了测定上述样品的纯度,现取10.0克试样配成250ml溶液。取出25.00ml所配溶液,用0.10mol/L的酸性KMnO4溶液滴定至终点。反应离子方程式为:
重复操作三次,每次消耗0.10mol/L KMnO4溶液体积分别为20.02 ml、 20.00 ml和19.98 ml。(相对原子质量Na 23 S 32 O 16)
①计算样品中Na2SO3的质量分数为 。(结果保留3位有效数字)
②操作时,若未用0.10mol/L的酸性KMnO4溶液润洗滴定管,会导致测定结果 。(填“偏高”、“偏低”或“没有影响”)
查看答案和解析>>
科目: 来源:2013-2014学年广东省高三上学期期中考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.20983Bi 和 21083Bi的核外电子数不同
B.NH3的电子式为: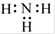
C.全部由非金属元素组成的化合物可能含离子键
D.离子化合物不可能含共价键
查看答案和解析>>
科目: 来源:2013-2014学年广东省高三上学期期中考试理综化学试卷(解析版) 题型:选择题
心脏起搏器电源—锂碘电池的电池反应为:2 Li(s) + I2 (s) = 2 LiI(s) ΔH
已知:4 Li(s) + O2 (g) = 2 Li2O(s) ΔH1
4 LiI(s) + O2 (g) = 2 I2 (s) + 2 Li2O(s) ΔH2 则下列说法正确的是( )
A.ΔH=1/2ΔH1 - ΔH2 B.ΔH=1/2ΔH1 + ΔH2
C.ΔH=1/2ΔH1 - 1/2ΔH2 D.ΔH=1/2ΔH1 +1/2ΔH2
查看答案和解析>>
科目: 来源:2013-2014学年广东省高三上学期期中考试理综化学试卷(解析版) 题型:选择题
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中Z的一种氧化物能使品红溶液褪色,则下列说法正确的是( )

A.非金属性:R<T<Q B.T与Q的电子数相差18
C.原子半径:R< T< Z D.X的氧化物既能与盐酸反应又能与氢氧化钠溶液反应
查看答案和解析>>
科目: 来源:2013-2014学年广东省高三上学期期中考试理综化学试卷(解析版) 题型:选择题
在水溶液中能大量共存的一组离子是( )
A.Na+ Cl- NO3- H+ B.Na+ Cu2+ Cl- S2-
C.K+ SO32- Fe3+ NO3- D.K+ NH4+ SiO32- SO42-
查看答案和解析>>
科目: 来源:2013-2014学年广东省高三上学期期中考试理综化学试卷(解析版) 题型:选择题
某反应的反应过程中能量变化如图所示(图中E表示活化能)。下列叙述正确的是( )
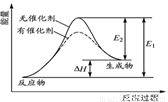
A.逆反应的活化能大于正反应的活化能
B.该反应为放热反应
C.催化剂能改变反应的焓变
D.催化剂能降低反应的活化能
查看答案和解析>>
科目: 来源:2013-2014学年广东省高三上学期期中考试理综化学试卷(解析版) 题型:选择题
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
叙述I 叙述II
A 水玻璃具有黏性 盛装烧碱溶液的试剂瓶不能用玻璃塞
B 往氯化钙溶液中通入足量的CO2
先有白色沉淀生成,后沉淀溶解 CaCO3不溶于水,Ca(HCO3)2可溶于水
C NH4Cl受热易分解 可用加热法除去I2中的NH4Cl
D 利用丁达尔现象区分氢氧化铁胶体和浓的氯化铁溶液 往氢氧化钠溶液中滴加饱和氯化铁溶液,加热至红褐色制得胶体
查看答案和解析>>
科目: 来源:2013-2014学年广东省高三上学期期中考试理综化学试卷(解析版) 题型:选择题
设nA为阿伏加德罗常数的数值,下列说法错误的是(H:1 O:16) ( )
A.常温下,1.8g H2O含有0.2nA个H-O 共价键
B.1L 0.3 mol·L-1的FeCl3溶液中Fe3+数目为0.3nA
C.标准状况下,22.4 L CCl4中含 nA个CCl4分子
D.标准状况下,22.4 L NO2和CO2的混合气体含有2nA个氧原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com