
科目: 来源:2013-2014学年四川省绵阳市高三第二次诊断性考试理综化学试卷(解析版) 题型:选择题
下列实验操作能达到目的的是
A.除去苯中混有的少量苯酚:加入适量NaOH溶液,振荡、静置后分液
B.除去乙酸乙酯中混有的少量乙酸:加入NaOH溶液并加热,振荡、静置后分液
C.检验卤代烃中的卤原子:取少量液体与NaOH溶液共热后滴加AgNO3溶液
D.检验FeCl3溶液中是否含有Fe2+:取少量溶液先滴加氯水,再滴加KSCN溶液
查看答案和解析>>
科目: 来源:2013-2014学年四川省绵阳市高三第二次诊断性考试理综化学试卷(解析版) 题型:选择题
25℃时,水溶液中c(H+)与c(OH-)的变化关系如图中曲线a c所示,下列判断错误的是
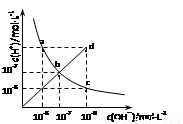
A.a c曲线上的任意一点都有c(H+)·c(OH-)=10-14
B.b d线段上任意一点对应的溶液都呈中性
C.d点对应溶液的温度高于25℃,pH<7
D.CH3COONa溶液不可能位于c点
查看答案和解析>>
科目: 来源:2013-2014学年四川省绵阳市高三第二次诊断性考试理综化学试卷(解析版) 题型:选择题
汽车上的催化转化器可将尾气中的主要污染物转化成无毒物质,反应为:
2NO(g)+2CO(g) N2(g)+2CO2(g) DH=-a kJ/mol(a>0)
N2(g)+2CO2(g) DH=-a kJ/mol(a>0)
在某温度时,用气体传感器测得不同时间的NO和CO浓度如下表:
|
时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
|
c(NO)/10-4 mol·L-1 |
10.0 |
4.05 |
2.50 |
1.60 |
1.00 |
1.00 |
|
c(CO)/10-3 mol·L-1 |
3.60 |
3.05 |
2.85 |
2.76 |
2.70 |
2.70 |
经分析,得出结论不正确的是
A.2~3 s间的平均反应速率v(NO)=9×10-5 mol/(L·s)
B.催化转化器对废气的转化速率在夏季时比冬季时高
C.若该催化转化器气舱容积为2 L,则达到平衡时反应放出热量1.8a J
D.该温度下,此反应的平衡常数K=5000
查看答案和解析>>
科目: 来源:2013-2014学年四川省绵阳市高三第二次诊断性考试理综化学试卷(解析版) 题型:选择题
将11.9 g Mg、Al、Fe组成的合金溶于足量NaOH溶液中,产生的气体在标准状况下体积为3.36 L。另取等质量合金溶于过量稀硝酸中,生成NO气体,向反应后的溶液中加入过量NaOH溶液,得到沉淀19.4 g,则上述反应中生成NO气体的体积为(标准状况下)
A.6.72 L B.11.2 L C.22.4 L D.4.48 L
查看答案和解析>>
科目: 来源:2013-2014学年四川省绵阳市高三第二次诊断性考试理综化学试卷(解析版) 题型:填空题
X、Y、Z、D、E、G六种短周期元素的原子序数依次递增。X、Y、D元素的基态原子中电子层数与未成对电子数均相等;D、E属于同族元素,G的单质和ED2化合物均具有漂白性;R元素的M层全满,N层只有1个电子。
请回答下列问题:(用对应的元素符号表示)
(1)R元素在元素周期表分区中属于______区元素,Y、Z、D三种元素中电负性由小到大的顺序是_________。
(2)X3D+的中心原子杂化轨道类型是__________,该离子的立体构型是 。
(3)向RED4的水溶液中加入ZX3的水溶液至过量,有关反应的离子方程式是 。
(4)向RG2的水溶液通入ED2,产生白色沉淀RG,该反应的离子方程式是 。
查看答案和解析>>
科目: 来源:2013-2014学年四川省绵阳市高三第二次诊断性考试理综化学试卷(解析版) 题型:实验题
单晶硅是信息产业中重要的基础材料。工业上可用焦炭与二氧化硅的混合物在高温下与氯气反应生成SiCl4和CO,SiCl4经提纯后用氢气还原得高纯硅。以下是实验室制备SiCl4的装置示意图。

实验过程中,石英砂中的铁、铝等杂质也能转化为相应氯化物,SiCl4、AlCl3、FeCl3遇水均易水解 ,有关物质的物理常数见下表:
,有关物质的物理常数见下表:
|
物质 |
SiCl4 |
AlCl3 |
FeCl3 |
|
沸点/℃ |
57.7 |
- |
315 |
|
熔点/℃ |
-70.0 |
- |
- |
|
升华温度/℃ |
- |
180 |
300 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式:_____________, 装置D的硬质玻璃管中发生反应的化学方程式是 。
 (2)装置C中的试剂是
; D、E间导管短且粗的原因是
。
(2)装置C中的试剂是
; D、E间导管短且粗的原因是
。
 (3)G中吸收尾气一段时间后,吸收液中肯定存在OH-、Cl-和SO42-。请设计实验,探究该吸收液中可能存在的其他酸根离子(忽略空气中CO2的影响)。
(3)G中吸收尾气一段时间后,吸收液中肯定存在OH-、Cl-和SO42-。请设计实验,探究该吸收液中可能存在的其他酸根离子(忽略空气中CO2的影响)。
【提出假设】假设1:只有SO32-;假设2:既无SO32-也无ClO-;假设3: 。
【设计方案,进行实验】可供选择的实验试剂有:3 mol/L H2SO4、1 mol/L NaOH、0.01 mol/L KMnO4、溴水、淀粉-KI、品红等溶液。
取少量吸收液于试管中,滴加3 mol/L H2SO4至溶液呈酸性,然后将所得溶液分置于a、b、c三支试管中,分别进行下列实验。请完成下表:
|
序号 |
操 作 |
可能出现的现象 |
结论 |
|
① |
向a试管中滴加几滴 溶液 |
若溶液褪色 |
则假设1成立 |
|
若溶液不褪色 |
则假设2或3成立 |
||
|
② |
向b试管中滴加几滴 溶液 |
若溶液褪色 |
则假设1或3成立 |
|
若溶液不褪色 |
假设2成立 |
||
|
③ |
向c试管中滴加几滴 溶液 |
|
假设3成立 |
查看答案和解析>>
科目: 来源:2013-2014学年四川省绵阳市高三第二次诊断性考试理综化学试卷(解析版) 题型:填空题
有机物G是制备液晶材料的中间体之一,其结构简式为:
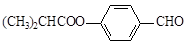 G的一种合成路线如下:
G的一种合成路线如下:
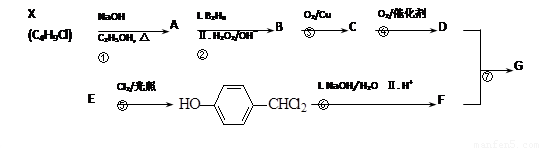
其中,A~F分别代表一种有机化合物,合成路线中的部分产物及反应条件已略去。
已知:X的核磁共振氢谱只有1种峰;RCH=CH2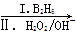 RCH2CH2OH;通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。请回答下列问题:
RCH2CH2OH;通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。请回答下列问题:
(1)A的结构简式是 ;C中官能团的名称是 。
(2)B的名称是 。第①~⑦步中属于取代反应的有 (填步骤编号)。
(3)写出反应⑤的化学方程式: 。
(4)第⑦步反应的化学方程式是 。
(5)G经催化氧化得到Y(C11H12O4),写出同时满足下列条件的Y的所有同分异构体的结构简式 。
a.苯环上的一氯代物有2种;b.水解生成二元羧酸和醇。
查看答案和解析>>
科目: 来源:2013-2014学年四川省绵阳市高三第二次诊断性考试理综化学试卷(解析版) 题型:填空题
工业制钛白粉产生的废液中含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4,可利用酸解法生产补血剂乳酸亚铁。其生产流程如下:
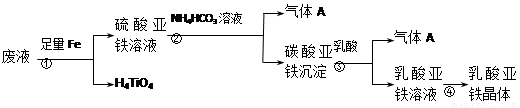
已知:TiOSO4可溶于水,在水中电离为TiO2+和SO42-。请回答下列问题:
(1)写出TiOSO4水解生成钛酸H4TiO4的离子方程式 。步骤①中加入足量铁屑的目的是 。
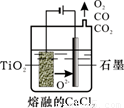
(2)工业上由H4TiO4可制得钛白粉TiO2。TiO2直接电解还原法(剑桥法)生产钛 是一种较先进的方法,电解质为熔融的CaCl2,原理如图所示,阴极的电极反应为_______________。
(3)步骤②的离子方程式是 ,所得副产品主要 是__________(填化学式)。
(4)步骤④的结晶过程中必须控制一定的真空度,原因是 。
(5)乳酸可由乙烯经下列步骤合成:
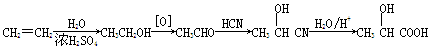
上述合成路线的总产率为60%,乳酸与碳酸亚铁反应转化为乳酸亚铁晶体的产率为90%,则生产468 kg乳酸亚铁晶体(M=234 g/mol)需要标准状况下的乙烯 m3。
查看答案和解析>>
科目: 来源:2013-2014学年四川省资阳市高三第二次诊断考试理综化学试卷(解析版) 题型:选择题
《环境研究通讯》刊文称:全世界每年因空气污染而死亡的人数约为210万。原因是大气中可吸入颗粒物(PM 2.5)浓度上升导致呼吸系统疾病。下列关于PM 2.5的说法不正确的是
A.PM 2.5是指大气中直径小于或等于2.5 um(10-6 m)的颗粒物,因此均能形成胶体
B.研制开发燃料电池汽车,降低机动车尾气排放,可以减少PM 2.5污染
C.PM 2.5专用口罩中使用了活性炭,是利用了活性炭的吸附性
D.工厂利用胶体电泳性质采用静电除尘工艺,可部分降低细颗粒物造成的污染
查看答案和解析>>
科目: 来源:2013-2014学年四川省资阳市高三第二次诊断考试理综化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列说法正确的是
A.密封保存的46 g NO2气体含有的分子数为NA
B.0.1 mol/L 碳酸钠溶液中阴离子总数大于0.1 NA
C.标准状况下,22.4 L HF中含有的氟原子数目为NA
D.常温常压下,7.1 g Cl2与足量的Fe充分反应,转移的电子数目为0.2 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com