
科目: 来源:2013-2014学年四川省高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
下述实验能达到预期目的的是
实验内容 实验目的
A 向1mL0.2mol/LNaOH溶液中滴入2滴0.1mol/LMgCl2 溶液,产生白色沉淀后,再滴加2滴0.1mol/LFeCl3溶液,又生成红褐色沉淀 证明在相同条件下,溶解度Mg(OH)2>Fe(OH)3
B 向混有BaCO3沉淀的NaOH溶液中滴入已知浓度的盐酸(用酚酞作指示剂) 滴定其中NaOH含量
C 两种一元碱溶液X和Y(X的pH比Y大l),分别加水稀释l00倍后,pH相等 证明稀释前c(X)=10c(Y)
D 测定等物质的量浓度的HF与HCl溶液的pH,后者较小 证明非金属性Cl>F
查看答案和解析>>
科目: 来源:2013-2014学年四川省高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
常温下,在某200 mL的稀硫酸和稀硝酸的混合溶液中逐量地加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。(设硝酸只被还原为NO气体, Fe的相对原子质量为56)。下列有关分析错误的是
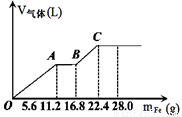
A、原混合酸中NO3-的物质的量为0.2 mol
B、原混合酸中H2SO4物质的量浓度为2mol/L
C、OA段与BC段反应中电子转移的物质的量之比为2:1
D、取20mL原混合酸加水稀释至1L后溶液的pH=1
查看答案和解析>>
科目: 来源:2013-2014学年四川省高三上学期第三次月考理综化学试卷(解析版) 题型:填空题
A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示) 。 (2)由A、B两种元素以原子个数比5∶1形成离子化合物X,X的电子式为 。
(3)由A、B元素形成的化合物B2A4可以与O2、KOH溶液形成原电池,该原电池负极的电极反应式为 。
(4)①若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式: 。②若E是非金属元素,其单质在电子工业中有重要应用,其氧化物晶体中E原子的杂化方式为 。 (5)由A、C、D、F四种元素形成的化合物Y(DAFC3)(已知A2FC3的Ka1=1.3×10-2、Ka2=6.3×10-8),则Y溶液中各离子浓度由大到小的顺序为 ;向Y溶液中加入一定量的NaOH,使溶液中c(AFC3-)=c(FC32-),则此时溶液呈 (填“酸性”、“碱性”或“中性”);用惰性电极电解Y的水溶液,阳极无气体产生,阳极的电极反应式为 。
查看答案和解析>>
科目: 来源:2013-2014学年四川省高三上学期第三次月考理综化学试卷(解析版) 题型:填空题
(1)Fe3+可以与SCN-、CN-、F-、有机分子等形成很多的配合物。
①写出基态Fe3+的核外电子排布式 。
②已知(CN)2是直线型分子,并有对称性,则(CN)2中π键和σ键的个数比为 。
③下图是SCN-与Fe3+形成的一种配合物,画出该配合物中的配位键(以箭头表示)。
④F-不仅可与Fe3+形成[FeF6]3+,还可以与Mg2+、K+形成一种立方晶系的离子晶体(如下图)。该晶体的化学式为 。


(2)氨气是一种重要的化工原料。
①液氨和水类似,也能发生电离:NH3+NH3 NH4++NH2-,其离子积常数为l.0×l0-30。现将2.3g金属钠投入1.0 L液氨中,钠完全反应生成NaNH2,假设溶液的体积不变,所得溶液中NH4+的浓度
NH4++NH2-,其离子积常数为l.0×l0-30。现将2.3g金属钠投入1.0 L液氨中,钠完全反应生成NaNH2,假设溶液的体积不变,所得溶液中NH4+的浓度
为 。
②已知:N2(g)+O2(g)=2NO(g) △H=+180kJ·mol-l
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-908 kJ·mol-l
写出氨气被一氧化氮氧化生成氮气和气态水的热化学方程式: 。
(3)在下图装置中,若通电一段时间后乙装置左侧电极质量增加。

①下列说法错误的是 ;
A.乙中左侧电极反应式:Cu2++2e-=Cu
B.电解一段时间后,装置丙的pH减小
C.向甲中通人适量的HCl气体,可使溶液恢复到电解前的状态
D.电解一段时间后,向乙中加入0.1molCu(OH)2可使电解质溶液复原,则电路中通过的电子为0.2mol②若将甲中溶液换成MgCl2,则电解总反应的离子方程式为 ;
③若Cu电极上质量增加2.16 g, 甲溶液体积为200mL, 则甲溶液的pH= 。
查看答案和解析>>
科目: 来源:2013-2014学年四川省高三上学期第三次月考理综化学试卷(解析版) 题型:填空题
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
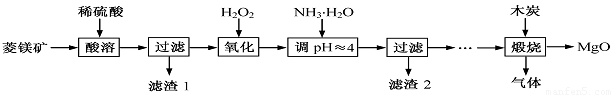 (1)MgCO3与稀硫酸反应的离子方程式为
。
(1)MgCO3与稀硫酸反应的离子方程式为
。
(2)加入H2O2氧化时,发生反应的化学方程式为 。(3)滤渣2的成分是 (填化学式)。
(4)煅烧过程存在以下反应:2MgSO4+C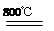 2MgO+2SO2↑+CO2↑、MgSO4+C
2MgO+2SO2↑+CO2↑、MgSO4+C MgO+SO2↑+CO↑、 MgSO4+3C
MgO+SO2↑+CO↑、 MgSO4+3C MgO+S↑+3CO↑。
MgO+S↑+3CO↑。
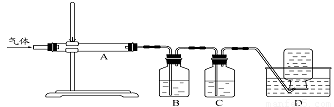
利用上图装置对煅烧产生的气体进行分步吸收或收集。
①D中收集的气体是 (填化学式)。
②B中盛放的溶液可以是 (填字母)。
a.NaOH 溶液 b.Na2CO3溶液 c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式: 。
查看答案和解析>>
科目: 来源:2013-2014学年四川省高三上学期第三次月考理综化学试卷(解析版) 题型:填空题
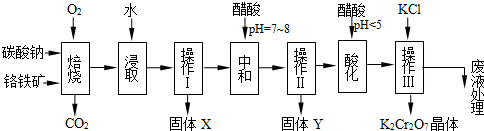
铬铁矿的主要成分可表示为FeO·Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:
已知:①4FeO·Cr2O3+ 8Na2CO3+
7O2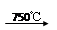 8Na2CrO4
+ 2 Fe2O3 + 8CO2↑;
8Na2CrO4
+ 2 Fe2O3 + 8CO2↑;
②Na2CO3
+ Al2O3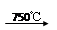 2NaAlO2
+ CO2↑;③ Cr2O72-+ H2O
2NaAlO2
+ CO2↑;③ Cr2O72-+ H2O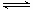 2CrO42- +
2H+
2CrO42- +
2H+
(1)固体X中主要含有_________(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用__________(填写仪器或试剂名称)。
(2)酸化步骤用醋酸调节溶液pH<5,其目的是_________________________________。
|
物质 |
溶解度/(g/100g水) |
||
|
0°C |
40°C |
80°C |
|
|
KCl |
28 |
40.1 |
51.3 |
|
NaCl |
35.7 |
36.4 |
38 |
|
K2Cr2O7 |
4.7 |
26.3 |
73 |
|
Na2Cr2O7 |
163 |
215 |
376 |
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、 、
过滤、_______、干燥。
(4)右表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl。该反应在溶液中能发生的理由是_______________。
(5)酸性溶液中过氧化氢能使Cr2O72-生成蓝色的过氧化铬(CrO5分子结构为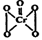 ),
该反应可用来检验Cr2O72-的存在。写出反应的离子方程式:
。
),
该反应可用来检验Cr2O72-的存在。写出反应的离子方程式:
。
该反应 (填“属于”或“不属于”)氧化还原反应。
(6)称取重铬酸钾试样2.500g配成250mL溶液,取出25mL与碘量瓶中,加入10mL2mol/ L H2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min。然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O32—=2I-+S4O62—)。
①判断达到滴定终点的依据是 ;
②若实验中共用去Na2S2O3标准溶液40.00mL,则所得产品中重铬酸钾的纯度为 。(保留3位有效数字, K2Cr2O7的摩尔质量为294g/mol)。
查看答案和解析>>
科目: 来源:2013-2014学年四川省绵阳市高三”二诊“模拟测试(一)化学试卷 (解析版) 题型:选择题
十八大报告中提出“大力推进生态文明建设,提高生态文明水平,建设美丽中国”。化学已渗透到人类生活的各个方面。下列说法正确的是
A.PM2.5是指大气中直径≤2.5微米的颗粒物,只要戴普通口罩就对人体健康无影响
B.垃圾是放错地方的资源,应分类回收利用
C.高纯度的硅单质广泛用于制作光导纤维,光导纤维是新型高分子非金属结构材料
D.地沟油的主要成分是高级脂肪酸甘油酯,可用于制肥皂和加工食用油
查看答案和解析>>
科目: 来源:2013-2014学年四川省绵阳市高三”二诊“模拟测试(一)化学试卷 (解析版) 题型:选择题
下列说法正确的是
A.电解质溶液能导电,是因为在通电时电解质电离产生了自由移动的离子
B.饱和石灰水中加入少量CaO,恢复至室温后溶液的pH值不变
C.将AlCl3溶液和Na2SO3溶液分别蒸干并灼烧,得到Al2O3和Na2SO3
D.pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液,则溶液浓度大小关系:
c(CH3COONa)> c(Na2CO3)> c(C6H5ONa)>c(NaOH)
查看答案和解析>>
科目: 来源:2013-2014学年四川省绵阳市高三”二诊“模拟测试(一)化学试卷 (解析版) 题型:选择题
下列离子方程式书写正确的是
A.将过量的NaOH溶液滴入同浓度的少量Ca(HCO3)2溶液中Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-
B.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全Ba2++OH-+H++ SO42-=BaSO4↓+H2O
C.服用阿司匹林过量出现水杨酸( )反应,可静脉注滴NaHCO3溶液:
)反应,可静脉注滴NaHCO3溶液: +
2 HCO3- →
+
2 HCO3- → +
2 CO2↑ + 2 H2O
+
2 CO2↑ + 2 H2O
D.向FeI2溶液中加少量氯水 2Fe2++Cl2=2Fe3++2Cl-
查看答案和解析>>
科目: 来源:2013-2014学年四川省绵阳市高三”二诊“模拟测试(一)化学试卷 (解析版) 题型:选择题
若NA为阿伏加德罗常数的值,下列说法正确的是
A.NA个Fe(OH)3胶体粒子的质量为107g
B.8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA
C.标准状况下,将2.24L Cl2溶于水,可得到HClO分子的数目是0.1NA
D.2.3gNa与氧气完全反应,反应中转移的电子数介于0.1NA到0. 2NA之间
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com