
科目: 来源:2013-2014学年四川省眉山市高三第一次诊断性考试化学试卷(解析版) 题型:选择题
一定质量的镁、铝合金与硝酸溶液恰好完全反应,得硝酸盐溶液和NO2、N2O4、NO的混合气体,这些气体与标准状况下3.36L氧气混合后通入水中,所有气体恰好完全被水吸收生成硝酸。若向所得硝酸盐溶液中加入2mol/L NaOH溶液至沉淀最多时停止加入,将所产生沉淀滤出,向滤液加水稀释至500ml,此时所得溶液物质的量浓度为
A.0.5mol/L B.1mol/L C.1.2mol/L D.2mol/L
查看答案和解析>>
科目: 来源:2013-2014学年四川省眉山市高三第一次诊断性考试化学试卷(解析版) 题型:填空题
A~F均为元素周期表中前四周期元素,其相关信息如下表:
元素 相 关 信 息
A A的基态原子最外层电子排布式为2s22p3
B B是地壳中含量最高的元素
C C+与B的简单离子的电子层结构相同
D D的一种核素的质量数为64,中子数为35
E 、F E 、F既同周期又同族,且原子序数F比E多2
请回答下列问题:
(1)D的价电子的电子排布式是 ;F原子的原子结构示意图为 。
(2)A、B的第一电离能的大小顺序为 。
(3)AB3- 中A原子的杂化轨道类型为_______;与A2B互为等电子体的分子的分子式为 (任写一个即可)。
(4)D晶体的晶胞如图所示为面心立方最密堆积 (在晶胞 的顶点和面心均含有一个D原子)。则D的晶体中D原子的配位数为 。

(5)已知17gA的简单氢化物催化氧化生成气态水时放出QkJ的热量,请写出A的简单氢化物催化氧化的热化学反应方程式 。
(6)C2B2的电子式为____;它可与E的二氯化物溶液反应,若反应的C2B2与E的二氯化物的物质的量之比为1:2,则该反应的化学反应方程式为 。
查看答案和解析>>
科目: 来源:2013-2014学年四川省眉山市高三第一次诊断性考试化学试卷(解析版) 题型:填空题
化学反应原理在科研和生产中有广泛应用。
Ⅰ、如图装置所示,A、B中的电极为多孔的惰性电极;C、D为夹在浸有Na2SO4溶液的滤纸条上的铂夹;电源有a、b两极。若A、B中充满KOH溶液后倒立于KOH溶液的水槽中。切断K1,闭合K2、K3通直流电。

回答下列问题:
(1) a是电源的 极,写出A中的电极反应式为_____。
(2)湿的Na2SO4滤纸条上能观察到的现象有____________。
(3)电解一段时间后,A、B中均有气体包围电极,若此时切断K2、K3,闭合K1,发现电流表的指针移动,写出此时B中的电极反应式为 。
Ⅱ、甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列反应合成甲醇:CO(g)+2H2(g)
 CH3OH(g)
ΔH,下表所列数据是该反应在不同温度下的化学平衡常数(K)。请回答下列问题:
CH3OH(g)
ΔH,下表所列数据是该反应在不同温度下的化学平衡常数(K)。请回答下列问题:
|
温度 |
250℃ |
300℃ |
350℃ |
|
K |
2.041 |
0.270 |
0.012 |
(4)由表中数据判断ΔH 0(填“>”、“<”或“=”)。
(5)其他条件不变,只改变其中一个条件,下列措施可提高甲醇产率的是 。
A.升高温度;B.使用合适的催化剂;C.缩小容器的容积;D.充入过量的H2;E.恒压时,充入He;F.从体系中分离出CH3OH
(6)某温度下,将2mol CO和6 mol H2充入2L密闭容器中,反应进行到4min末达到平衡,此时测得c(CO) =0.2 mol/L ,则0~4min内H2的反应速率为 ;若保持温度容积不变再向其中充入一定量的CH3OH,重新达到化学平衡状态,与原平衡状态相比,此时平衡混合气体中CH3OH的体积分数 (填“变大”、“变小”、或“不变”)。
查看答案和解析>>
科目: 来源:2013-2014学年四川省眉山市高三第一次诊断性考试化学试卷(解析版) 题型:实验题
根据Mg能在CO2中燃烧,某兴趣小组推测Na应该也能在CO2中燃烧,且固体产物可能为C、Na2O和Na2CO3中的两种或三种。该小组用如下图装置进行了实验探究。已知PdCl2能被CO还原得到黑色的Pd。

回答下列问题:
(1)为了使反应随开随用,随关随停,上图虚线方框内应选用 装置(填下图字母代号),如何检验所选装置的气密性 。

(2)装置2中所盛试剂为 。
A.NaOH溶液 B.饱和NaHCO3溶液
C.饱和Na2CO3溶液 D.饱和NaCl溶液
(3)检测装置的气密性完好并装好药品后,在点燃酒精灯前应先进行装置1中的反应操作,待观察到 现象时,再点燃酒精灯,这步操作的目的是 。
(4)由实验现象和进一步的探究得出反应机理。
A.装置6中有黑色沉淀生成;
B.取反应后直玻管中的固体物质23.0g溶于足量的水中,无气泡产生且得到澄清的溶液;将溶液加水稀释配成250 mL的溶液;
C.取25.00ml步骤B的溶液,滴加足量BaCl2溶液,将生成的白色沉淀过滤、洗涤、干燥,称量得固体质量为1.97g。
①步骤C中不溶物干燥前必须经过洗涤,如何检验该沉淀是否洗涤干净 。
②该探究得出钠与二氧化碳反应的化学方程式为 。
查看答案和解析>>
科目: 来源:2013-2014学年四川省眉山市高三第一次诊断性考试化学试卷(解析版) 题型:填空题
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。目前我国已经在技术上取得突破——从硫酸渣中分离出各种成分并加以利用。其流程和相关数据如下:

查资料得知:
|
物质名称 |
溶度积(Ksp) |
pH值 |
|
|
开始沉淀 |
完全沉淀 |
||
|
Mg(OH)2 |
5.6×10-12 |
9.3 |
10.8 |
|
Fe(OH)3 |
2.8×10-16 |
2.7 |
3.7 |
|
Al(OH)3 |
1.3×10-33 |
3.7 |
4.7 |
请回答下列问题:
(1)写出固体A的化学式为 。
(2)若要测定溶液的pH是否达到3.7,下列实验用品中可选用的是 。
A.石蕊试液 B.广泛pH试纸 C.精密pH试纸 D.pH计
(3)完成下列离子反应方程式
①溶液D生成固体E ; ②溶液F生成固体G 。
(4)要将固体C、固体E和固体G都转化为相应的稳定氧化物,需进行的实验操作为 。
(5)若不考虑溶液体积的变化,请计算溶液H中c(Mg2+)= 。
查看答案和解析>>
科目: 来源:2013-2014学年四川省高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
下列措施有利于节能减排、改善环境质量的有
① 发展核电,以减少火力发电带来的二氧化硫和二氧化碳排放问题
② 积极推行“限塑令”,加快研发利用二氧化碳合成的聚碳酸酯类可降解塑料
③ 加速建设地铁、轻轨等轨道交通,减少汽车尾气排放
④ 发展低碳经济、循环经济,推广可利用太阳能、风能的城市照明系统
⑤ 使用生物酶降解生活废水中的有机物,使用填埋法处理未经分类的生活垃圾
A.①②③④ B. ①②⑤ C. ①②④⑤ D. ③④⑤
查看答案和解析>>
科目: 来源:2013-2014学年四川省高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 0.2mol铁粉与足量水蒸气反应生成的H2分子数为0.3NA
B. 常温常压下,0.1mol Na2O2与CO2完全反应转移电子数为0.1NA
C. 50mL18.4mol·L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA
D. 某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA
查看答案和解析>>
科目: 来源:2013-2014学年四川省高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
下列物质转化在给定条件下能实现的是
①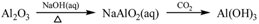
②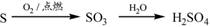
③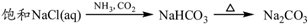
④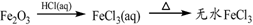
⑤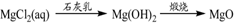
A. ①③⑤ B. ②③④ C. ②④⑤ D. ①④⑤
查看答案和解析>>
科目: 来源:2013-2014学年四川省高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
下列相关反应的离子方程式书写错误的是
A.在强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4:3ClO—+4OH—+2Fe(OH)3=3Cl—+5H2O+2FeO42—
B.少量SO2通入苯酚钠溶液中:2C6H5O—+SO2+H2O=2C6H5OH+SO32—
C.0.01mol·L-1NH4Al(SO4)2溶液与0.02mol·L-1Ba(OH)2溶液等体积混合:
NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O
D.少量SO2通入NaClO溶液中:SO2 + ClO—+ OH—= SO42— + Cl— + H+
查看答案和解析>>
科目: 来源:2013-2014学年四川省高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
一定温度下,将1molA和1molB气体充入2L恒容密闭容器,发生反应A(g)+ B(g)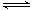 xC(g)+D(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示。下列说法正确的是
xC(g)+D(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示。下列说法正确的是
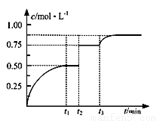
A.反应方程式中的x=1
B.t2时刻改变的条件是使用催化剂
C.t3时刻改变的条件是移去少量物质D
D.t1~t3间该反应的平衡常数均为4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com