
科目: 来源:2012-2013学年陕西省延安市秋高考模拟理综化学试卷(解析版) 题型:填空题
“神七”登天标志着我国的航天事业进入了新的篇章。
(1)火箭升空时,由于与大气层的剧烈摩擦,产生高温。为了防止火箭温度过高,在火箭一面涂上一种特殊的涂料,该涂料的性质最可能的是 。
A.在高温下不融化 B.在高温下可分解气化
C.在常温下就分解气化 D.该涂料不可能发生分解
(2)火箭升空需要高能的燃料,经常是用N2O4和N2H4和作为燃料,其反应的方程式是:N2O4+N2H4→N2+H2O。请配平该反应方程式: N2O4+ N2H4→ N2+ H2O
该反应中被氧化的原子与被还原的原子的物质的量之比是 。这个反应应用于火箭推进器,除释放大量的热和快速产生大量气体外,还有一个很大的优点是 。
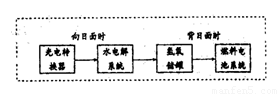
(3)如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,燃料电池放电时的负极反应为: 。如果某段时间内氢氧储罐中共收集到33.6L气体(已折算成标况),则该段时间内水电解系统中转移电子的物质的量为 mol。
(4)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料。 已知该反应的阳极反应为:4OH—4e-=O2↑+2H2O 则阴极反应为: 。有人提出,可以设计反应2CO=2C+O2(△H>0、△S<0)来消除CO的污染。请你判断上述反应是否能发生? 理由 。
(5).北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。丙烷脱氢可得丙烯。
已知:① C3H8(g)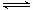 CH4(g)+HC≡CH(g)+H2(g);
△H1=156.6 kJ·mol-1
CH4(g)+HC≡CH(g)+H2(g);
△H1=156.6 kJ·mol-1
②CH3CH=CH2(g)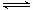 CH4(g)+
HC≡CH (g);△H2=32.4 kJ·mol-1
CH4(g)+
HC≡CH (g);△H2=32.4 kJ·mol-1
则相同条件下,反应C3H8(g)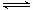 CH3CH=CH2(g)+H2(g)的△H=_____kJ·mol-1
CH3CH=CH2(g)+H2(g)的△H=_____kJ·mol-1
查看答案和解析>>
科目: 来源:2012-2013学年陕西省延安市秋高考模拟理综化学试卷(解析版) 题型:填空题
氮是地球上含量最丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)右图是1 mol NO2和1mol
CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式
。
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g)
 2NH3(g)△H<0其化学平衡常数K与温度t的关系如右表:请完成下列问题;
2NH3(g)△H<0其化学平衡常数K与温度t的关系如右表:请完成下列问题;
|
t/℃ |
200 |
300 |
400 |
|
K |
K1 |
K2 |
0.5 |
①试比较K1、K2的大小,K1____K2(填写“>”、“=”或“<”)
②下列各项能作为判断该反应达到化学平衡状态的依据是____一(填序号字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
③400℃时,反应2NH3(g)  N2(g)+3H2(g)的化学平衡常数的值为 。当测得NH3和N2、H2的物质的量分别为3mol和2mol、1mol时,则该反应的v(N2)正 __
v(N2)逆(填写“>”、“=”或“<”=)
N2(g)+3H2(g)的化学平衡常数的值为 。当测得NH3和N2、H2的物质的量分别为3mol和2mol、1mol时,则该反应的v(N2)正 __
v(N2)逆(填写“>”、“=”或“<”=)
查看答案和解析>>
科目: 来源:2012-2013学年陕西省延安市秋高考模拟理综化学试卷(解析版) 题型:填空题
2010年上海世博会场馆,大量的照明材料或屏幕都使用了发光二极管(LED)。目前市售LED品片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、lnGaN(氮化铟镓)为主。已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如图。

试回答:
⑴镓的基态原子的电子排布式是 。
⑵砷化镓晶胞中所包含的砷原子(白色球)个数为 ,与同一个镓原子相连的砷原子构成的空间构型为 。
⑶N、P、As处于同一主族,其氢化物沸点由高到低的顺序是 。 (用氢化物分子式表示)
⑷砷化镓可由(CH3)3Ga和AsH3在700℃时制得。(CH3)3Ga中镓原子的杂化方式为 。
⑸比较二者的第一电离能:As______Ga(填“<”、“>”或“=”)。
⑹下列说法正确的是 (填字母)。
A.砷化镓晶胞结构与NaCl相同 B.GaP与GaAs互为等电子体
C.电负性:As>Ga D.砷化镓晶体中含有配位键
查看答案和解析>>
科目: 来源:2012-2013学年陕西省延安市秋高考模拟理综化学试卷(解析版) 题型:填空题
Ⅰ.2009年墨西哥、美国等地出现甲型H1N1流感疫情,引起全世界的关注,这种流感疫情是由甲型H1N1病毒引起的。美国疾病控制和预防中心推荐使用瑞士罗氏制药公司生产的“达菲”胶囊和英国葛兰素—史克公司生产的喷雾式药剂“乐感清”两款药物。
达菲和乐感清的结构简式如下图所示:


请回答下列问题:
(1)乐感清的分子式是____ 。
(2)合成达菲的主要原料莽草酸(结构简式为 
 )存在于我国盛产的八角茴香中。关于莽草酸性质的描述,下列说法正确的是( )
)存在于我国盛产的八角茴香中。关于莽草酸性质的描述,下列说法正确的是( )
A. 1 mol莽草酸与足量的金属钠反应可生成4mol H2。
B. 1 mol莽草酸与足量氢氧化钠溶液反应,最多可消耗氢氧化钠4 mol。
C. 1 mol莽草酸与足量的碳酸钠溶液反应可生成二氧化碳气体1 mol。
D. 1 mol莽草酸与足量的碳酸氢钠溶液反应可生成二氧化碳气体1 mol
(3)下列每组中各有三对物质,它们都能用分液漏斗分离的是
A.乙酸乙酯和水,酒精和水,植物油和水
B.四氯化碳和水,溴苯和水,硝基苯和水
C.甘油和水,乙酸和水,乙酸和乙醇
D.汽油和水,苯和水,乙二醇和水
Ⅱ.下图中A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3溶液发生反应,C和D的相对分子质量相等,且E为无支链的化合物。请回答下列问题:
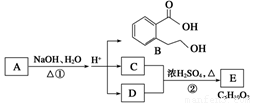
(1)C分子中官能团的名称是 ;化合物B不能发生的反应是 (填字母序号)。
a.加成反应 b.取代反应 c.消去反应
d.酯化反应 e.水解反应 f.氧化反应
(2)反应②的化学方程式是___________________________。(3) A的结构简式是_________________。
(4)同时符合下列三个条件的B的同分异构体的数目有______个。
a含有间二取代苯环结构 b.属于非芳香酸酯 c.可与FeCl3溶液发生显色反应
写出其中任意一个同分异构体的结构简式__________________________________。
查看答案和解析>>
科目: 来源:2013-2014学年上海市高三上学期第三次月考化学试卷(解析版) 题型:选择题
化学在生产和日常生活中有着重要的应用。下列说法不正确的是
A.K2FeO4能与水缓慢反应生成Fe(OH)3和O2,故可用作水的消毒剂和净化剂
B.钢铁表面烤蓝生成一层致密的Fe3O4,能起到防腐蚀作用
C.常温下氨能与氯气反应生成氯化氢和氮气,因此可用浓氨水检查氯气管道中某处是否泄漏
D.用氯气与乙烷混合光照获得纯净的1,2-二氯乙烷
查看答案和解析>>
科目: 来源:2013-2014学年上海市高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列关于纯净物、混合物、强电解质、弱电解质和非电解质的正确组合是( )
纯净物 混合物 强电解质 弱电解质 非电解质
A 胆矾 水煤气 硫酸 醋酸 干冰
B 氢氧化钡 蔗糖溶液 硫酸钡 醋酸 氢气
C 碱石灰 石灰水 苛性钾 水 氨气
D 石灰石 水玻璃 氯化钙 氢氧化铁 碳酸钙
查看答案和解析>>
科目: 来源:2013-2014学年上海市高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列有关物质结构和性质的叙述正确的是:
①具有16个质子、16个中子和18个电子的微粒符号可表示为:32 16S2-;
②羟基电子式为: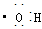 ;
;
③HClO的结构式:H—Cl—O;
④NaHCO3在水中的电离方程式:NaHCO3→Na++H++CO32-;
⑤Na2O的水溶液能导电,这不能说明Na2O是电解质;
⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,故SiO2是两性氧化物;
⑦分馏、干馏、裂化都是化学变化
A.①②⑤ B.①④⑥⑦ C.②③④⑥ D.②③⑤⑥⑦
查看答案和解析>>
科目: 来源:2013-2014学年上海市高三上学期第三次月考化学试卷(解析版) 题型:选择题
向FeCl3和BaCl2的混合液中通入过量SO2,有白色沉淀产生。下列说法正确的是
A.白色沉淀为BaSO3 B.该实验表明FeCl3有还原性
C.反应后溶液酸性增强 D.反应后滴加KSCN溶液显红色
查看答案和解析>>
科目: 来源:2013-2014学年上海市高三上学期第三次月考化学试卷(解析版) 题型:选择题
长式周期表共有18个纵行,从左到右排为1~18列,即碱金属为第1列,稀有气体元素为第18列。按这种规定,下列说法正确的是
A.第9列元素中有非金属元素
B.只有第二列的元素原子最外层电子排布为ns2
C.第四周期第8列元素是铁元素
D.第15列元素原子的最外层电子排布为ns2np5
查看答案和解析>>
科目: 来源:2013-2014学年上海市高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列物质性质的变化规律中与共价键键能大小有关的是
①F2、Cl2、Br2、I2的熔点、沸点逐渐升高;②HF、HCl、HBr、HI的热稳定性依次减弱
③金刚石的硬度、熔点、沸点都高于晶体硅;④NaF、NaCl、NaBr、NaI熔点依次降低
A.仅③ B.①③ C.②④ D.②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com