
科目: 来源:2014届江苏省扬州市高三上学期10月月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法一定正确的是( )
A.9.2 g C7H8和C3H8O3的混合物中所含氢原子总数为0.8NA
B.标准状况下,11.2 L C2H5OH中所含的分子数为0.5NA
C.将含0.1 mol FeCl3的溶液滴加到沸水中完全水解可生成0.1NA个Fe(OH)3胶粒
D.0.1 mol Na2O2参加反应转移的电子数目是0.2NA
查看答案和解析>>
科目: 来源:2014届江苏省扬州市高三上学期10月月考化学试卷(解析版) 题型:选择题
下列物质转化在给定条件下不能实现的是( )
①Si SiO2
SiO2 H2SiO3;②S
H2SiO3;②S SO3
SO3 H2SO4;③C
H2SO4;③C CO2
CO2 Na2CO3
Na2CO3
④MgCl2溶液 MgCl2·6H2O
MgCl2·6H2O Mg;⑤Na
Mg;⑤Na Na2O2
Na2O2 NaOH
NaOH
A.①②③ B.①②④ C.①②③④ D.①②③④⑤
查看答案和解析>>
科目: 来源:2014届江苏省扬州市高三上学期10月月考化学试卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A.向AlCl3溶液中滴加氨水:Al3++3OH-=Al(OH)3↓
B.向NaHCO3溶液中加入少量Ca(OH)2溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O
C.向苯酚溶液中滴加Na2CO3溶液: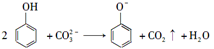
D.向氯化亚铁溶液中滴加稀硝酸:3Fe2++4H++ NO3-=3Fe3++NO↑+2H2O
查看答案和解析>>
科目: 来源:2014届江苏省扬州市高三上学期10月月考化学试卷(解析版) 题型:选择题
下列图示与对应的叙述不相符的是( )
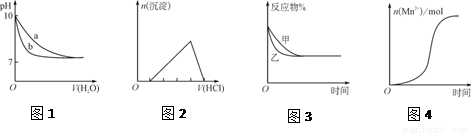
A.图1表示相同温度下,向pH=10的氢氧化钠溶液和氨水中分别加水稀释时pH的变化曲线,其中a表示氨水稀释时pH的变化曲线
B.图2表示向含有少量氢氧化钠的偏铝酸钠溶液中滴加盐酸所得沉淀物质的量与盐酸体积的关系
C.图3表示压强对可逆反应CO(g)+H2O(g)  CO2(g)+H2(g)的影响,乙的压强比甲的压强大
CO2(g)+H2(g)的影响,乙的压强比甲的压强大
D.图4表示10 mL 0.01 mol·L-1KMnO4酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+)随时间的变化(Mn2+对该反应有催化作用)
查看答案和解析>>
科目: 来源:2014届江苏省扬州市高三上学期10月月考化学试卷(解析版) 题型:选择题
贝诺酯是一种治疗类风湿性关节炎药物,其结构简式如右图所示(未表示出其空间构型)。下列关于贝诺酯的描述正确的是( )

A.贝诺酯的分子式为C17H15NO5
B.贝诺酯中含有3种含氧官能团
C.贝诺酯能使溴水和酸性高锰酸钾溶液都褪色
D. 1 mol贝诺酯最多可以消耗9 mol H2
查看答案和解析>>
科目: 来源:2014届江苏省扬州市高三上学期10月月考化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W的原子序数依次增大,元素X的原子半径最小,Y元素和X元素在一定条件下能形成YX,Z和W的原子序数相差8,W原子的电子总数是其电子层数的5倍。下列叙述正确的是( )
A.Y可用于制造高性能可充电电池
B.WX3的沸点高于ZX3
C.Z的最高价含氧酸的酸性强于W的最高价含氧酸的酸性
D.原子半径的大小顺序:rW>rZ>rY>rX
查看答案和解析>>
科目: 来源:2014届江苏省扬州市高三上学期10月月考化学试卷(解析版) 题型:选择题
下列根据实验操作和现象所得出的结论不正确的是( )
选项 实验操作 实验现象 结论
A 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 2 min后,试管里出现凝胶 酸性:盐酸>硅酸
B 在酒精灯上加热铝箔 铝箔熔化但不滴落 熔点:氧化铝>铝
C 常温下,向浓硫酸中投入铁片 铁片不溶解 常温下,铁不与浓硫酸反应
D 向某溶液中先滴加KSCN溶液,再滴加少量氯水 先无明显现象,后溶液变成血红色 溶液中含有Fe2+,没有Fe3+
查看答案和解析>>
科目: 来源:2014届江苏省扬州市高三上学期10月月考化学试卷(解析版) 题型:选择题
常温下,向10 mL 0.1 mol·L-1的H2C2O4溶液中逐滴加入0.1 mol·L-1 KOH溶液,所得滴定曲线如图所示。下列说法正确的是( )

A.KHC2O4溶液呈弱碱性
B.B点时:c(K+)>c(HC2O4-)>c(H+)>c(OH-)
C.C点时:c(HC2O4-)+c(C2O42-)+c(H2C2O4)<c(K+)<c(HC2O4-)+2c(C2O42-)+c(H2C2O4)
D.D点时:c(H+)+c(HC2O4-)+c(H2C2O4)=c(OH-)
查看答案和解析>>
科目: 来源:2014届江苏省扬州市高三上学期10月月考化学试卷(解析版) 题型:选择题
在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
|
容器 |
甲 |
乙 |
|
反应物投入量 |
1 mol N2、3 mol H2 |
4 mol NH3 |
|
NH3的浓度(mol·L-1) |
c1 |
c2 |
|
反应的能量变化 |
放出a kJ |
吸收b kJ |
|
气体密度 |
ρ1 |
ρ2 |
|
反应物转化率 |
α1 |
α2 |
 (已知N2(g)+3H2(g)
2NH3(g);ΔH=-92.4 kJ·mol-1),下列说法正确的是(
)
(已知N2(g)+3H2(g)
2NH3(g);ΔH=-92.4 kJ·mol-1),下列说法正确的是(
)
A.c1<c2<2c1 B.a+b>92.4 C.α1+α 2=1 D.ρ2=2ρ1
查看答案和解析>>
科目: 来源:2014届江苏省扬州市高三上学期10月月考化学试卷(解析版) 题型:填空题
工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量CaO、FeO、CuO、NiO等氧化物)制取金属锌的流程如图所示。回答下列问题:

(1)酸浸时ZnFe2O4会生成两种盐,该反应的化学方程式为___________。
(2)净化Ⅰ操作分为两步:第一步是将溶液中少量的Fe2+氧化;第二步是控制溶液pH,使Fe3+转化为Fe(OH)3沉淀。
①写出酸性条件下H2O2与Fe2+反应的离子方程式:___________。
②25 ℃时,pH=3的溶液中,c(Fe3+)=________mol·L-1(已知25 ℃,Ksp[Fe( OH)3]=4.0×10-38)。
③净化Ⅰ生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是____________________。
(3)若没有净化Ⅱ操作,则对锌的制备带来的影响是_________________。
⑷本流程中可以循环利用的物质除锌外还有________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com