
科目: 来源:2014届天津市高三上学期第一次月考化学试卷(解析版) 题型:选择题
当0.2mol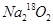 足量CO2完全反应后所得固体的质量为(
)
足量CO2完全反应后所得固体的质量为(
)
A.21.2g B.21.6g C.22.0g D.22.4g
查看答案和解析>>
科目: 来源:2014届天津市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列离子方程式不正确的是( )
A.三氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+2H2O+4NH4+
B.4mol/L的NaAlO2溶液和7mol/L的HCL等体积互相均匀混合:4 AlO2-+7H++H2O=3Al(OH)3↓+Al3+
C.在Mn2+溶液中加入HNO3再加入PbO2.得紫红色溶液:5PbO2+2Mn2++4H+=5 Pb2++2MnO4-+2H2O
D.将0.lmol/LNa2CO3 溶液数滴缓缓滴入O.lmol/L 25mL盐酸中2H++CO32-=CO2↑+H2O
查看答案和解析>>
科目: 来源:2014届天津市高三上学期第一次月考化学试卷(解析版) 题型:填空题
元素周期表是人们研究物质性质的重要工具,下表是元素周期表的一部分,请用化学用语回答下列问题:
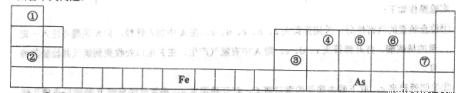
(1)①—⑦号元素原子半径最大的是____,最高价氧化物对应的水化物物酸性最强的是________________.
(2)写出由①-⑦号元素中的几种组成显碱性的盐的化学式____________________。(写出2种即可),并用离子方程式表示其中一种显碱性的原因____________________.
(3)写出③号元素的最高价氧化物与①-⑦号元素中金属性最强的元素的最高价氧化物的水化物反应的离子方程式_____________________。
(4) As在元素周期表中的位置是________________。
⑸As的原子结构示意图为________,其氢化物的电子式为___________.
(6)Y是由②⑥⑦三种元素组成,它的水溶液是一种生活中常见的消毒剂。As可以与Y的水溶液反应,生成其最高价含氧酸(H3AsO4 ),写出该反应的离子方程式_____________________,
当消耗1mol还原剂时转移电子的物质的量为______________________。
查看答案和解析>>
科目: 来源:2014届天津市高三上学期第一次月考化学试卷(解析版) 题型:实验题
实验题:I、下列方法适用于实验室中制备氨气的是____________________
A.固态氯化铵加热分解 B.向固体氢氧化钠中滴加浓氨水
C.氯化铵溶液与氢氧化钠溶液共热 D.固体氯化铵与氢氧化钙固体混合加热
II、为了在实验室中利用工业原料制备少量氨气,有人设计了如图所示的装置(图中夹持装置均已略去)。
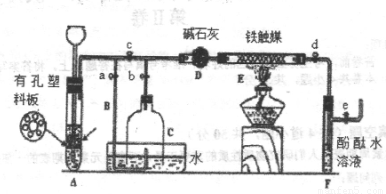
实验操作如下:
①检查装置的气密性后,关闭弹簧夹A.B.C.D.e。在A中加入锌粒,向长颈漏斗注入一定量的稀硫酸。打开弹簧夹C.D.e,则A中有氢气产生。在F出口处收集到氢气并检验其纯度。
②关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,如图所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③用酒精灯加热反应管E,继续通入氢气,待无底细口瓶C内水位下降到液面保持不变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。
请回答下列问题:
(1)写出反应管E中发生反应的化学方程式_______________________________________
用方程式解释F中溶液变红的原因______________________________________________
(2)C瓶内水位下降到液面保持不变时,A装置内发生的现象为____________________________,防止了实验装置中压强过大。此时再打开弹簧夹b的原因是_____________________________________,,C中气体的主要成分为.__________________________________________.
(3)为什么用酒精灯加热反应管E-段时间后再打开弹簧夹b____________________________
(4)为什么F装置不用防倒吸的装置_________________________________________________
查看答案和解析>>
科目: 来源:2014届天津市高三上学期第一次月考化学试卷(解析版) 题型:填空题
加碘食盐中通常加入的是KIO3,该物质在酸性条件下表现出较强的氧化性,可以和碘化物、亚硫酸盐等还原性物质发生反应。
(1)写出KIO3与KI在稀硫酸介质中发生反应的离子方程式______________________
(2)为测定菜加碘盐中碘元素的含量,某学生甲设计了如下实验:
A.准确称取wg食盐,使其完全溶解在适量的蒸馏水中;
B.用稀硫酸酸化所得溶液,加入过量的KI溶液,使其充分反应;
C.以___________________为指示剂,运滴加入物质的量浓度为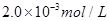 的硫代硫酸钠溶液10.0mL,恰好完全反应,判断反应完全的实验现象为____________________________________,则该加碘盐样品中碘元素的含量为______________________mg/Kg(用含w的代数式表示)。
的硫代硫酸钠溶液10.0mL,恰好完全反应,判断反应完全的实验现象为____________________________________,则该加碘盐样品中碘元素的含量为______________________mg/Kg(用含w的代数式表示)。
(已知: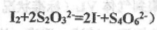 )
)
(3)某学生乙又进行了下列实验:
A.准确称取1.0g纯净的NaCl,加3mL蒸馏水配成溶液,溶液为无色;
B.滴入5滴指示剂和1mL 0.lmol/L Kl溶液,充分振荡,溶液不变化;
C.继续滴加l滴1mol/L的硫酸溶液,充分振荡,溶液变蓝色
推测实验中产生蓝色现象的原因,用离子方程式表示________________________
根据学生乙的实验结果,请对学生甲的实验结果进行分________________________(偏大、偏小、正确),其原因是________________________________________________.
查看答案和解析>>
科目: 来源:2014届天津市高三上学期第一次月考化学试卷(解析版) 题型:填空题
生铁中一般含有化合物B,B只有两种元素组成,它的含量、形状、分布对生铁性能影响很大,使生铁硬而脆,不宜进行机械加工。已知:(1)E、F、H、I、P常温下为气体,H、I、P为单质,E是一种红棕色气体。(2)反应①②均为制备理想的绿色水处理剂Na2FeO4的方法,其中反应①在生成Na2FeO4同时还生成NaNO2和H2O。各物质之闻的转化关系如下图所示f图中部分生成物没有列出)。

请填写以下空白:
(1)用电子式表示F的形成过程_________________________________________
(2)按要求完成下列反应:__________________________________________
反应③的离子方程式为________________________________________
反应①的化学方程式为________________________________________
(3)反应②中氧化剂与还原剂的物质的量比为__________________________________
反应④中的氧化产物的化学式为_______________________________________
(4)实验室中检验C溶液中金属阳离子的常用方法是________________________
(5)如果A与B反应时生成E与F的物质的量比为13:1,则化合物B的化学式为__________
查看答案和解析>>
科目: 来源:2014届安徽六校教育研究会高三第一次联考化学试卷(解析版) 题型:选择题
在火星上工作的美国“勇气号”、“机遇号”探测车的一个重要任务就是收集有关Fe2O3及硫酸盐的信息,以证明火星上存在或曾经存在过水。以下叙述正确的是
A.铝热剂就是单指Fe2O3粉和铝粉的混合物
B.检验从火星上带回来的红色物质是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液
C.还原amol Fe2O3所需H2、Al、CO的物质的量之比为3:2:3
D.明矾属于硫酸盐,含结晶水,是混合物
查看答案和解析>>
科目: 来源:2014届安徽六校教育研究会高三第一次联考化学试卷(解析版) 题型:选择题
过氧化钠与CO2作用,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2↑。当0.2molNa2O2与足量CO2完全反应后,下表对生成物Na2CO3和O2的描述中正确的是
Na2CO3的质量 关于O2的描述
A 21.2g O2的摩尔质量是36g·mol-1
B 21.6g 生成标准状况下O2的体积为2.24L
C 21.6g O2的摩尔质量是34g·mol-1
D 22.4 g 生成标准状况下O2的体积为2.24mL
查看答案和解析>>
科目: 来源:2014届安徽六校教育研究会高三第一次联考化学试卷(解析版) 题型:选择题
向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是
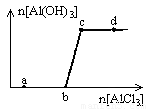
A.a点对应的溶液中:Na+、Fe3+、SO42-、HCO3-
B.b点对应的溶液中:Na+、S2-、SO42-、Cl-
C.c点对应的溶液中:Ag+、Ca2+、NO3-、F-
D.d点对应的溶液中:K+、NH4+、I-、CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com