
科目: 来源:2013-2014学年福建省四地六校高二上学期第二次月考化学试卷(解析版) 题型:选择题
对于反应3Fe(s)+4H2O(g)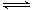 Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是
Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是
A.K=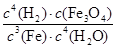
B.K=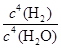
C.增大c(H2O)或减小c(H2),会使该反应平衡常数减小
D.改变反应的温度,平衡常数不一定变化
查看答案和解析>>
科目: 来源:2013-2014学年福建省四地六校高二上学期第二次月考化学试卷(解析版) 题型:选择题
下列事实不能用勒夏特列原理解释的是
A.开启啤酒瓶后,瓶中马上泛起大量泡沫
B.H2、I2、HI混合气体加压后颜色变深
C.红棕色的NO2加压后颜色先变深再变浅
D.工业上生产硫酸的过程中使用过量的空气,以提高二氧化硫的利用率
查看答案和解析>>
科目: 来源:2013-2014学年福建省四地六校高二上学期第二次月考化学试卷(解析版) 题型:填空题
如图为电解装置,X、Y为电极材料,a为电解质溶液。

(1)若a为含有酚酞的KCl溶液,X为Fe,Y为石墨,电解一段时间后:
X电极附近可观察到的实验现象是 ;
写出Y电极的电极反应式 。
(2)若要实现Cu +H2SO4=CuSO4+H2↑,
则Y电极材料是 ;
写出X电极的电极反应式 。
(3)若要利用该装置在铁制品表面镀上一层银,则a为 ,反应前两电极的质量相等,反应后电极质量相差2.16g,则该过程理论上通过电流表的电子数为 。
(4)若X、Y均为惰性电极,a为NaOH溶液,电解一段时间后,溶液的pH (填“增大”“不变”“减小”),若要使溶液恢复原来的状态,可往溶液中加入 。
查看答案和解析>>
科目: 来源:2013-2014学年福建省四地六校高二上学期第二次月考化学试卷(解析版) 题型:填空题
工业上合成氨的热反应方程式如下:N2(g)+3H2(g)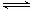 2NH3(g) △H=-92 kJ/mol
2NH3(g) △H=-92 kJ/mol
(1)若已知破坏1mol 键、H—H键键分别需吸收的能量为946 kJ、436 kJ,则断开1molN—H需吸收的能量为
kJ。
键、H—H键键分别需吸收的能量为946 kJ、436 kJ,则断开1molN—H需吸收的能量为
kJ。
(2)在恒温恒压的条件下,将2mol N2和6molH2通入一容积可变的容器中反应,达到平衡后气体的体积为反应前的75%,则该过程释放的能量为 kJ,氮气的转化率为 ,平衡后氨气占混合气体的体积分数为 。
(3)若将1mol N2和1molH2通入两个相同体积的密闭容器甲和乙中,甲容器保持温度和体积不变,乙容器保持温度和压强不变,经过一段时间后,两容器均达到平衡状态。
①建立平衡所需的时间:甲 乙(填“>”,“<”或“=”)
②达到平衡后氨气的体积分数:甲 乙(填“>”,“<”或“=”)
查看答案和解析>>
科目: 来源:2013-2014学年福建省四地六校高二上学期第二次月考化学试卷(解析版) 题型:填空题
向2L密闭容器中加入一定量的A、B、C三种气体,一定条件下发生反应,各物质的物质的量随时间变化如图甲所示[t0~15 s阶段n(B)未画出]。图乙为t2时刻后改变条件平衡体系中反应速率随时间变化的情况,且四个阶段所改变的外界条件均不同。已知t3~t4阶段为使用催化剂。观察下图,回答以下问题:

(1)甲图中从反应至达到平衡状态,生成物C的平均反应速率为____________________。
(2)图乙中t2时引起平衡移动的条件是______,t5时引起平衡移动的条件是_______。(填序号)
A.升高温度 B.增大反应物浓度 C.使用催化剂 D.减少体系压强
(3)图乙中表示平衡混合物中,在这四个阶段中C的物质的量最高的一段时间是______。(填序号): A.15s-t2时段 B.t3-t4时段 C.t4-t5时段 D.t6以后
(4)该反应的化学方程式可以表示为:_______________________________________________________,
正反应为______________(填“放热”或“吸热”)反应。
(5)反应开始时加入的B的物质的量为________________。
查看答案和解析>>
科目: 来源:2013-2014学年福建省四地六校高二上学期第二次月考化学试卷(解析版) 题型:填空题
研究NO2、SO2 、CO等大气污染气体的测量及处理具有重要意义。
(1)I2O5可使H2S、CO、HC1等氧化,常用于定量测定CO的含量。已知:
2I2(s)+5O2(g)=2I2O5(s) △H=-75.56 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H=-566.0 kJ·mol-1
写出CO(g)与I2O5(s)反应生成I2(s)和CO2(g)的热化学方程式: 。
(2)一定条件下,NO2与SO2反应生成SO3和NO两种气体:NO2(g)+SO2(g)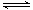 SO3(g)+NO(g)将体积比为1∶2的NO2、SO2气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
。
SO3(g)+NO(g)将体积比为1∶2的NO2、SO2气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1molSO2的同时生成1molNO
测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K= 。
(3)从脱硝、脱硫后的烟气中获取二氧化碳,用二氧化碳合成甲醇是碳减排的新方向。将CO2转化为甲醇的热化学方程式为:CO2
(g)+3H2(g)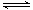 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
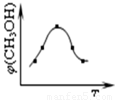
①取五份等体体积CO2和H2的的混合气体 (物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH) 与反应温度T的关系曲线如图所示,则上述CO2转化为甲醇反应的△H3 0(填“>”、“<”或“=”)。
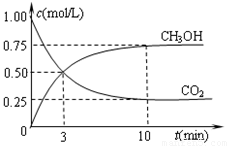
②在容积为1L的恒温密闭容器中充入1molCO2和3molH2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如下左图所示。若在上述平衡体系中再充0.5molCO2和1.5mol水蒸气(保持温度不变),则此平衡将 移动(填“向正反应方向”、“不”或“逆反应方向”)。
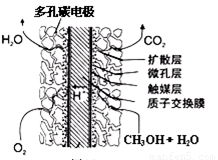
③直接甲醇燃料电池结构如上右图所示。其工作时负极电极反应式可表示为 。
查看答案和解析>>
科目: 来源:2013-2014学年福建省高二上学期期中联考化学试卷(解析版) 题型:选择题
全球变暖给我们敲响了警钟,地球正面临巨大的挑战,下列说法不正确的是( )
A.推进小火力发电站的兴建,缓解地方用电困难,促进地方经济的快速发展
B.推广“低碳经济”,减少温室气体的排放
C.推广“绿色自由”计划,吸收空气中的CO2并利用廉价能源合成汽油
D.利用晶体硅制作的太阳能电池可将太阳能直接转化为电能
查看答案和解析>>
科目: 来源:2013-2014学年福建省高二上学期期中联考化学试卷(解析版) 题型:选择题
下面各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )

A.②>①>③>④ B.④>②>①>③
C.④>②>③>① D.③>②>④>①
查看答案和解析>>
科目: 来源:2013-2014学年福建省高二上学期期中联考化学试卷(解析版) 题型:选择题
下列反应既是氧化还原反应,又是吸热反应的是( )
A.实验室制备氢气 B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的碳与水的反应 D.铝粉与氧化铁粉末反应
查看答案和解析>>
科目: 来源:2013-2014学年福建省高二上学期期中联考化学试卷(解析版) 题型:选择题
在一定条件下,A和B反应可生成C和D,其能量变化如下:

下列有关反应A+B=C+D的说法正确的是( )
A.反应前后原子的种类和数目可能改变
B.该反应若有热量变化,则一定是氧化还原反应
C.若该反应为放热反应,则不需加热反应就一定能进行
D.该反应遵循能量守恒,所以一定有能量变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com